
【題目】燃煤的煙氣中含有 SO2,為了治理霧霾天氣,工廠采用多種方法實現煙氣脫硫。
Ⅰ.(1)“濕式吸收法”利用吸收劑與 SO2 發生反應從而脫硫。下列試劑中適合用作該法吸收劑的是_____(填字母序號)。
a. 石灰乳 b.CaCl2溶液
(2)某工廠利用含 SO2 的煙氣處理含Cr2O72-的酸性廢水,吸收塔中反應后的鉻元素以Cr3+形式存在,具體流程如下:

①用 SO2 處理含鉻廢水時,利用了 SO2 的_____性。
②吸收塔中發生反應的離子方程式為_____。
Ⅱ.石灰-石膏法和燒堿法是常用的煙氣脫硫法。石灰-石膏法的吸收反應為Ca(OH)2+SO2= CaSO3↓+H2O。吸收產物亞硫酸鈣由管道輸送至氧化塔氧化,反應為2CaSO3+O2+4H2O =2CaSO4·2H2O。其流程如圖:

燒堿法的吸收反應為2NaOH+SO2=Na2SO3+H2O。該法的特點是氫氧化鈉堿性強、吸收快、效率高。其流程如圖:

已知:
試劑 | Ca(OH)2 | NaOH |
價格(元/kg) | 0.36 | 2.9 |
吸收 SO2 的成本(元/mol) | 0.027 | 0.232 |
(3)石灰-石膏法和燒堿法相比,石灰-石膏法的優點是_______,缺點是_______。
(4)某學習小組在石灰-石膏法和燒堿法的基礎上,設計一個改進的、能實現物料循環的煙氣脫硫方案,流程圖中的甲、乙、丙各是_____、_____、_____(填化學式)

【答案】a 還原 3SO2+Cr2O72-+2H+=2Cr3++3SO42-+H2O 原料便宜,成本低 吸收慢,效率低 NaOH Ca(OH)2 Na2SO3
【解析】
Ⅰ(1)二氧化硫與氯化鈣不能發生反應,而與氫氧化鈣可以反應生成亞硫酸鈣,因為氫氧化鈣溶解度不大,所以用石灰乳來吸收二氧化硫,故答案為:a;
(2)①重鉻酸根具有強氧化性,二氧化硫具有還原性,則可以用 SO2 處理含鉻廢水,故答案為:還原;
②吸收塔中為二氧化硫與重鉻酸根發生氧化還原反應,其發生反應的離子方程式為3SO2+Cr2O72-+2H+=2Cr3++3SO42-+H2O,故答案為:3SO2+Cr2O72-+2H+=2Cr3++3SO42-+H2O;
Ⅱ(3)對比兩個流程可知,基本反應原理都為二氧化硫與堿發生反應,氫氧化鈣原料廉價易得,成本低,但氫氧化鈣溶解度不大,吸收慢,效率低,故答案為:原料便宜,成本低;吸收慢,效率低;
(4)分析流程并對比前兩個流程可知,該流程的目的是改進前兩個流程的缺點,即氫氧化鈣吸收效率低,應用吸收效率較高的氫氧化鈉,則甲為氫氧化鈉,又氫氧化鈉成本高,需要循環利用,則可用氫氧化鈣制備氫氧化鈉,則乙為氫氧化鈣,由此可推知丙為亞硫酸鈉,亞硫酸鈉與氫氧化鈣可以發生復分解反應生成氫氧化鈉和亞硫酸鈣,實現氫氧化鈉的再生,降低成本,故答案為:NaOH;Ca(OH)2;Na2SO3。


 名校練考卷期末沖刺卷系列答案
名校練考卷期末沖刺卷系列答案科目:高中化學 來源: 題型:
【題目】常溫下,0.2mol/L一元酸HA與等濃度的NaOH溶液等體積混合后,所得溶液中部分微粒組分及濃度如圖所示,下列說法正確的是

A. HA是強酸
B. 該混合液pH=7
C. 圖中x表示HA,Y表示OH-,Z表示H+
D. 該混合溶液中:c(A-)+c(Y)=c(Na+)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某弱酸溶液中存在電離平衡HA![]() H++A-,下列敘述不正確的是:
H++A-,下列敘述不正確的是:
A. 溶液中離子濃度的關系滿足:c(H+) = c(OH-)+c(A-)
B. 常溫下,加入NaA固體可使HA的電離常數增大
C. HA溶液中加少量的NaA固體,平衡逆向移動
D. 0.10mol/L的HA溶液中加水稀釋,溶液中c(OH-)增大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某有機物的結構簡式如圖所示,Na、NaOH、NaHCO3分別與等物質的量的該物質恰好反應時,Na、NaOH、NaHCO3的物質的量之比為( )
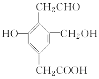
A. 3∶3∶2B. 3∶2∶1
C. 1∶1∶1D. 3∶2∶2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學小組采用如圖裝置,以環己醇制備環己烯:
密度(g/cm3) | 熔點(℃) | 沸點(℃) | 溶解性 | |
環己醇 | 0.96 | 25 | 161 | 能溶于水 |
環己烯 | 0.81 | -103 | 83 | 難溶于水 |
已知: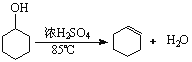
(1)制備粗品
將12.5mL環己醇加入試管A中,再加入1mL濃硫酸,搖勻后放入碎瓷片,緩慢加熱至反應完全,
在試管C內得到環己烯粗品。
①試管C置于冰水浴中的目的是 _____________________________________。
②導管B除了導氣外還具有的作用是____________,A中碎瓷片的作用是 ___________。
(2)制備精品
①環己烯粗品中含有環己醇和少量酸性雜質等。加入飽和食鹽水,振蕩、靜置、分層,環己烯在______ 層(填“上”或“下”),分液后用___________________(填入編號)洗滌。
A.KMnO4溶液 B.稀H2SO4 C.Na2CO3溶液
②再將環己烯按圖裝置蒸餾,冷卻水從________口進入。蒸餾時要加入生石灰,目的是:_________________________。
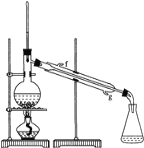
③收集產品時,控制的溫度應在________________左右,實驗制得的環己烯精品質量低于理論產量,可能的原因是 _______
A.蒸餾時從70℃開始收集產品
B.環己醇實際用量多了
C.制備粗品時環己醇隨產品一起蒸出
(3)以下區分環己烯精品和粗品的方法,合理的是_______
A.用酸性高錳酸鉀溶液 B.用金屬鈉 C.測定沸點
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機物I(分子式為C19H20O4)屬于芳香酯類物質,是一種調香劑,其合成路線如下:
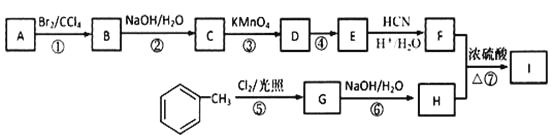
已知:①A 屬于脂肪烴,核磁共振氫譜顯示有 2 組峰,面積比為 3:1,其蒸氣密度是相同條件下 H2 的 28 倍;D 分子式為C4H8O3;E 分子式為 C4H6O2,能使溴水褪色。
②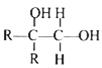
![]()
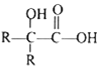 其中 R 為烴基。
其中 R 為烴基。
③![]()
![]()
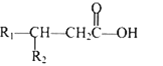 其中 R1 和 R2 均為烴基。
其中 R1 和 R2 均為烴基。
回答下列問題:
(1)A 的結構簡式為_______。
(2)D 中官能團的名稱是_______。
(3)反應②化學方程式為_______。
(4)E的同系物K 比E 多一個碳原子,K有多種鏈狀同分異構體,其中能發生銀鏡反應且能水解的有_______種。
(5)反應①~⑦屬于取代反應的是_______ (填序號)。
(6)反應⑦的化學方程式為_______。
(7)參照上述合成路線,以![]() 原料(無機試劑任選),經 4 步反應制備可降解塑料
原料(無機試劑任選),經 4 步反應制備可降解塑料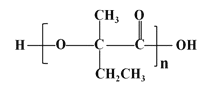 _______ (例如合成流程CH3CH2Br
_______ (例如合成流程CH3CH2Br![]() CH3CH2OH
CH3CH2OH![]() CH3COOCH2CH3)
CH3COOCH2CH3)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖所示為800 ℃時A、B、C三種氣體在密閉容器中反應時濃度的變化,只從圖上分析能得出的結論是( )
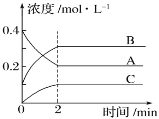
A.發生的反應可表示為2B(g)+C(g) ![]() 2A(g)
2A(g)
B.開始時,正、逆反應同時開始
C.前2 min A的分解速率為0.1mol·L-1·min-1
D.2 min時,A、B、C的濃度之比為2∶3∶1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某研究小組擬合成除草劑苯達松和染料中間體X。

已知信息:

(1)下列說法正確的是___。
A.化合物B到C的轉變涉及到取代反應 B.化合物C具有兩性
C.試劑D可以是甲醇 D.苯達松的分子式是C10H10N2O3S
(2)化合物F的結構簡式是________。
(3) 寫出E+G→H的化學方程式______。
(4)寫出分子式為C6H13NO2,同時符合下列條件的同分異構體的結構簡式,寫出2個即可_____。
①分子中有一個六元環,且成環原子中最多含2個非碳原子;
②1H﹣NMR譜和IR譜檢測表明分子中有4種化學環境不同的氫原子。有N﹣O鍵,沒有過氧鍵(﹣O﹣O﹣)。
(5)設計以CH3CH2OH和 為原料制備X(
為原料制備X( )的合成路線(無機試劑任選,合成中須用到上述①②兩條已知信息,用流程圖表示)。_____
)的合成路線(無機試劑任選,合成中須用到上述①②兩條已知信息,用流程圖表示)。_____
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在催化條件下發生反應:N2O(g)+CO(g) ![]() CO2(g)+N2(g)可使環境污染性氣體轉化為無害氣體。反應進程中的能量變化如圖所示。下列說法正確的是
CO2(g)+N2(g)可使環境污染性氣體轉化為無害氣體。反應進程中的能量變化如圖所示。下列說法正確的是

A. 加入催化劑使反應的△H變小
B. 該反應的熱化學方程式為:N2O(g)+CO(g) ![]() CO2(g)+N2(g) △H﹦ - 226 kJ/mol
CO2(g)+N2(g) △H﹦ - 226 kJ/mol
C. 反應物的總能量小于生成物的總能量
D. 該反應正反應的活化能大于逆反應的活化能
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com