
【題目】A、B、C、D均為中學化學中常見的單質或化合物,它們之間的關系如圖所示(部分產物已略去)。
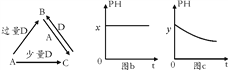
(1)若A為金屬單質,D是某強酸的稀溶液,則反應C+D→B的離子方程式為_______。
(2)若A為強堿,D為氣態氧化物。常溫時,將B的水溶液露置于空氣中,其pH隨時間 t變化可能如上圖的圖b或圖c所示(不考慮D的溶解和水的揮發)。
①若圖b符合事實,則D的化學式為 _________________________________________;
②若圖c符合事實,則其pH變化的原因是 _____________________________________(用離子方程式表示)
【答案】 3Fe2++4H++NO3-═3Fe3++NO↑+2H2O CO2 2HSO3-+O2=2H++2SO4 2-
【解析】本題考查物質的推斷,D是某強酸的稀溶液,A為金屬單質,A與少量的D反應,與足量D反應產物是不同,根據轉化關系,A為Fe,D為HNO3,C為Fe(NO3)2,因此C和D反應的離子方程式為3Fe2++4H++NO3-═3Fe3++NO↑+2H2O;(2)①A為強堿,D為氣態氧化物,即為酸性氧化物,D為SO2或CO2,圖bpH不變,因此D為CO2,因為+4價S具有還原性,溶液被空氣中的氧氣氧化;②D為SO2,B為NaHSO3,NaHSO3容易被空氣氧化成,因此離子反應方程式為2HSO3-+O2=2H++2SO42-。


科目:高中化學 來源: 題型:
【題目】下列實驗操作都要用玻璃棒:①過濾 ②蒸發 ③溶解 ④向容量瓶轉移液體,其中玻璃棒作用相同的是( )
A. ①和② B. ①和③ C. ①和④ D. ③和④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定溫度下,1 molX和n mol Y在容積為2L的密閉容器中發生如下反應:X(g)+Y(g)![]() 2Z(g)+M(s),5min后達到平衡,此時生成0.2 mol Z。下列說法正確的是
2Z(g)+M(s),5min后達到平衡,此時生成0.2 mol Z。下列說法正確的是
A.若將容器壓縮時,正逆反應速率均不變
B.5 min內平均反應速率v(X)=0.02 mol/(L·min)
C.向平衡后的體系中加入l molM(s),平衡向逆反應方向移動
D.當混合氣體的質量不再發生變化時,說明反應達到平衡狀態
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】W、X、Y、Z均為短周期主族元素,且原子序數依次增大。已知W元素的原子形成的離子是一個質子;X、Y在元素周期表中處于相鄰的位置,它們的單質在常溫下均為無色氣體;Z為同周期中原子半徑最大的元素。下列有關說法正確的是
A. 四種元素均為非金屬元素
B. W與X、Y形成的最簡單分子的沸點:X>Y
C. Y、Z形成的化合物中只含離子鍵
D. W、Y、Z形成的化合物的電子式為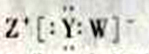
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】反應H2(g)+Cl2(g)═2HCl(g) 的發生過程能量變化如下所示:
![]()
下列說法錯誤的是
A.H﹣H鍵比Cl﹣Cl鍵穩定
B.△H=﹣184.5 kJmol﹣1
C.正反應活化能比逆反應活化能高
D.在相同條件下,1mol H2(g)和1mol Cl2(g)分別在點燃和光照條件下反應生成2mol HCl(g),重新恢復到原來的狀態時△H相同
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com