
【題目】A—E五種物質都含有同一種元素,它們之間的轉化關系如圖所示,其中A為淡黃色固體化合物,B為單質。

(1)固體A的名稱為____,單質B的常見用途有:_____(任寫一條)。
(2)寫出下列反應的化學方程式
①B→C__________
②A→D__________
(3)寫出將氯氣通入C溶液中的化學方程式_____,其溶液有漂白作用,漂白原理是______。(寫反應方程式)
【答案】過氧化鈉; 制作高壓鈉燈,Na-K液態合金做原子反應堆的導熱劑,制備鈉的化合物,制備某些金屬等(任寫一條); 2Na + 2H2O = 2NaOH + H2↑; 2Na2O2 + 2CO2 = 2Na2CO3 + O2; Cl2 + 2NaOH = NaCl + NaClO + H2O; NaClO + H2O + CO2 = NaHCO3 + HClO。
【解析】
A~E五種物質都含有同一種元素,A為淡黃色固體化合物,可由單質B轉化得到,且A又能與二氧化碳反應生成D,則A為Na2O2,D為Na2CO3,而B能與氯氣反應生成E,則B為Na、E為NaCl,A、B均可以轉化生成C,C可以轉化得到D、E,可推知C為NaOH,據此進行解答。
(1)固體A的名稱為過氧化鈉,鈉的常見用途有:制作高壓鈉燈,Na-K液態合金做原子反應堆的導熱劑,制備鈉的化合物,制備某些金屬等;
故答案為:過氧化鈉;制作高壓鈉燈,Na-K液態合金做原子反應堆的導熱劑,制備鈉的化合物,制備某些金屬等(任寫一條);
(2)①B→C的化學方程式:2Na + 2H2O = 2NaOH + H2↑,②A→D的化學方程式:2Na2O2 + 2CO2 = 2Na2CO3 + O2;
故答案為:2Na + 2H2O = 2NaOH + H2↑;2Na2O2 + 2CO2 = 2Na2CO3 + O2;
(3)將氯氣通入C溶液中的化學方程式:Cl2 + 2NaOH = NaCl + NaClO + H2O,其溶液有漂白作用,漂白原理是:NaClO + H2O + CO2 = NaHCO3 + HClO;
故答案為:Cl2 + 2NaOH = NaCl + NaClO + H2O;NaClO + H2O + CO2 = NaHCO3 + HClO。


科目:高中化學 來源: 題型:
【題目】NiSO4、NiCl2是制取高純鎳和電鍍行業的重要原料,回答下列問題:
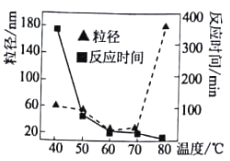
(1)堿性條件下利用肼(N2H2)還原NiCl2溶液可生成高純Ni納米粒子和某氣體單質,寫出反應的離子方程式_________________________________。溫度對反應時間和Ni粒徑的影響如圖所示,溫度為___________(選填字母)℃時,很難形成納米級別的Ni(已知納米級別的Ni與膠體分散質的大小一致)。
A.43 B.50 C.64 D.79
(2)利用某含鎳廢料(主要成分為Ni,還含有鋁、鐵的氧化物)可制備硫酸鎳晶體(NiSO4·7H2O),其流程如圖所示:

已知:Ksp[Ni(OH)2]=2.0×10-15 K sp[Fe(OH)2]=8.0×10-16
K sp[Fe(OH)3]=4.0×10-38
①寫出“氧化”步驟中發生反應的化學方程式_________________________________,步驟需要控制溫度40℃左右,其目的是_________________________________。
②已知“酸浸”所得濾液中c(Ni2+)=1mol/L,c(Fe2+)=0.1mol/L,試通過計算證明“氧化”步驟的必要性__________________________________________________________________(離子濃度小于1×10-5mol/L時可認為沉淀完全,要有計算過程和合理的文字敘述)。
③“系列操作”包括__________、冷卻結晶、過濾、乙醇洗滌、干燥等操作,其中利用乙醇洗滌硫酸鎳晶體的優點是____________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關化學反應與能量的說法中錯誤的是( )
A. 化學反應必然伴隨著能量變化
B. 油脂在人體中氧化是放熱反應
C. 鎂與鹽酸反應是吸熱反應
D. 氫分子(H-H)變成2個H需吸收能量
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為了研究化學反應A+B===C+D的能量變化情況,某同學設計了如圖所示裝置。當向盛有A的試管中滴加試劑B時,看到U形管中甲處液面下降乙處液面上升。試回答下列問題:

(1)該反應為____________反應(填“放熱”或“吸熱”)。
(2)反應物化學鍵斷裂吸收的能量________(填“高”或“低”)于生成物化學鍵形成放出的能量。
(3)寫出一個符合題中條件的化學方程式:_______________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表是元素周期表的一部分,按要求完成各小題。
IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
2 | ⑥ | ⑦ | ||||||
3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
4 | ② | ④ | ⑨ |
(1)元素①的元素符號:_______________
(2)元素⑧的單質電子式_______________
(3)元素⑤的原子結構示意圖______________
(4)化學性質最不活潑的元素______(填元素符號,下同),非金屬性最強的元素是________。金屬性最強的單質_______。
(5)①③⑤三種元素的最高價氧化物水化物中,堿性最強的 _____(填化學式,下同)。①③⑤三種元素的原子半徑由大到小的順序為_____________。
(6)某元素的最高價氧物的水化物既能與酸反應生成鹽和水又能與堿反應生成鹽與水,該元素的最高價氧化物和鹽酸反應的化學方程式為 _____,與氫氧化鈉溶液反應的化學方程式_____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表是元素周期表短周期的一部分:

(1)①表示的元素名稱是____,②對應簡單離子結構示意圖為_____,簡單離子半徑比較②______④。(填“大于”、“小于”、“等于”)
(2)③位于元素周期表第__________周期第__________族。
(3)④的單質與NaOH溶液反應的離子方程式_______________。
(4)用電子式表示③和⑤形成化合物的過程_______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在給定的條件下,下列選項所示的物質間轉化均能實現的是
A. SiO2![]() SiCl4
SiCl4![]() Si
Si
B. FeS2![]() SO2
SO2![]() H2SO4
H2SO4
C. N2![]() NH3
NH3![]() NH4Cl(aq)
NH4Cl(aq)
D. MgCO3![]() MgCl2(aq)
MgCl2(aq) ![]() Mg
Mg
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氯乙烷跟化合物之間的轉化如圖所示:

(1)寫出各反應的化學方程式
①__________
②_________
③__________
④__________
(2)根據上述方程式回答下列問題:
①上述化學反應的反應類型有__________,__________,__________。
②用AgNO3溶液通過__________反應可證明鹵代烴中含鹵元素(填序號)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖為以Pt為電極的氫氧燃料電池的工作原理示意圖,稀H2SO4溶液為電解質溶液。下列有關說法不正確的是

A. a極為負極,電子由a極經外電路流向b極
B. a極的電極反應式:H2-2e-===2H+
C. 電池工作一段時間后,裝置中c(H2SO4)增大
D. 若將H2改為CH4,消耗等物質的量的CH4時,O2的用量增多
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com