
【題目】化學·選修3:物質結構與性質
氟及其化合物用途非常廣泛,自然界中氟多以化合態形式存在,主要有螢石(CaF2)、冰晶石( Na3AlF6)等。回答下列問題:
(1)基態氟原子中有_________________種能量不同的電子。
(2)NF3是微電子工業中優良的等離子刻蝕氣體。NF3與NH3的空間構型相同,但是NH3( -33° C)的沸點比NF3( -129° C)的高,原因為_____________。
(3)氟硼酸( HBF4,屬于強酸)常用于替代濃硫酸作鉛蓄電池的電解質溶液,可由HF和BF3合成,從化學鍵形成角度分析HF與BF3能化合的原因:________。
(4)液態[H2F]+中存在[H2F]+和[HF2]- ,[HF2]-的結構可表示為[F-H…F]- ,[H2F]+的VSEPR模型名稱為________形。NaHF2可用于制無水氟化氫和供雕刻玻璃、木材防腐等。常溫常壓下為白色固體,易溶于水,160°C分解。NaHF2中所含作用力的類型有______. (填字母)。
a 離子鍵 b 共價鍵 c 配位鍵 d 氫鍵
(5)CaF2是難溶化合物,其品胞結構如圖所示:
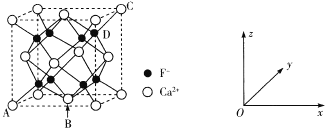
①若原子坐標參數A處為(0,0,0),B處為(![]() ,C處為(1,1,1),則D處為_____.
,C處為(1,1,1),則D處為_____.
②每個Ca2+周圍距離最近的Ca2+共有_____個。
③已知:CaF2晶體密度為cg·cm-3 ,則晶胞中Ca2+與最近的F-之間的距離為____nm(設NA表示阿伏加德羅常數的值,用含c、NA的式子表示)。
【答案】3 二者均為分子晶體,但是NH3分子間能形成氫鍵 HF分子中F原子有孤電子對,而BF3分子中B原子有空軌道,二者可以形成配位鍵 四面體 abd ![]() 12
12 ![]()
【解析】
(1)基態F 原子的電子排布式為1s22s22p5,所以有3種不同能量的電子,故答案為:3;
(2)NH3與NF3均為分子晶體,NH3能形成分子間氫鍵,所以熔沸點更高,故答案為:二者均為分子晶體,但是NH3分子間能形成氫鍵;
(3)BF3分子中B原子上有空軌道,而HF分子中的F原子上有孤電子,對,當BF3與HF靠近時,HF分子中F原子的孤電子對填充BF3分子中B原子的空軌道,二者形成配位鍵,從而結合形成HBF4,故答案為:HF分子中F原子有孤電子對,而BF3分子中B原子有空軌道,二者可以形成配位鍵;
(4)[H2F]+中F的價層電子對數為![]() 4,故為sp3雜化,VSEPR模型為四面體。NaHF2 中Na+與[HF2]-之間為離子鍵,[F—H
4,故為sp3雜化,VSEPR模型為四面體。NaHF2 中Na+與[HF2]-之間為離子鍵,[F—H![]() F]-中含共價鍵和氫鍵,故答案為:四面體;abd;
F]-中含共價鍵和氫鍵,故答案為:四面體;abd;
(5)①D點在底面和側面的投影均為面對角線的![]() 處,故坐標為
處,故坐標為![]() ;
;
②晶胞中Ca2+構成面心立方最密堆積方式,每個Ca2+周圍最近的Ca2+有12個,故答案為:12;
③根據均攤法可知,1個氟化鈣晶胞中有4個F-,![]() =4Ca2+;設晶胞中棱長為acm;氟化鈣的式量為78;,根據密度計算公式
=4Ca2+;設晶胞中棱長為acm;氟化鈣的式量為78;,根據密度計算公式![]() ,所以a=
,所以a=![]() ,從晶胞結構可以看出,與Ca2+最近的F-距離為
,從晶胞結構可以看出,與Ca2+最近的F-距離為![]() a,即
a,即![]() ,故答案為:
,故答案為:![]() 。
。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】符合分子式“C6H6”的多種可能結構如圖所示,下列說法正確的是

A. 1~5對應的結構中能使溴的四氯化碳溶液褪色的有4個
B. 1~5對應的結構中一氯取代物只有1種的有3個
C. 1~5對應的結構中所有原子均可能處于同一平面的有1個
D. 1~5對應的結構均能與氫氣在一定條件下發生加成反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Cu2O是一種半導體材料,基于綠色化學理念設計的一種制取Cu2O的電解池示意圖如下,電池總反應為2Cu+H2O![]() Cu2O+H2↑。下列說法正確的是
Cu2O+H2↑。下列說法正確的是

A.石墨電極上產生氫氣
B.銅電極發生還原反應
C.銅電極接直流電源的負極
D.當有0.1mol電子轉移時,有0.1mol Cu2O生成
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定條件下,兩體積均為1 L的容器中發生反應:CO(g)+2H2(g) ![]() CH3OH(g) ΔH。容器中起始各物質的物質的量如下表所示,兩容器中c(H2)隨時間t的變化如下圖所示。
CH3OH(g) ΔH。容器中起始各物質的物質的量如下表所示,兩容器中c(H2)隨時間t的變化如下圖所示。
容器 | 溫度 | CO | H2 | CH3OH |
Ⅰ | T1℃ | a mol | 2 mol | 0 mol |
Ⅱ | T1℃ | 0.5 mol | 1 mol | 0 mol |

下列說法正確的是
A.0~5 min時,容器Ⅰ中v(CO)=0.1 mol·L-1·min-1
B.a>1
C.若容器Ⅱ溫度改變為T2(T2>T1)時,平衡常數K=1,則ΔH<0
D.T1℃時,若向容器Ⅰ中充入CO、H2、CH3OH各1 mol,反應將向逆反應方向進行
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下面是A~G七種元素的電子排布:
元素 電子排布 電子層 | A | B | C | D | E | F | G |
K | 1 | 2 | 2 | 2 | 2 | 2 | 2 |
L | 4 | 5 | 6 | 8 | 8 | 8 | |
M | 1 | 3 | 7 |
試根據由上述元素構成的物質的化學式回答下列問題。
(1)寫出一種常見的由非極性鍵形成的雙原子分子:____________________。
(2)寫出一種由極性鍵形成的雙原子分子:____________________。
(3)寫出一種由極性鍵形成的三原子分子:____________________。
(4)寫出一種由三種元素形成的既含離子鍵又含共價鍵的化合物:__________,其電子式為____________________。
(5)寫出一種既含離子鍵又含非極性鍵的化合物:__________,其電子式為__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA為阿伏加德羅常數的值。下列說法正確的是
A.4.0g由CO2和SO2組成的混合物中含有的質子數為2NA
B.1L0.5mol/LpH=7的CH3COONH4溶液中NH4+數目為0.5NA
C.常溫下,0.1mol環氧乙烷(![]() )中含有的共價鍵數目為0.3NA
)中含有的共價鍵數目為0.3NA
D.22.4LCO2與足量Na2O2充分反應,轉移的電子數目為NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】倍他樂克是一種治療高血壓的藥物,其中間體F合成路線如下:

回答下列問題:
(1)A的分子式為____ 。 D中官能團的名稱是____ 。
(2)B與足量NaOH溶液反應的化學方程式為____。
(3)D→E的反應類型為_____。
(4)反應⑤加入試劑X反應后只生成中間體F,則X結構簡式為 ___。
(5)滿足下列條件的C的同分異構體有_____種。
①能發生銀鏡反應;
②與NaOH溶液反應時,1molC最多消耗3molNaOH;
③苯環上只有4個取代基,且直接與苯環相連的烴基處于間位。其中核磁共振氫譜有4種不同化學環境的氫,且峰面積比為1︰6︰2︰1的可能是____(寫結構簡式)。
(6)根據已有知識及題目相關信息,完成以 和CH3OH、CH3ONa為原料制備
和CH3OH、CH3ONa為原料制備 的合成路線流程圖(無機試劑任選)____。
的合成路線流程圖(無機試劑任選)____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】交聯聚合物P的結構片段如圖所示。下列說法不正確的是(圖中![]() 表示鏈延長)
表示鏈延長)

A. 聚合物P中有酯基,能水解
B. 聚合物P的合成反應為縮聚反應
C. 聚合物P的原料之一丙三醇可由油脂水解獲得
D. 鄰苯二甲酸和乙二醇在聚合過程中也可形成類似聚合物P的交聯結構
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表是元素周期表的一部分,表中所列的字母分別代表一種化學元素。
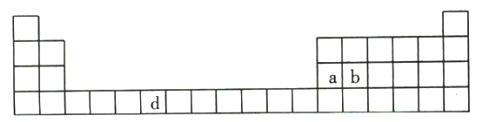
(1)請寫出元素d的基態原子的電子排布式: _______________________________________。
(2)b的氧化物中b原子與氧原子之間的共價鍵類型是__________________________其中b原子的雜化方式是____________________________________________。
(3)a的單質晶體中原子的堆積方式如圖甲所示,其晶胞如圖乙所示,原子之間相互位置關系的平面圖如圖丙所示。
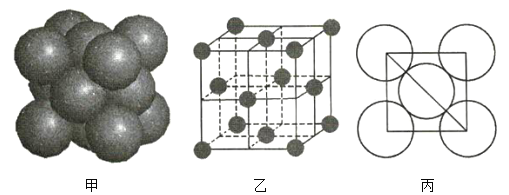
若已知a元素原子的半徑為d,NA代表阿伏加德羅常數,a元素原子的摩爾質量為M,則1個晶胞中a原子的數目為____________________________,該晶體的密度為____________________________________(用字母表示)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com