
ĪŠŅ}─┐Ī┐Ž┬łD╦∙╩Š╩Ūį¬╦žų▄Ų┌▒ĒĄ─▓┐Ęų▌å└¬łDŻ¼Ė∙ō■į¬╦žó┘Ī½óŌį┌ų▄Ų┌▒ĒųąĄ─╬╗ų├░┤Ņ}─┐ę¬Ū¾╗ž┤Ż║
ó┘ | |||||||||||||||||
ó┌ | ó█ | ó▄ | |||||||||||||||
ó▌ | ó▐ | ó▀ | óÓ | ||||||||||||||
óß | |||||||||||||||||
óŌ |
(1)īæ│÷ė╔į¬╦žó┘ó█ó▄░┤įŁūėéĆöĄ▒╚4:2:3ĮM│╔Ą─╬’┘|Ą─╗»īW╩Į_______Ż¼Ųõ║¼ėąĄ─╗»īWµIŅÉą═ėą________ĪŻ
(2)į¬╦žó▌~óÓą╬│╔Ą─║åå╬ļxūėųąŻ¼ļxūė░ļÅĮė╔┤¾ĄĮąĪĄ─Ēśą“×ķ____________(ė├ļxūėĘ¹╠¢▒Ē╩Š)ĪŻ
(3)į¬╦žó█ó▀óߥ─║åå╬ÜŌæBÜõ╗»╬’Ęą³cė╔Ė▀ĄĮĄ═Ą─Ēśą“┼┼┴ą╩Ū______(ė├╗»īW╩Į▒Ē╩Š)ĪŻ
(4)īæ│÷į¬╦žóŌĄ─įŁūėĮYśŗ╩ŠęŌłD______ĪŻ
(5)į¬╦žó┌║═ó▄ĮM│╔Ą─ę╗ĘN╗»║Ž╬’╩Ūę²Ų£ž╩ęą¦æ¬Ą─ų„ę¬ÜŌ¾wŻ¼ŲõļŖūė╩Į×ķ_________Ż¼īó╔┘┴┐įō╗»║Ž╬’═©╚ļė╔į¬╦žó▄ó▌ó▐ĮM│╔Ą─ę╗ĘN¹}╚▄ę║ųąŻ¼īæ│÷ŽÓæ¬Ą─╗»īWĘĮ│╠╩Į_____ĪŻ
(6)į¬╦žóÓĄ─ę╗ĘNč§╗»╬’═©╚ļ┬╚╗»õ^╚▄ę║¤o│┴ĄĒŻ¼═©╚ļŽ§╦ßõ^╚▄ę║ģsĢ■«a╔·░ū╔½│┴ĄĒŻ¼īæ│÷╔┘┴┐įōč§╗»╬’═©╚ļŽ§╦ßõ^╚▄ę║Ą─ļxūėĘĮ│╠╩Į___ĪŻ
ĪŠ┤░ĖĪ┐NH4NO3 ļxūėµIĪóŻ©śOąįŻ®╣▓ārµI P3- >S2- > Na+ > Al3+ NH3 >AsH3 > PH3 
![]() CO2+2NaAlO2+3H2O==2Al(OH)3Ī²+Na2CO3 3SO2+3Ba2++2
CO2+2NaAlO2+3H2O==2Al(OH)3Ī²+Na2CO3 3SO2+3Ba2++2![]() +2H2O==3BaSO4Ī²+2NOĪ³+4H+
+2H2O==3BaSO4Ī²+2NOĪ³+4H+
ĪŠĮŌ╬÷Ī┐
Ė∙ō■į¬╦žį┌ų▄Ų┌▒ĒĄ─ĮYśŗ┼ąöÓį¬╦žĘNŅÉŻ¼Ė∙ō■į¬╦žų▄Ų┌┬╔╝░╬’┘|ąį┘|Ęų╬÷ĮŌ┤ĪŻ
ė╔į¬╦žį┌ų▄Ų┌▒Ēųą╬╗ų├Ż¼┐╔ų¬ó┘×ķHŻ¼ó┌×ķCŻ¼ó█×ķNŻ¼ó▄×ķOŻ¼ó▌×ķNaŻ¼ó▐×ķAlŻ¼ó▀×ķPŻ¼óÓ×ķSŻ¼óß×ķAsŻ¼óŌ×ķRbŻ¼
(1) HĪóNĪóO░┤░┤įŁūėéĆöĄ▒╚4:2:3ĮM│╔Ą─╬’┘|Ą─╗»īW╩Į×ķNH4NO3Ż¼õ@Ė∙ļxūė┼cŽ§╦ßĖ∙ļxūėķg┤µį┌ļxūėµIŻ¼Ž§╦ßĖ∙ļxūėųąN┼cOęį╣▓ārµIĮY║ŽŻ¼ät╗»īWµIŅÉą═ėąļxūėµIĪóŻ©śOąįŻ®╣▓ārµIŻ¼╣╩┤░Ė×ķŻ║NH4NO3Ż╗ļxūėµIĪóŻ©śOąįŻ®╣▓ārµIŻ╗
(2) į¬╦žó▌~óÓą╬│╔Ą─║åå╬ļxūėųąŻ¼ļŖūėīėöĄįĮČÓŻ¼░ļÅĮįĮ┤¾Ż¼║╦═ŌļŖūėöĄŽÓ═¼ĢrŻ¼║╦ļŖ║╔įĮ┤¾Ż¼░ļÅĮįĮąĪŻ¼ätļxūė░ļÅĮė╔┤¾ĄĮąĪĄ─Ēśą“×ķP3->S2-> Na+> Al3+Ż¼╣╩┤░Ė×ķŻ║P3->S2-> Na+> Al3+Ż╗
(3) ĮM│╔║═ĮYśŗŽÓ╦ŲĄ─╬’┘|Ż¼ŽÓī”Ęųūė┘|┴┐įĮ┤¾Ż¼Ęųūėķgū„ė├┴”įĮ┤¾Ż¼Ęą³cįĮĖ▀Ż¼ätĘą³cAsH3> PH3Ż¼NH3Ęųūėķg┤µį┌ÜõµIŻ¼ätĘą³cūŅĖ▀Ż¼╣╩Ęą³cė╔Ė▀ĄĮĄ═Ą─Ēśą“┼┼┴ą╩ŪNH3>AsH3> PH3Ż¼╣╩┤░Ė×ķŻ║NH3>AsH3> PH3Ż╗
(4) Rbį┌į¬╦žų▄Ų┌▒ĒųąĄ┌╬Õų▄Ų┌IAūÕŻ¼╣▓ėą5éĆļŖūėīėŻ¼ūŅ═ŌīėļŖūėöĄ×ķ1Ż¼ätįŁūėĮYśŗ╩ŠęŌłD Ż¼╣╩┤░Ė×ķŻ║
Ż¼╣╩┤░Ė×ķŻ║ Ż╗
Ż╗
(5) į¬╦žC║═OĮM│╔Ą─ę╗ĘN╗»║Ž╬’×ķCO2Ż¼╩Ūę²Ų£ž╩ęą¦æ¬Ą─ų„ę¬ÜŌ¾wŻ¼ŲõļŖūė╩Į×ķ![]() Ż¼īó╔┘┴┐Č■č§╗»╠╝═©╚ļŲ½õX╦ßŌc╚▄ę║ųąĘ┤æ¬╔·│╔Üõč§╗»õX│┴ĄĒ║═╠╝╦ßŌcŻ¼╗»īWĘĮ│╠╩Į×ķŻ║CO2+2NaAlO2+3H2O==2Al(OH)3Ī²+Na2CO3Ż¼╣╩┤░Ė×ķŻ║
Ż¼īó╔┘┴┐Č■č§╗»╠╝═©╚ļŲ½õX╦ßŌc╚▄ę║ųąĘ┤æ¬╔·│╔Üõč§╗»õX│┴ĄĒ║═╠╝╦ßŌcŻ¼╗»īWĘĮ│╠╩Į×ķŻ║CO2+2NaAlO2+3H2O==2Al(OH)3Ī²+Na2CO3Ż¼╣╩┤░Ė×ķŻ║![]() Ż╗CO2+2NaAlO2+3H2O==2Al(OH)3Ī²+Na2CO3Ż╗
Ż╗CO2+2NaAlO2+3H2O==2Al(OH)3Ī²+Na2CO3Ż╗
(6) į¬╦žSĄ─ę╗ĘNč§╗»╬’═©╚ļ┬╚╗»õ^╚▄ę║¤o│┴ĄĒŻ¼═©╚ļŽ§╦ßõ^╚▄ę║ģsĢ■«a╔·░ū╔½│┴ĄĒŻ¼ätįōč§╗»╬’×ķSO2Ż¼Ę┤æ¬ļxūėĘĮ│╠╩Į×ķŻ║3SO2+3Ba2++2![]() +2H2O=3BaSO4Ī²+2NOĪ³+4H+Ż¼╣╩┤░Ė×ķŻ║3SO2+3Ba2++2
+2H2O=3BaSO4Ī²+2NOĪ³+4H+Ż¼╣╩┤░Ė×ķŻ║3SO2+3Ba2++2![]() +2H2O=3BaSO4Ī²+2NOĪ³+4H+ĪŻ
+2H2O=3BaSO4Ī²+2NOĪ³+4H+ĪŻ


 ķåūx┐ņ▄接┴ą┤░Ė
ķåūx┐ņ▄接┴ą┤░Ė
| ─Ļ╝ē | Ė▀ųąšn│╠ | ─Ļ╝ē | │§ųąšn│╠ |
| Ė▀ę╗ | Ė▀ę╗├Ō┘Mšn│╠═Ų╦]ŻĪ | │§ę╗ | │§ę╗├Ō┘Mšn│╠═Ų╦]ŻĪ |
| Ė▀Č■ | Ė▀Č■├Ō┘Mšn│╠═Ų╦]ŻĪ | │§Č■ | │§Č■├Ō┘Mšn│╠═Ų╦]ŻĪ |
| Ė▀╚² | Ė▀╚²├Ō┘Mšn│╠═Ų╦]ŻĪ | │§╚² | │§╚²├Ō┘Mšn│╠═Ų╦]ŻĪ |
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐ė├ČĶąįļŖśOļŖĮŌūŃ┴┐Ž┬┴ą╚▄ę║ę╗Č╬Ģrķg║¾Ż¼į┘╝ė╚ļę╗Č©┴┐└©╠¢ā╚Ą─╝āā¶╬’Ż¼─▄╩╣╚▄ę║╗ųÅ═ĄĮįŁüĒĄ─│╔Ęų║═ØŌČ╚Ą─╩Ū
A. AgNO3[AgNO3] B. NaOH[NaOH] C. KCl[H2O] D. CuSO4[CuO]
ĪŠ┤░ĖĪ┐D
ĪŠĮŌ╬÷Ī┐╩»─½ļŖśO×ķČĶąįļŖśOŻ¼╚▄ę║ųąĻ¢ļxūėį┌ĻÄśOĘ┼ļŖŻ¼ĻÄļxūėį┌Ļ¢śOĘ┼ļŖĪŻAĪóļŖĮŌAgNO3╚▄ę║Ż¼Ag+į┌ĻÄśOĘ┼ļŖ╔·│╔AgŻ¼OH-į┌Ļ¢śOĘ┼ļŖ╔·│╔O2Ż¼Ūęn(Ag)Ī├n(O2)=2Ī├1,ätæ¬╝ė╚ļAg2O╗ųÅ═ØŌČ╚Ż¼╣╩AÕeš`Ż╗BĪóļŖĮŌNaOH╚▄ę║Ż¼H+į┌ĻÄśOĘ┼ļŖ╔·│╔H2Ż¼OH-į┌Ļ¢śOĘ┼ļŖ╔·│╔O2Ż¼Ūęn(H2)Ī├n(O2)=2Ī├1,ätæ¬╝ė╚ļę╗Č©┴┐Ą─H2O╗ųÅ═įŁśėŻ¼╣╩BÕeš`Ż╗CĪóļŖĮŌKCl╚▄ę║Ż¼H+į┌ĻÄśOĘ┼ļŖ╔·│╔H2Ż¼Cl-į┌Ļ¢śOĘ┼ļŖ╔·│╔Cl2Ż¼Ūęn(H2)Ī├n(Cl2)=1Ī├1,ätæ¬╝ė╚ļę╗Č©┴┐HCl╗ųÅ═įŁśėŻ¼╣╩CÕeš`Ż╗DĪóļŖĮŌCuSO4╚▄ę║Ż¼Cu2+į┌ĻÄśOĘ┼ļŖ╔·│╔CuŻ¼OH-į┌Ļ¢śOĘ┼ļŖ╔·│╔O2Ż¼Ūęn(Cu)Ī├n(O2)=2Ī├1,ätæ¬╝ė╚ļę╗Č©┴┐CuO╗ųÅ═įŁśėŻ¼╣╩Dš²┤_ĪŻ╣╩▀xDĪŻ
³cŠ”Ż║Ęų╬÷ļŖĮŌĘ┤æ¬Ą─įŁ└ĒŻ¼į┌ā╔śO╬÷│÷╩▓├┤╬’┘|Ż©╣╠¾w╗“ÜŌ¾wŻ®Ż¼ŽÓ«öė┌╩▓├┤╬’┘|├ōļxĘ┤款wŽĄŻ¼Ė∙ō■į¬╦ž╩ž║Ń║═įŁūė▒╚└²Ż¼╝ė╚ļī”æ¬Ą─╬’┘|Ż¼╝┤┐╔╩╣╚▄ę║═Ļ╚½Å═įŁĪŻ
ĪŠŅ}ą═Ī┐å╬▀xŅ}
ĪŠĮY╩°Ī┐
28
ĪŠŅ}─┐Ī┐╣żśI╔Žė├ļŖĮŌĘ©╠Ä└Ē║¼µć╦ßąįÅU╦«▓óĄ├ĄĮå╬┘|NiĄ─įŁ└Ē╚ńłD╦∙╩ŠĪŻŽ┬┴ąšfĘ©▓╗š²┤_Ą─╩Ū
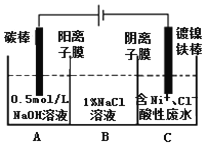
ęčų¬Ż║ó┘Ni2Ż½į┌╚§╦ßąį╚▄ę║ųą░l╔·╦«ĮŌ
ó┌č§╗»ąįŻ║Ni2Ż½(Ė▀ØŌČ╚)>HŻ½>Ni2Ż½(Ą═ØŌČ╚)
A. ╠╝░¶╔Ž░l╔·Ą─ļŖśOĘ┤æ¬Ż║4OHŻŁŻŁ4eŻŁ=O2Ī³Ż½2H2O
B. ļŖĮŌ▀^│╠ųąŻ¼BųąNaCl╚▄ę║Ą─╬’┘|Ą─┴┐ØŌČ╚īó▓╗öÓ£p╔┘
C. ×ķ┴╦╠ßĖ▀NiĄ─«a┬╩Ż¼ļŖĮŌ▀^│╠ųąąĶę¬┐žųŲÅU╦«pH
D. ╚¶īółDųąĻ¢ļxūė─ż╚źĄ¶Ż¼īóAĪóBā╔╩ę║Ž▓óŻ¼ätļŖĮŌĘ┤æ¬┐éĘĮ│╠╩Į░l╔·Ė─ūā
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐Ž┬┴ąļxūėĘĮ│╠╩Įš²┤_Ą─╩Ū
A.ė├ØŌ¹}╦ß╦ß╗»Ą─KMnO4╚▄ę║č§╗»H2C2O4Ż║6H+Ż½5H2C2O4Ż½2MnO4-ŻĮ10CO2Ī³Ż½2Mn2+Ż½8H2O
B.Ž“Ca(HCO3)2╚▄ę║ųąĄ╬╝ė╚ļ╔┘┴┐NaOH╚▄ę║Ż║Ca2+Ż½2HCO3ŻŁŻ½2OHŻŁŻĮCaCO3Ī²Ż½CO32ŻŁŻ½2H2O
C.Ž“Fe(NO3)3╚▄ę║ųą╝ė╚ļ▀^┴┐Ą─HI╚▄ę║Ż║2NO3ŻŁŻ½8H+Ż½6IŻŁŻĮ3I2Ż½2NOĪ³Ż½4H2O
D.ė├╩»─½ļŖśOļŖĮŌMgCl2╚▄ę║Ż║Mg2+Ż½2ClŻŁŻ½2H2O![]() Mg(OH)2Ī²Ż½H2Ī³Ż½Cl2Ī³
Mg(OH)2Ī²Ż½H2Ī³Ż½Cl2Ī³
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐į┌╚▌Ęe▓╗ūāĄ─├▄ķ]╚▌Ų„ųąŻ¼į┌ę╗Č©Śl╝■Ž┬░l╔·Ę┤æ¬Ż║2AB(g)+C(s)Ż¼Ūę▀_ĄĮŲĮ║ŌŻ¼«ö╔²Ė▀£žČ╚ĢrŻ¼╚▌Ų„ā╚ÜŌ¾wĄ─├▄Č╚ūā┤¾Ż¼ätŽ┬┴ą┼ąöÓš²┤_Ą─╩Ū( )
A.╚¶š²Ę┤æ¬×ķ╬³¤ßĘ┤æ¬Ż¼ätA×ķÜŌæB
B.╚¶š²Ę┤æ¬×ķĘ┼¤ßĘ┤æ¬Ż¼ätA×ķĘŪÜŌæB
C.╚¶į┌ŲĮ║Ō¾wŽĄųą╝ė╚ļ╔┘┴┐CŻ¼ätįōŲĮ║Ō─µŽ“ęŲäė
D.╚¶Ė─ūā£žČ╚Ż¼ÜŌ¾wĄ─ŲĮŠ∙─”Ā¢┘|┴┐▓╗ūāŻ¼ätAę╗Č©×ķĘŪÜŌæB
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐╝ū┤╝╝╚╩Ūųžę¬Ą─╗»╣żįŁ┴ŽŻ¼ėų┐╔ū„×ķ╚╝┴ŽĪŻ└¹ė├║Ž│╔ÜŌ(ų„ę¬│╔Ęų×ķCOĪóCO2║═H2)į┌┤▀╗»ä®Ą─ū„ė├Ž┬║Ž│╔╝ū┤╝Ż¼░l╔·Ą─ų„ę¬Ę┤æ¬╚ńŽ┬Ż║
ó┘CO(g)+2H2(g)CH3OH(g)Ī„H1
ó┌CO2(g)+3H2(g)CH3OH(g)+H2O(g)Ī„H2
ó█CO2(g)+H2(g)CO(g)+H2O(g)Ī„H3
╗ž┤Ž┬┴ąå¢Ņ}Ż║
(1)ęčų¬Ī„H1=®ü99kJĪżmol®ü1Ż¼ęčų¬Ī„H2=®ü58kJĪżmol®ü1Ż¼ätĪ„H3=______kJĪżmol®ü1ĪŻ
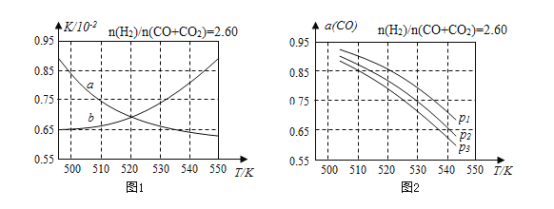
(2)Ę┤æ¬ó┘Ą─╗»īWŲĮ║Ō│ŻöĄKĄ─▒Ē▀_╩Į×ķ______Ż╗łD1ųą─▄š²┤_Ę┤ė│ŲĮ║Ō│ŻöĄKļS£žČ╚ūā╗»ĻPŽĄĄ─Ū·ŠĆ×ķ________(╠ŅŪ·ŠĆś╦ėøūų─Ė)ĪŻ
(3)║Ž│╔ÜŌĄ─ĮM│╔n(H2)/n(CO+CO2)=2.60Ģr¾wŽĄųąĄ─COŲĮ║Ō▐D╗»┬╩(a)┼c£žČ╚║═ē║ÅŖĄ─ĻPŽĄ╚ńłD2╦∙╩ŠĪŻa(CO)ųĄļS£žČ╚╔²Ė▀Č°________(╠ŅĪ░į÷┤¾Ī▒╗“Ī░£pąĪĪ▒)łD2ųąĄ─ē║ÅŖė╔┤¾ĄĮąĪ×ķ________ĪŻ
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐Ž┬┴ąėąĻPĮī┘Ą─╣żśIųŲĘ©ųąŻ¼š²┤_Ą─╩Ū
A. ęį║Ż╦«×ķįŁ┴ŽųŲĄ├Š½¹}Ż¼į┘ļŖĮŌŠ½¹}Ą─╦«╚▄ę║ųŲ╚ĪŌc
B. ė├║Ż╦«Īó╩»╗ę╚ķĄ╚×ķįŁ┴ŽŻ¼Įøę╗ŽĄ┴ą▀^│╠ųŲĄ├č§╗»µVŻ¼ė├H2▀ĆįŁč§╗»µVųŲĄ├µV
C. ęįĶFĄV╩»ĪóĮ╣╠┐Īó┐šÜŌĪó╩»╗ę╩»Ą╚×ķįŁ┴ŽŻ¼═©▀^Ę┤欫a╔·Ą─COį┌Ė▀£žŽ┬▀ĆįŁĶFĄV╩»ųŲĄ├ĶF
D. Å─õX═┴ĄVųą½@Ą├č§╗»õXį┘ųŲĄ├┬╚╗»õX╣╠¾wŻ¼ļŖĮŌ╚█╚┌Ą─┬╚╗»õXĄ├ĄĮõX
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐┴“§Ż┬╚(SO2Cl2)┐╔ė├ū„ėąÖC╗»īWĄ─┬╚╗»ä®Ż¼į┌╦Ä╬’║═╚Š┴ŽĄ─ųŲ╚Īųąę▓ėąųžę¬ū„ė├ĪŻ─│╗»īWīW┴ĢąĪĮMöMė├Ė╔į’Ą─Cl2║═SO2į┌╗Ņąį╠┐┤▀╗»Ž┬ųŲ╚Ī┴“§Ż┬╚ĪŻĘ┤æ¬Ą─╗»īWĘĮ│╠╩Į×ķŻ║SO2(g)+ Cl2(g) =SO2Cl2(l) ”żH =97.3 kJĪżmol1Ż¼īŹ“×čbų├╚ńłD╦∙╩Š(▓┐ĘųŖA│ųčbų├╬┤«ŗ│÷)ĪŻ
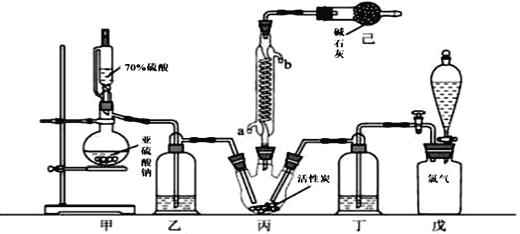
ęčų¬Ż║┴“§Ż┬╚═©│ŻŚl╝■Ž┬×ķ¤o╔½ę║¾wŻ¼╚█³c54.1ĪµŻ¼Ęą³c69.1ĪµĪŻį┌│▒ر┐šÜŌųąĪ░░l¤¤Ī▒Ż╗100ĪŃCęį╔Žķ_╩╝ĘųĮŌŻ¼╔·│╔Č■č§╗»┴“║═┬╚ÜŌŻ¼ķLŲ┌Ę┼ų├ę▓Ģ■░l╔·ĘųĮŌĪŻ
╗ž┤Ž┬┴ąå¢Ņ}Ż║
Ż©1Ż®čbų├╝ūųąū„×ķĘ┤æ¬╚▌Ų„Ą─āxŲ„Ą─├¹ĘQ×ķ________Ż¼čbų├╝║Ą─ū„ė├╩Ū________Ż╗╚ń║╬┐žųŲā╔ĘNĘ┤æ¬╬’¾wĘeŽÓĄ╚Ż║________ĪŻ
Ż©2Ż®čbų├╬ņ╔ŽĘĮĘųę║┬®ČĘųąūŅ║├▀xė├Ž┬┴ąįć䮯║Ż©_______Ż®(▀x╠Ņūų─Ė)ĪŻ
AŻ«š¶s╦« BŻ«’¢║═╩│¹}╦« CŻ«ØŌÜõč§╗»Ōc╚▄ę║ DŻ«6.0 molL1¹}╦ß
Ż©3Ż®╚¶╚▒╔┘čbų├ęę║═ČĪ(Š∙╩óĘ┼ØŌ┴“╦ß)Ż¼│▒ر┬╚ÜŌ║═Č■č§╗»┴“░l╔·Ę┤æ¬Ą─╗»īWĘĮ│╠╩Į╩Ū________________________________________ĪŻ
Ż©4Ż®┬╚╗Ū╦ß(ClSO3H)╝ė¤ßĘųĮŌŻ¼ę▓─▄ųŲĄ├┴“§Ż┬╚Ż║2ClSO3H ŻĮSO2Cl2 + H2SO4Ż¼Ęųļxā╔ĘN«a╬’Ą─ĘĮĘ©╩ŪŻ©_______Ż® (▀x╠Ņūų─Ė)ĪŻ
AŻ«ųžĮYŠ¦ BŻ«▀^×V CŻ«š¶s DŻ«▌═╚Ī
Ż©5Ż®ķLŲ┌ā”┤µĄ─┴“§Ż┬╚Ģ■░l³SŻ¼┐╔─▄Ą─įŁę“╩Ū________ (ė├╗»īWĘĮ│╠╩Į║═▒žę¬Ą─╬─ūų╝ėęįĮŌßī)ĪŻ
Ż©6Ż®╚¶Ę┤æ¬ųąŽ¹║─Ą─┬╚ÜŌ¾wĘe×ķ896 mL(ś╦£╩ĀŅørŽ┬)Ż¼ūŅ║¾Įø▀^Ęųļx╠ß╝āĄ├ĄĮ4.05 g╝āā¶Ą─┴“§Ż┬╚Ż¼ät┴“§Ż┬╚Ą─«a┬╩×ķ________ĪŻ×ķ╠ßĖ▀▒ŠīŹ“×ųą┴“§Ż┬╚Ą─«a┬╩Ż¼į┌īŹ“×▓┘ū„ųąąĶę¬ūóęŌĄ─╩┬ĒŚėą________________ ________________________________________ (īæā╔Śl╝┤┐╔)ĪŻ
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐╚ńłD╦∙╩ŠŻ¼╝ūĪóęę╩ŪļŖ╗»īWīŹ“×čbų├Ż¼šł╗ž┤Ž┬┴ąå¢Ņ}Ż║

Ż©1Ż®╚¶╝ūĪóęęā╔éƤ²▒ŁųąŠ∙╩óĘ┼’¢║═NaCl╚▄ę║ĪŻ
ó┘╝ūųą╩»─½░¶╔ŽĄ─ļŖśOĘ┤æ¬╩Į╩Ū____________ĪŻ
ó┌īóرØÖĄ─ĄĒĘ█KIįć╝łĘ┼į┌ęę¤²▒ŁĄ─╔ŽĘĮŻ¼░l¼Fįć╝łŽ╚ūā╦{║¾═╩╔½Ż¼▀@╩Ūę“×ķļŖĮŌ╔·│╔Ą──│ĘNÜŌ¾wAč§╗»┴╦IŻŁ╔·│╔┴╦I2ĪŻ╚¶AÜŌ¾w║═I2░┤╬’┘|Ą─┴┐ų«▒╚×ķ5Ī├1Ę┤æ¬Ż¼Ūę╔·│╔ā╔ĘN╦߯¼įōĘ┤æ¬Ą─╗»īWĘĮ│╠╩Į×ķ_________ĪŻ
ó█╚ń╣¹▓╗┐╝æ]ÜŌ¾w«a╬’┼c¤²▒Łųą╚▄ę║ų«ķgĄ─Ę┤æ¬Ż¼«öęęĘ┤æ¬ėą0.01 molļŖūė▐DęŲ║¾═Żų╣īŹ“ׯ¼¤²▒Łųą╚▄ę║Ą─¾wĘe×ķ100 mLŻ¼ät╚▄ę║╗ņä“║¾Ą─c(OH-)ŻĮ_____ĪŻ
Ż©2Ż®╚¶╝ūĪóęęā╔¤²▒ŁųąŠ∙╩óĘ┼CuSO4╚▄ę║ĪŻ
ó┘╝ūųąĶF░¶╔ŽĄ─ļŖśOĘ┤æ¬╩Į×ķ_______________ĪŻ
ó┌ęęųą┐éĘ┤æ¬Ą─ļxūėĘĮ│╠╩Į×ķ_________________ĪŻ
ó█╚ń╣¹Ų╩╝Ģręęųą╩óĘ┼100 mL pHŻĮ5Ą─CuSO4╚▄ę║(25Īµ)Ż¼ę╗Č╬Ģrķg║¾╚▄ę║Ą─c(H+)ŻĮ0.1mol/LŻ¼╚¶ę¬╩╣╚▄ę║╗ųÅ═ĄĮŲ╩╝ĢrĄ─ØŌČ╚(║÷┬į╚▄ę║¾wĘeĄ─ūā╗»)Ż¼┐╔Ž“╚▄ę║ųą╝ė╚ļ_____ (╠Ņīæ╬’┘|Ą─╗»īW╩Į)______gĪŻ
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐Ęė╠¬║¼Ų¼╩Ūę╗ĘNų╬»¤Ž¹╗»ŽĄĮy╝▓▓ĪĄ─╦Ä╬’Ż¼Ųõėąą¦│╔ĘųĄ─ĮYśŗ║å╩Į╚ńłD╦∙╩ŠŻ«Ž┬┴ąī”įōėąą¦│╔ĘųĄ─šfĘ©š²┤_Ą─╩ŪŻ©ĪĪĪĪŻ®
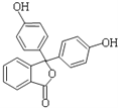
A. ║╦┤┼╣▓š±ÜõūVųąėą5éĆĘÕ
B. ūŅČÓėą14éĆ╠╝įŁūė╣▓ŲĮ├µ
C. ┐╔─▄░l╔·┐sŠ█Ę┤æ¬╔·│╔Ė▀Ęųūė╗»║Ž╬’
D. 1molįō╬’┘|ūŅČÓ─▄┼c║¼4molNaOHĄ─¤²ēA╚▄ę║Ę┤æ¬
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
ć°ļHīWąŻā×▀x - ŠÜ┴Ģāį┴ą▒Ē - įćŅ}┴ą▒Ē
║■▒▒╩Ī╗ź┬ōŠW▀`Ę©║═▓╗┴╝ą┼Žó┼eł¾ŲĮ┼_ | ŠW╔Žėą║”ą┼Žó┼eł¾īŻģ^ | ļŖą┼įp“_┼eł¾īŻģ^ | ╔µÜv╩Ę╠ō¤oų„┴xėą║”ą┼Žó┼eł¾īŻģ^ | ╔µŲ¾ŪųÖÓ┼eł¾īŻģ^
▀`Ę©║═▓╗┴╝ą┼Žó┼eł¾ļŖįÆŻ║027-86699610 ┼eł¾Ó]ŽõŻ║58377363@163.com