
下列有關能量的判斷或表示方法正確的是
| A.從C(石墨)=C(金剛石)ΔH=1.9 kJ·mol-1,可知金剛石比石墨更穩(wěn)定 |
| B.等質量的硫蒸氣和硫固體分別完全燃燒,后者放出熱量更多 |
| C.由H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1,則向含0.1 mol HCl的鹽酸中加入4.0 gNaOH固體,放出熱量等于5.73 kJ |
| D.2 gH2完全燃燒生成液態(tài)水放出285.8 kJ熱量,則氫氣燃燒的熱化學方程式為:2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1 |
D
解析試題分析:A.物質所含有的能量越低就越穩(wěn)定。由于C(石墨)=C(金剛石)吸收能量,所以金剛石不如石墨更穩(wěn)定。錯誤。B.等質量的硫蒸氣比硫固體所含有的能量高,所以硫蒸汽完全燃燒,放出熱量更多。錯誤。NaOH固體溶解于水會放出熱量,所以向含0.1 mol HCl的鹽酸中加入4.0 gNaOH固體,放出熱量大于5.73 kJ。錯誤。D.2 gH2即1mol的氫氣完全燃燒生成液態(tài)水放出285.8 kJ熱量,則2mol的氫氣燃燒放出熱量為571.6 kJ。所以其燃燒的熱化學方程式為:2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1。正確。
考點:考查物質燃燒釋放的能量與物質的狀態(tài)、及熱化學方程式的關系的知識。


科目:高中化學 來源: 題型:單選題
金剛石和石墨都是碳的單質,石墨在一定條件下可以轉化為金剛石并需要吸收能量,已知12克石墨或金剛石完全燃燒時放出的熱量依次為Q1和Q2,下列說法錯誤的是( )
| A.Q1<Q2 |
| B.石墨不如金剛石穩(wěn)定 |
| C.質量相等的石墨與金剛石,石墨具有的能量比金剛石低 |
| D.質量相等的石墨與金剛石完全燃燒,生成的二氧化碳一樣多 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
用Cl2生產(chǎn)某些含氯有機物時會產(chǎn)生副產(chǎn)物HCl。 利用反應A:4HCl+O2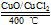 2Cl2+2H2O,
2Cl2+2H2O,
可實現(xiàn)氯的循環(huán)利用。
已知:Ⅰ.反應A中,4mol HCl被氧化,放出115.6kJ的熱量.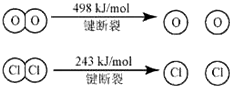
Ⅱ.則斷開1 mol H—O鍵與斷開1 mol H—Cl鍵所需能量相差約為
| A.16kJ | B.24kJ | C.32kJ | D.48kJ |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列有關中和熱的說法正確的是( )
| A.表示中和熱的熱化學方程式:H+(l)+OH-(l)=H2O(l) ΔH=-57.3 kJ/mol |
| B.準確測量中和熱的實驗過程中,至少需測定溫度4次 |
| C.中和熱的實驗過程中,環(huán)形玻璃攪拌棒材料若用銅代替,則測量出的中和熱數(shù)值偏小 |
| D.已知2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l) ΔH=-114.6 kJ/mol,則該反應的中和熱為114.6 kJ/mol |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
已知:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=+49.0 kJ·mol-1
②CH3OH(g)+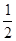 O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
下列說法正確的是
| A.CH3OH轉變成H2的過程一定要吸收能量 |
| B.①反應中,反應物的總能量高于生成物總能量 |
C.根據(jù)②推知反應:CH3OH(l)+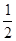 O2(g)=CO2(g)+2H2(g)的ΔH>-192.9 kJ·mol-1 O2(g)=CO2(g)+2H2(g)的ΔH>-192.9 kJ·mol-1 |
| D.反應②中的能量變化如下圖所示 |
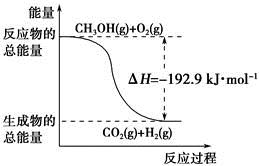
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列說法正確的是( )
| A.需要加熱方能發(fā)生的反應一定是吸熱反應 |
| B.若反應為放熱反應,則該反應不必加熱就可發(fā)生 |
| C.放熱反應比吸熱反應容易發(fā)生 |
| D.化學反應都伴隨著能量的變化 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
常溫下,已知:
4Al(s)+3O2(g)=2Al2O3(s)ΔH1
4Fe(s)+3O2(g)=2Fe2O3(s)ΔH2
下面關于ΔH1、ΔH2的比較正確的是( )
| A.ΔH1>ΔH2 | B.ΔH1<ΔH2 |
| C.ΔH1=ΔH2 | D.無法計算 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
已知:CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH1=-890.3 kJ·mol-1;H2(g)+O2(g)=H2O(l) ΔH2=-285.8 kJ·mol-1。CO2氣體與H2氣體反應生成甲烷氣體與液態(tài)水的熱化學方程式為CO2(g)+4H2(g)=CH4(g)+2H2O(l)ΔH3,其中ΔH3的數(shù)值為( )
| A.-252.9 kJ·mol-1 | B.+252.9 kJ·mol-1 |
| C.-604.5 kJ·mol-1 | D.+604.5 kJ·mol-1 |
查看答案和解析>>
國際學校優(yōu)選 - 練習冊列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com