
【題目】化學與生活、社會發展息息相關,下列有關說法不正確的是( )
A. “青蒿一握,以水二升漬,絞取汁”,屠呦呦對青蒿素的提取屬于化學變化
B. “霾塵積聚難見路人”,霧霾所形成的氣溶膠有丁達爾效應
C. 《本草綱目》記載的“凡酸壞之酒,皆可蒸燒”的實驗方法可用來分離乙酸和乙醇
D. “丹砂(HgS)燒之成水銀,積變又還成了丹砂”,該過程發生了分解、化合、氧化還原反應
 走進文言文系列答案
走進文言文系列答案科目:高中化學 來源: 題型:
【題目】2017年春節,京津冀及周邊區域遭遇“跨年”霧霾,二氧化硫、氮氧化物以及可吸入顆粒物這三項是霧霾主要組成,消除氮氧化物污染是研究方向之一。
(1)用CH4催化還原氮氧化物可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH=-574.0 kJ·mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH=-1160.0 kJ·mol-1
③H2O(g)=H2O(l) ΔH=-44.0 kJ·mol-1
請寫出CH4(g)與NO2(g)反應生成N2(g) ,CO2(g)和H2O(l)的熱化學方程式_______________________ 。
(2)用活性炭還原法處理氮氧化物。有關反應為:C(s)+2NO(g)![]() N2(g)+CO2(g),某研究小組向恒容密閉容器加入一定量的活性炭和NO,恒溫(T0C)條件下反應,反應進行到不同時間測得各物質的濃度如下:
N2(g)+CO2(g),某研究小組向恒容密閉容器加入一定量的活性炭和NO,恒溫(T0C)條件下反應,反應進行到不同時間測得各物質的濃度如下:
濃度(mol/L) 時間(min) | NO | N2 | CO2 |
0 | 0.100 | 0 | 0 |
10 | 0.058 | 0.021 | 0.021 |
20 | 0.040 | 0.030 | 0.030 |
30 | 0.040 | 0.030 | 0.030 |
40 | 0.032 | 0.034 | 0.017 |
50 | 0.032 | 0.034 | 0.017 |
①下列說法不能作為判斷該反應達到化學平衡狀態標志的是_______
A.活性炭的質量 B.v 正(N2) = 2v逆 (NO)
C.容器內壓強保持不變 D.容器內混合氣體的密度保持不變
E.容器內混合氣體的平均相對分子質量保持不變
F.容器內CO2的濃度保持不變
②在T0C時,該反應的平衡常數為______________(小數點后保留兩位有效數字);
③在30 min時,若只改變某一條件,反應重新達到平衡,則改變的條件是___________;
④在50 min時保持溫度和容器體積不變再充入NO和N2,使二者的濃度均增加至原來的兩倍,則化學平衡_______(填“正向移動”、“逆向移動”或“不移動”)
(3)利用反應6NO2+8NH3= 7N2+12H2O構成電池的方法,既能實現有效消除氮氧化物的排放,減輕環境污染,又能充分利用化學能,裝置如圖所示。

①A電極的電極反應式為______________
②下列關于該電池的說法正確的是(_____)
A.電子從右側電極經過負載后流向左側電極
B.為使電池持續放電,離子交換膜需選用陰離子交換膜
C.電池工作一斷時間,溶液的pH不變
D.當有4.48LNO2被處理時,轉移電子物質的量為0.8mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA為阿伏加德羅常數的值。下列說法正確的是
A.高溫下,0.2 mol Fe與足量水蒸氣反應,生成的H2分子數目為0.3NA
B.室溫下,1 L pH=13的NaOH溶液中,由水電離的OH離子數目為0.1NA
C.氫氧燃料電池正極消耗22.4 L(標準狀況)氣體時,電路中通過的電子數目為2NA
D.5NH4NO3![]() 2HNO3+4N2↑+9H2O反應中,生成28 g N2時,轉移的電子數目為3.75NA
2HNO3+4N2↑+9H2O反應中,生成28 g N2時,轉移的電子數目為3.75NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】[2015·新課標全國卷Ⅰ]NA為阿伏加德羅常數的值。下列說法正確的是
A.18 gD2O和18 gH2O中含有的質子數均為10NA
B.2 L 0.5 mol·L1亞硫酸溶液中含有的H+離子數為2NA
C.過氧化鈉與水反應時,生成0.1 mol氧氣轉移的電子數為0.2NA
D.密閉容器中2 mol NO與1 mol O2充分反應,產物的分子數為2NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如下圖為實驗室某濃鹽酸試劑瓶上的標簽,試根據有關數據回答下列問題:

(1)該濃鹽酸的物質的量濃度為___________mol/L。
(2)取用任意體積的該鹽酸溶液時,下列物理量中不隨所取體積的多少而變化的是_________。
A.溶液中HCl的物質的量 B.溶液的濃度
C.溶液中Cl-的數目 D.溶液的密度
(3)某學生現需450 mL物質的量濃度為0.3 mol/L稀鹽酸。
①該學生需要量取___________ mL上述濃鹽酸進行配制。
②配制時正確的操作順序是(用字母表示)________;
A.用30mL水洗滌燒杯2—3次,洗滌液均注入容量瓶,振蕩
B.用量筒準確量取所需濃鹽酸的體積,慢慢沿杯壁注入盛有少量水(約30mL)的燒杯中, 用玻璃棒慢慢攪動,使其混合均勻
C.將已冷卻的鹽酸沿玻璃棒注入500mL的容量瓶中
D.將容量瓶蓋緊,顛倒搖勻
E.改用膠頭滴管加水,使溶液凹面恰好與刻度線相切
F.繼續往容量瓶內小心加水,直到液面接近刻度線1—2cm處
③在配制過程中,下列實驗操作對所配制的稀鹽酸的物質的量濃度有何影響?(填“偏高”或“偏低”或“無影響”)。
I、用量筒量取濃鹽酸時俯視觀察凹液面____________;
II、用量筒量取濃鹽酸后,洗滌量筒2~3次,洗滌液也轉移到容量瓶_________;
III、溶液注入容量瓶前沒有恢復到室溫就進行定容____________。
(4)若在標準狀況下,將V LHCl氣體溶于1L水中,所得溶液密度為d g/mL,則此溶液的物質的量濃度為________mol/L。(填字母)(2分)
![]()
![]()
![]()
![]()
(5)現將100mL 0.5mol/L的鹽酸與200mL 0.1mol/LCuCl2溶液混合,體積變化忽略不計,所得溶液中Cl-的物質的量濃度是_________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】伏打電堆是由幾組鋅和銀的圓板堆積而成,所有的圓板之間夾放著幾張鹽水泡過的布。下圖為最初的伏打電堆模型,由八組鋅和銀串聯組成的圓板堆積而成。下列說法正確的是
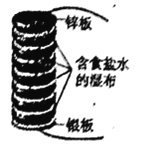
A. 該原電池正極的電極方程式為:O2+4e-+4H+==2H2O
B. 電池長時間工作后,中間的布上會有白色固體顆粒生成,該固體顆粒為Ag2O
C. 當電路中轉移0.2 mol電子時,消耗鋅板的總質量為52 g
D. 該伏打電堆工作時,在銀板附近會有Cl2放出
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】早期火箭發動機使用的推進劑為液氧和汽油。火箭發射過程中,推進劑的燃燒是將( )
A. 化學能轉化為熱能 B. 動能轉化為熱能
C. 化學能轉化為電能 D. 熱能轉化為化學能
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com