
���}Ŀ��ƽ���ҕ�@ʾ�����a(ch��n)�^(gu��)���Юa(ch��n)�������ďU������ĩ![]() ��
��![]() ��
��![]() ��
��![]() ��FeO�����|(zh��)
��FeO�����|(zh��)![]() ij�n�}С�M�Դ˷�ĩ��ԭ�ϣ��O(sh��)Ӌ(j��)��D1��ˇ���̌�(du��)�YԴ�M(j��n)�л��գ��õ�
ij�n�}С�M�Դ˷�ĩ��ԭ�ϣ��O(sh��)Ӌ(j��)��D1��ˇ���̌�(du��)�YԴ�M(j��n)�л��գ��õ�![]() �������F�@�\��
�������F�@�\��

��֪��
��![]() ���ԗl���£����ˮ��Һ����
���ԗl���£����ˮ��Һ����![]() ��
��![]() �ɷN��Ҫ������ʽ��
�ɷN��Ҫ������ʽ��![]() ��ˮ�⣬
��ˮ�⣬![]() ���^��(qi��ng)�����ԣ�
���^��(qi��ng)�����ԣ�
��![]() ������ϡ���
������ϡ���
��![]() �����F�@�\
�����F�@�\![]() �V������ˮ�ă���̎����
�V������ˮ�ă���̎����
![]() �VҺA����Ҫ�ɷ�______
�VҺA����Ҫ�ɷ�______![]() �(xi��)���W(xu��)ʽ
�(xi��)���W(xu��)ʽ![]() ��
��
![]() ��(xi��)������(y��ng)
��(xi��)������(y��ng)![]() ���x�ӷ���ʽ______��
���x�ӷ���ʽ______��
![]() ����(y��ng)
����(y��ng)![]() ֮ǰҪϴ��V��B����(du��)�V��B�M(j��n)��ϴ��Č�(sh��)�(y��n)����������______
֮ǰҪϴ��V��B����(du��)�V��B�M(j��n)��ϴ��Č�(sh��)�(y��n)����������______
![]() ϡ��Ԫ�ص��ἃ��߀�ɲ�����ȡ������֪������HT������ȡ���܌���x�ӏ�ˮ��Һ����ȡ����(l��i)���^(gu��)�̱�ʾ��
ϡ��Ԫ�ص��ἃ��߀�ɲ�����ȡ������֪������HT������ȡ���܌���x�ӏ�ˮ��Һ����ȡ����(l��i)���^(gu��)�̱�ʾ��![]() ˮ��
ˮ��![]() �ЙC(j��)��
�ЙC(j��)��![]() �ЙC(j��)��
�ЙC(j��)��![]() ˮ��
ˮ��![]() ����Һ�õ�
����Һ�õ�![]() �ЙC(j��)��
�ЙC(j��)��![]() ���ټ���
���ټ���![]() �@���^���ĺ�
�@���^���ĺ�![]() ��ˮ��Һ�����x������������ȡ����ԭ����______��
��ˮ��Һ�����x������������ȡ����ԭ����______��
![]() �õζ����y(c��)���Ƶõ�
�õζ����y(c��)���Ƶõ�![]() �a(ch��n)Ʒ���ȣ�
�a(ch��n)Ʒ���ȣ�

����![]() ��Һ�ڿ՚���¶��һ�Εr(sh��)�g�����M(j��n)�еζ����t�y(c��)��ԓ
��Һ�ڿ՚���¶��һ�Εr(sh��)�g�����M(j��n)�еζ����t�y(c��)��ԓ![]() �a(ch��n)Ʒ���|(zh��)����?j��n)?sh��)______
�a(ch��n)Ʒ���|(zh��)����?j��n)?sh��)______![]() ����ƫ��������ƫС�������o(w��)Ӱ���
����ƫ��������ƫС�������o(w��)Ӱ���![]()
![]() ��֪
��֪![]() ������pH������
������pH������![]() ��
��![]() ������pH������
������pH������![]() ��
��![]() ������pH������
������pH������![]() ��
��![]() �r(sh��)
�r(sh��)![]() ������NaOH��Һ����
������NaOH��Һ����![]() �F(xi��n)��
�F(xi��n)��![]() ��Һ
��Һ![]() ����
����![]() �s�|(zh��)
�s�|(zh��)![]() ��(l��i)�Ƃ������F�@�\����(sh��)�(y��n)�п��x�õ�ԇ����
��(l��i)�Ƃ������F�@�\����(sh��)�(y��n)�п��x�õ�ԇ����![]() ��Һ��
��Һ��![]() ��NaOH��Һ���ʯ��ˮ��ϡ
��NaOH��Һ���ʯ��ˮ��ϡ![]() ��Һ��ϡ�}�ᣮ
��Һ��ϡ�}�ᣮ
��(sh��)�(y��n)���E���Ξ飺
![]() ����
����![]() �s�|(zh��)��
�s�|(zh��)��![]() ��Һ�У�����������NaOH��Һ��
��Һ�У�����������NaOH��Һ��![]() ��______��
��______��
![]() ______��
______��
![]() ��
��![]() �еõ�����Һ�м��������@��Һ��______��______�^(gu��)�V��ϴ�졢�������ɣ��������F�@���w
�еõ�����Һ�м��������@��Һ��______��______�^(gu��)�V��ϴ�졢�������ɣ��������F�@���w![]()
���𰸡�![]()
![]() �ز�������©���м����sˮ���](m��i)�^(gu��)��������ˮ��Ȼ���£��؏�(f��)
�ز�������©���м����sˮ���](m��i)�^(gu��)��������ˮ��Ȼ���£��؏�(f��)![]() �� �������ᣬ��ʹƽ�������M(j��n)�У�ʹ
�� �������ᣬ��ʹƽ�������M(j��n)�У�ʹ![]() �M(j��n)��ˮ�� ƫ�� �^(gu��)�V��ϴ�� �������ܽ���������ϡ�����У��������m��
�M(j��n)��ˮ�� ƫ�� �^(gu��)�V��ϴ�� �������ܽ���������ϡ�����У��������m��![]() ��Һ����ַ���(y��ng) ���l(f��)��s ��s�Y(ji��)��
��Һ����ַ���(y��ng) ���l(f��)��s ��s�Y(ji��)��
��������
�U������ĩ![]() ��
��![]() ��
��![]() ��
��![]() ��FeO�����|(zh��)
��FeO�����|(zh��)![]() ����NaOH��Һ��
����NaOH��Һ��![]() ��NaOH��Һ����(y��ng)���ɹ����c��
��NaOH��Һ����(y��ng)���ɹ����c��![]() ��
��![]() ��FeO������(y��ng)��Ȼ���^(gu��)�V���VҺA�к��й����c��NaOH���V��A�к���
��FeO������(y��ng)��Ȼ���^(gu��)�V���VҺA�к��й����c��NaOH���V��A�к���![]() ��
��![]() ��FeO�� ��?y��n)V���м���ϡ���ᣬ
��FeO�� ��?y��n)V���м���ϡ���ᣬ![]() ��FeO�ܽ�����
��FeO�ܽ�����![]() ��
��![]() ��
��![]() ������ϡ���ᣬȻ���^(gu��)�V���VҺB�к���
������ϡ���ᣬȻ���^(gu��)�V���VҺB�к���![]() ��
��![]() �����ᣬ�V��B�к���
�����ᣬ�V��B�к���![]() ��
��
���VҺB�����õ������F��Ȼ��ӟ����l(f��)�����������@��ͨ�^(gu��)���l(f��)��s����s�Y(ji��)���õ������F�@�C�� ���V��B����ϡ������p��ˮ��![]() ���^��(qi��ng)�����ԣ��܌��p��ˮ���������⣬������߀ԭ�õ�
���^��(qi��ng)�����ԣ��܌��p��ˮ���������⣬������߀ԭ�õ�![]() ������Һ�м���A�õ�
������Һ�м���A�õ�![]() �ҝ�Һ����
�ҝ�Һ����![]() �����õ�
�����õ�![]() ��
��
![]() ����(j��)���Ϸ�����ֻ�ж�������������NaOH��Һ�����ԞVҺA����Ҫ�ɷ֞�
����(j��)���Ϸ�����ֻ�ж�������������NaOH��Һ�����ԞVҺA����Ҫ�ɷ֞�![]() ���ʴ𰸞飺
���ʴ𰸞飺![]() ��
��
![]() ����(y��ng)
����(y��ng)![]() ��
��![]() ��
��![]() ������߀ԭ����(y��ng)���p��ˮ�������������⣬�x�ӷ���(y��ng)����ʽ��
������߀ԭ����(y��ng)���p��ˮ�������������⣬�x�ӷ���(y��ng)����ʽ��![]()
![]() ��
��
�ʴ𰸞飺![]()
![]() ��
��
![]() ϴ������ķ����ǣ��ز�������©���м����sˮ���](m��i)�^(gu��)��������ˮ��Ȼ���£��؏�(f��)
ϴ������ķ����ǣ��ز�������©���м����sˮ���](m��i)�^(gu��)��������ˮ��Ȼ���£��؏�(f��)![]() �Σ��Ķ��õ��^�����ij����ز�������©���м����sˮ���](m��i)�^(gu��)��������ˮ��Ȼ���£��؏�(f��)
�Σ��Ķ��õ��^�����ij����ز�������©���м����sˮ���](m��i)�^(gu��)��������ˮ��Ȼ���£��؏�(f��)![]() �Σ��ʴ𰸞飺�ز�������©���м����sˮ���](m��i)�^(gu��)��������ˮ��Ȼ���£��؏�(f��)
�Σ��ʴ𰸞飺�ز�������©���м����sˮ���](m��i)�^(gu��)��������ˮ��Ȼ���£��؏�(f��)![]() �Σ�
�Σ�
![]() �������ᣬ��ʹƽ�������M(j��n)�У�ʹ
�������ᣬ��ʹƽ�������M(j��n)�У�ʹ![]() �M(j��n)��ˮ�ӣ����Կ��x������������ȡ�����ʴ𰸞飺�������ᣬ��ʹƽ�������M(j��n)�У�ʹ
�M(j��n)��ˮ�ӣ����Կ��x������������ȡ�����ʴ𰸞飺�������ᣬ��ʹƽ�������M(j��n)�У�ʹ![]() �M(j��n)��ˮ�ӣ�
�M(j��n)��ˮ�ӣ�
![]() ����
����![]() ��Һ�ڿ՚���¶��һ�Εr(sh��)�g�����M(j��n)�еζ������ց��F�x�ӱ����������F�x�ӣ��t���၆�F��Ƚ��ͣ���(d��o)�����၆�F��Һ�w�e�������Ԝy(c��)��ԓ
��Һ�ڿ՚���¶��һ�Εr(sh��)�g�����M(j��n)�еζ������ց��F�x�ӱ����������F�x�ӣ��t���၆�F��Ƚ��ͣ���(d��o)�����၆�F��Һ�w�e�������Ԝy(c��)��ԓ![]() �a(ch��n)Ʒ���|(zh��)����?j��n)?sh��)ƫ�ʴ𰸞飺ƫ��
�a(ch��n)Ʒ���|(zh��)����?j��n)?sh��)ƫ�ʴ𰸞飺ƫ��
![]() ���x�y���Թ��w����Һ�����^(gu��)�V������������ϴ��õ��^���������|(zh��)�����F�x�Ӻ͚������x�ӷ���(y��ng)���ɳ������\�x�Ӻ��^(gu��)���������x������ƫ�\����x�ӣ�Ȼ������^(gu��)�V�������x���ʴ𰸞飺�^(gu��)�V��ϴ�죻
���x�y���Թ��w����Һ�����^(gu��)�V������������ϴ��õ��^���������|(zh��)�����F�x�Ӻ͚������x�ӷ���(y��ng)���ɳ������\�x�Ӻ��^(gu��)���������x������ƫ�\����x�ӣ�Ȼ������^(gu��)�V�������x���ʴ𰸞飺�^(gu��)�V��ϴ�죻
![]() �����F�������@��ϵõ������F�@�C�����Ԍ������ܽ���������ϡ�����У��������m��
�����F�������@��ϵõ������F�@�C�����Ԍ������ܽ���������ϡ�����У��������m��![]() ��Һ����ַ���(y��ng)�õ������F��Һ���ʴ𰸞飺�������ܽ���������ϡ�����У��������m��
��Һ����ַ���(y��ng)�õ������F��Һ���ʴ𰸞飺�������ܽ���������ϡ�����У��������m��![]() ��Һ����ַ���(y��ng)��
��Һ����ַ���(y��ng)��
![]() ��
��![]() �еõ�����Һ�м��������@��Һ������Һ�Ы@ȡ���w�������l(f��)��s����s�Y(ji��)�����^(gu��)�V��ϴ�졢�������ɵķ������Ķ��õ����w���ʴ𰸞飺���l(f��)��s����s�Y(ji��)����
�еõ�����Һ�м��������@��Һ������Һ�Ы@ȡ���w�������l(f��)��s����s�Y(ji��)�����^(gu��)�V��ϴ�졢�������ɵķ������Ķ��õ����w���ʴ𰸞飺���l(f��)��s����s�Y(ji��)����


 �����u(p��ng)�r(ji��)ϵ�д�
�����u(p��ng)�r(ji��)ϵ�д� ��ӡ�Ļ��n�r(sh��)�y(c��)�u(p��ng)ϵ�д�
��ӡ�Ļ��n�r(sh��)�y(c��)�u(p��ng)ϵ�д� ��(d��o)�W(xu��)�c�y(c��)ԇϵ�д�
��(d��o)�W(xu��)�c�y(c��)ԇϵ�д�
| �꼉(j��) | �����n�� | �꼉(j��) | �����n�� |
| ��һ | ��һ���M(f��i)�n�����]�� | ��һ | ��һ���M(f��i)�n�����]�� |
| �߶� | �߶����M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
| ���� | �������M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�
���}Ŀ�����I(y��)��늽ⷨ̎��������ԏUˮ���õ����|(zh��)Ni��ԭ����D��ʾ��
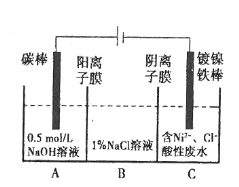
��֪����Ni2+����������Һ�аl(f��)��ˮ��������ԣ�Ni2+(�ߝ��)��H+��Ni2+(�͝��)�������f(shu��)�������_����
A.̼���ϰl(f��)����늘O����(y��ng)��4OH����4e-=O2��+2H2O
B.�������Ni�Įa(ch��n)�ʣ�늽��^(gu��)������Ҫ���ƏUˮpH
C.늽��^(gu��)���У�B��NaCl��Һ�����|(zh��)������Ȍ������p��
D.�D���(y��ng)�x��Ĥȥ������A��B���Һϲ����t늽ⷴ��(y��ng)������ʽ�l(f��)����׃
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�
���}Ŀ��25��r(sh��)����20 mL 0.1 mol��L��1һԪ����HA��Һ�еμ�0. 1 mol�� L��1 NaOH��Һ����Һ��1g[c(A-)/c(HA)]�cpH�P(gu��n)ϵ��D��ʾ�������f(shu��)�����_����

A. A�c(di��n)��(du��)��(y��ng)��Һ�У�c(Na+)��c(A-)��c(H+)��c(OH-)
B. 25��r(sh��)��HA�����x����(sh��)��1. 0�� 10��5.3
C. B�c(di��n)��(du��)��(y��ng)��NaOH��Һ�w�e��10 mL
D. ��(du��)C�c(di��n)��Һ�ӟ�(�����]�]�l(f��))���tc(A-)/[c(HA)c(OH-)]һ������
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�
���}Ŀ�������ЙC(j��)����(y��ng)����ʽ��(sh��)��(xi��)���_���ǣ� ��
A.�����c�Ț��ȡ������(y��ng)��CH4��Cl2![]() CH2Cl2��H2
CH2Cl2��H2
B.�����c�Ҵ�����������(y��ng)��CH3COOH��CH3CH2OH![]() CH3COOCH2CH3
CH3COOCH2CH3
C.�Ҵ��Ĵ���������(y��ng)��CH3CH2OH��O2![]() CH3CHO��H2O
CH3CHO��H2O
D.���c�������������(y��ng)��![]() ��HNO3
��HNO3![]()
![]() ��H2O
��H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�
���}Ŀ���P(gu��n)�����ЈD��Ĕ������_����

A���DI��ʾ������(y��ng)I2(g)+H2(g) ![]() 2HI(g) ��H<0�l(f��)��v-t�P(gu��n)ϵ������t1�r(sh��)�̸�׃�ėl�������ߜض�
2HI(g) ��H<0�l(f��)��v-t�P(gu��n)ϵ������t1�r(sh��)�̸�׃�ėl�������ߜض�
B���D����ʾ��25���r(sh��)���ô�����Һ�ζ�40��00 mL 0��1000 mol��L-1NaOH��Һ�ĵζ�����(xi��n)������c(CH3COOH)=0��1000mol/L
C���D����ʾ������(y��ng)2NO2(g) ![]() N2O4(g)��ƽ���wϵ�У�N2O4�İٷֺ����c�ضȣ�T��������(qi��ng)��P����׃���P(gu��n)ϵ��������H<0��P1<P2
N2O4(g)��ƽ���wϵ�У�N2O4�İٷֺ����c�ضȣ�T��������(qi��ng)��P����׃���P(gu��n)ϵ��������H<0��P1<P2
D���D����ʾ��25���r(sh��)���քeϡጵ��w�e����pH��NaOH��Һ�c��ˮ�r(sh��)��pH׃������������(xi��n)a��(du��)��(y��ng)��ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�
���}Ŀ���������|(zh��)һ������ͬϵ����ǣ� ��
��![]() ��
��![]() ��
��![]() ��C2H4 ��CH2=CH-CH=CH2 ��C3H6 ��
��C2H4 ��CH2=CH-CH=CH2 ��C3H6 ��![]() ��
��![]()
A.�ܺ͢�B.�١��ں͢�C.�ݡ��ߺ͢�D.�͢�
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�
���}Ŀ����֪��CH3��CH=CH2��HBr�D��CH3��CHBr��CH3(��Ҫ�a(ch��n)��)��1 molij�NA���ȼ������Եõ�8molCO2��4mol H2O��ԓ�NA�ڲ�ͬ�l�����ܰl(f��)����D��ʾ��һϵ��׃���������f(shu��)�����_���ǣ� ��
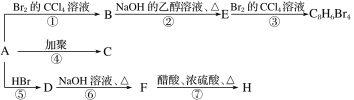
A.A�ĽY(ji��)��(g��u)��(ji��n)ʽC8H10
B.C�ĽY(ji��)��(g��u)��(ji��n)ʽ![]()
C.D��F�ķ���(y��ng)�(l��i)������ȥ����(y��ng)
D.B��E����(y��ng)�Ļ��W(xu��)����ʽ��![]() +NaOH
+NaOH![]()
![]() +NaBr
+NaBr
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�
���}Ŀ����������(j��)�ữ�W(xu��)����ʽ�ó��ĽY(ji��)Փ���_����![]()
A.��֪![]()
![]() ���t��
���t��![]() gNaOH��ϡ��Һ�cϡ������ȫ�кͣ��ų��ğ���С��
gNaOH��ϡ��Һ�cϡ������ȫ�кͣ��ų��ğ���С��![]()
B.��֪![]()
![]() ���t��(bi��o)�r��1mol�����ȫȼ���ų�
���t��(bi��o)�r��1mol�����ȫȼ���ų�![]() kJ�ğ���
kJ��
C.��֪![]()
![]() ��
��![]()
![]() ���t
���t![]()
D.��֪P![]() ���ף�
���ף�![]()
![]() �t�ף�
�t�ף�![]() ���t���ױȼt��(w��n)��
���t���ױȼt��(w��n)��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�
���}Ŀ�����Ȼ�����(S2Cl2)��һ�N��Ҫ�Ļ���ԭ�ϣ����������z������׃�����z�ܟ�l(f��)ճ������׃Ӳ�����|(zh��)������Y�Ͽ�֪S2Cl2�����������|(zh��)��
�������|(zh��) | ���� | ɫ�B(t��i) | �]�l(f��)�� | ���c(di��n) | ���c(di��n) |
���� | ���SɫҺ�w | �ד]�l(f��) | ��76�� | 138�� | |
���W(xu��)���|(zh��) | ��300��������ȫ�ֽ⣻ ��S2Cl2+Cl2 �����ߟ���c������|��������ȼ����Σ�U(xi��n)�� ���ܟ����ˮ�ֽ�şᣬ�ų����g�ԟ��⣻ | ||||
��1����ȡ����S2Cl2
��(sh��)�(y��n)�ҿ��������c�����Ț���110��140�淴��(y��ng)�Ƶ�S2Cl2��Ʒ��
�كx��m�����Q(ch��ng)��___���b��F��ԇ����������___��
���b���B�����A��___��E��D��
�ی�(sh��)�(y��n)ǰ���_(k��i)K1��ͨ��һ�Εr(sh��)�g�ĵ�?d��)��űM�b�Ã�(n��i)�՚⡣��(sh��)�(y��n)�Y(ji��)��ֹͣ�ӟ����ͨ��һ�Εr(sh��)�g�ĵ�?d��)⣬��Ŀ���?/span>___��
�ܞ������S2Cl2�ļ��ȣ���(sh��)�(y��n)���P(gu��n)�I�ǿ��ƺÜضȺ�___��
��2����S2Cl2��ˮ��(qi��ng)�ҷ���(y��ng)�a(ch��n)�����F����a(ch��n)������һ�N���wX��ʹƷ�t��Һ��ɫ���ӟ���ֻ֏�(f��)ԭ��ҷ���(y��ng)�^(gu��)����ֻ��һ�NԪ�ػ��σr(ji��)�l(f��)��׃������(xi��)��ԓ����(y��ng)�Ļ��W(xu��)����ʽ___��
�ڼ�ͬ�W(xu��)�����(y��n)�C�ɷN���w�a(ch��n)���ˮ�����ɵĚ��w����ͨ�^(gu��)�����y�cϡ����Ļ����Һ��Ʒ�t��Һ��NaOH ��Һ��ԓ����___������С������С�����ԭ����___��
��3��ijͬ�W(xu��)���˜y(c��)��S2Cl2�cˮ����(y��ng)�����ɵĚ��wX�ڻ�Ϛ��w�е��w�e��?j��n)?sh��)���O(sh��)Ӌ(j��)������(sh��)�(y��n)������

��W��Һ������___(���(bi��o)̖(h��o))��
a��H2O2��Һ b��KMnO4��Һ(�����ữ) c����ˮ
��ԓ��Ϛ��w�К��wX���w�e��?j��n)?sh��)��____(�ú�V��m��ʽ�ӱ�ʾ)��
�鿴�𰸺ͽ���>>
��(gu��)�H�W(xu��)У��(y��u)�x - ����(x��)��(c��)�б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��(b��o)ƽ�_(t��i) | �W(w��ng)���к���Ϣ�e��(b��o)��(zhu��n)�^(q��) | ����p�_�e��(b��o)��(zhu��n)�^(q��) | ��vʷ̓�o(w��)���x�к���Ϣ�e��(b��o)��(zhu��n)�^(q��) | �����֙�(qu��n)�e��(b��o)��(zhu��n)�^(q��)
�`���Ͳ�����Ϣ�e��(b��o)�Ԓ(hu��)��027-86699610 �e��(b��o)�]�䣺58377363@163.com