
【題目】有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 和
和![]() 六種粒子,屬于同一氧化還原反應中的反應物和生成物,下列敘述不正確的是
六種粒子,屬于同一氧化還原反應中的反應物和生成物,下列敘述不正確的是
A.被氧化和被還原的離子數目比為![]()
B.該反應說明![]() 、
、![]() 、、
、、![]() 在溶液不能大量共存
在溶液不能大量共存
C.每![]() 發生氧化反應,轉移
發生氧化反應,轉移![]()
D.若利用該反應設計原電池,則負極反應為:![]()
【答案】C
【解析】
由題意可以確定,鐵元素的化合價升高,N元素的化合價格下降低,則有8Fe2++NO3-+10H+=8Fe3++NH4++3H2O,該反應中氧化劑(NO3-)與還原劑(Fe2+)物質的量之比為1:8; 若有lmol NO3- 發生還原反應,轉移電子數為8mol;若把該反應設計成原電池,負極反應為Fe2+-e-=Fe3+,據此分析。
A.反應中氧化劑![]() 與還原劑
與還原劑![]() 物質的量之比為1:8,故A正確;
物質的量之比為1:8,故A正確;
B.酸性條件下![]() 可氧化
可氧化![]() ,說明
,說明![]() 、
、![]() 、
、![]() 在溶液不能大量共存,故B正確;
在溶液不能大量共存,故B正確;
C.若有![]() 發生還原反應,轉移電子數為8mol,而不是氧化,故C錯誤;
發生還原反應,轉移電子數為8mol,而不是氧化,故C錯誤;
D.若把該反應設計成原電池,負極發生氧化反應,電極反應為![]() ,故D正確。
,故D正確。
故選C。


科目:高中化學 來源: 題型:
【題目】電致變色玻璃以其優異的性能將成為市場的新寵。如圖所示為五層膜的玻璃電致變色系統,其工作原理是:在外接電源下,通過在膜材料內部發生氧化還原反應,實現對器件的光透過率進行多級可逆性調節。(已知:WO3和Li4Fe4[Fe(CN)6]3均為無色透明,LiWO3和Fe4[Fe(CN)6]3均為藍色)下列有關說法正確的是

A. 當B外接電源負極時,膜由無色變為藍色
B. 當B外接電源負極時,離子儲存層發生反應為:Fe4[Fe(CN)6]3+4Li++4eˉ=Li4Fe4[Fe(CN)6]3
C. 當A接電源的負極時,此時Li+得到電子被還原
D. 當A接電源正極時,膜的透射率降低,可以有效阻擋陽光
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列指定反應的化學用語表達正確的是( )
A | 質子交換膜氫氧燃料電池的負極反應 | O2+2H2O+4e﹣=4OH﹣ |
B | 用鐵電極電解飽和食鹽水 | 2Cl﹣+2H2O=Cl2↑+H2↑+20H﹣ |
C | 鍋爐水垢中的CaSO4用飽和Na3CO3溶液浸泡 | CO32﹣+CaSO4=CaCO3+SO42﹣ |
D | KClO堿性溶液與Fe(OH)3反應制取K2FeO4 | 3ClO﹣+2Fe(OH)3=2FeO43﹣+3Cl﹣+4H++H2O |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】高分子材料在疫情防控和治療中起到了重要的作用。下列說法正確的是
A.聚乙烯是生產隔離衣的主要材料,能使酸性高錳酸鉀溶液褪色
B.聚丙烯酸樹脂是3D打印護目鏡鏡框材料的成分之一,可以與NaOH溶液反應
C.天然橡膠是制作醫用無菌橡膠手套的原料,它是異戊二烯發生縮聚反應的產物
D.聚乙二醇可用于制備治療新冠病毒的藥物,聚乙二醇的結構簡式為![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】電化學原理在生產生活中應用十分廣泛。請回答下列問題:
(1)通過SO2傳感器可監測大氣中SO2的含量,其工作原理如圖1所示。
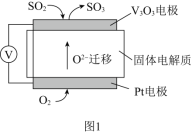
①固體電解質中O2-向______極移動(填“正”或“負”)。
②寫出V2O5電極的電極反應式:_____________。
(2)近期科學家研究發現微生物可將生產廢水中的尿素[CO(NH2)2]直接轉化為對環境友好的兩種物質,其工作原理如圖2所示。回答下列問題:
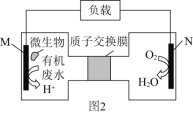
①N極為____極(填“正”或“負”),M電極反應式______________________。
②N極消耗標準狀況下33.6L氣體時,M極理論上處理的尿素的質量為______g。
(3)人工光合系統裝置(如圖)可實現以CO2和H2O合成CH4。下列說法不正確的是__________。
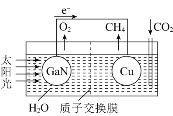
A.該裝置為原電池,且銅為正極
B.電池工作時,H+向Cu電極移動
C.GaN電極表面的電極反應式為2H2O-4e-=O2+4H+
D.反應CO2+2H2O![]() CH4+2O2中每消耗1molCO2轉移4mole-
CH4+2O2中每消耗1molCO2轉移4mole-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】利用微生物燃料電池進行廢水處理,可實現碳氮聯合轉化。某微生物燃料電池的工作原理如圖所示,其中M、N為厭氧微生物電極。下列有關敘述錯誤的是

A.負極反應式為![]()
B.電池工作時,![]() 由M極區移向N極區
由M極區移向N極區
C.相同條件下,M極區生成的![]() 與N極區生成的
與N極區生成的![]() 的體積之比為
的體積之比為![]()
D.好氧微生物反應器中發生的反應的離子方程式為![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】垃圾假單胞菌株能夠在分解有機物的同時分泌物質產生電能,其原理如下圖所示。下列說法正確的是( )

A. 電流由左側電極經過負載后流向右側電極
B. 放電過程中,正極附近pH 變小
C. 若1molO2 參與電極反應,有4 mol H+穿過質子交換膜進入右室
D. 負極電極反應為:H2PCA + 2e-=PCA + 2H+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】室溫下,某同學進行CO2與Na2O2反應的探究實驗,回答下列問題。
(1)用如圖裝置制備純凈的CO2
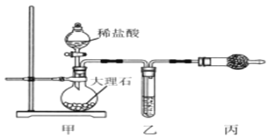
①丙裝置的名稱是__________,乙、丙裝置中盛裝的試劑分別是______、_____。
②若CO2 中混有HCl,則HCl與Na2O2反應的化學方程式為________。
(2)按照下面的裝置圖進行實驗(夾持裝置略)。
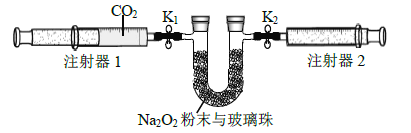
①先組裝儀器,然后_____________,再用注射器1抽取100 mL 純凈的CO2,將其連接在K1 處,注射器2的活塞推到底后連接在K2 處,具支U 形管中裝入足量的Na2O2 粉末與玻璃珠。
②打開止水夾K1、K2,向右推動注射器1的活塞,可觀察到的現象是__________。
③實驗過程中反應的化學方程式為______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】無水四氯化錫(SnCl4)常用作有機合成的氯化催化劑。實驗室可用熔融的錫(熔點231.9C)與Cl2 反應制備SnCl4裝置如下圖所示。
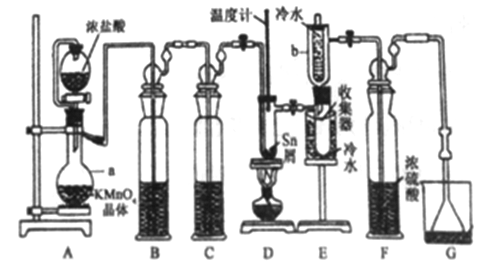
已知,① SnCl4在空氣中極易水解生成SnO2xH2O;②SnCl2、SnCl4有關物理性質如下表。
物質 | 顏色、狀態 | 熔點/℃ | 沸點/℃ |
SnCl2 | 無色晶體 | 246 | 652 |
SnCl4 | 無色液體 | -33 | 114 |
回答下列問題:
(1)儀器a的名稱是__________,其中發生反應的離子方程式為________。
(2)裝置B、C 中盛裝的試劑分別是_______、__________。
(3)當觀察到裝置F液面上方出現_____現象時才開始點燃酒精燈,待錫熔化后適當增大氯氣流量,繼續加熱。此時繼續加熱的目的有:①加快氯氣與錫反應,②__________。
(4)E裝置中b的作用是___________。
(5)若制得產品中含有少量Cl2,則可采用下列_____(填字母)措施加以除去。
A.加入NaOH 萃取分液 B.加入足量錫再加熱蒸餾
C.加入碘化鉀冷凝過濾 D.加入飽和食鹽水萃取
(6)可用滴定法測定最后產品的純度。準確稱取該樣品mg加入到適量濃鹽酸溶解,然后再加水稀釋至250 mL,用移液管移取25.00 ml,稀釋后的溶液于錐形瓶中,加入兩滴淀粉溶液作指示制,用cmol/L 的KIO3 標準溶液進行滴定,平行滴定3 次,平均消耗V mL的標準溶液。已知滴定時發生的反應為:Sn2++IO3-+H+→Sn4++I2+H2O(未配平)。回答下列問題:
①判斷達到滴定終點的現象為____________。
②產品中SnCl2(摩爾質量為M g/mol )的含量為____%(用含m、c、V、M 的代數式表示)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com