
下列實驗事實能用平衡移動原理解釋的是
A. |
B. |
C. |
D.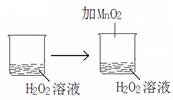 |
AC
解析試題分析:如果改變影響平衡的1個條件,平衡就向能夠減弱這種改變的方向進行,中這就是勒夏特列原理,該原理適用于所有的平衡體系。A、水是弱電解質(zhì),存在電離平衡。加熱促進電離,水的離子積常數(shù)增大,適用于勒夏特列原理,A正確;B、醋酸和次氯酸屬于不同的酸,電離程度不同,不適用于勒夏特列原理,B不正確;C、NO2存在電離平衡2NO2 N2O4,正方應(yīng)是放熱反應(yīng)。加熱抑制電離,NO2的濃度增大,適用于勒夏特列原理,C正確;D、二氧化錳能促進雙氧水的分解,不適用于勒夏特列原理,D不正確,答案選AC。
N2O4,正方應(yīng)是放熱反應(yīng)。加熱抑制電離,NO2的濃度增大,適用于勒夏特列原理,C正確;D、二氧化錳能促進雙氧水的分解,不適用于勒夏特列原理,D不正確,答案選AC。
考點:考查勒夏特列原理的應(yīng)用


 陽光課堂課時作業(yè)系列答案
陽光課堂課時作業(yè)系列答案科目:高中化學(xué) 來源: 題型:單選題
難揮發(fā)性二硫化鉭(TaS2 )可采用如下裝置提純。將不純的TaS2 粉末裝入石英管一端,抽真空后引入適量碘并封管,置于加熱爐中。反應(yīng)如下: TaS2(g)+ 2I2(g) TaI4(g) + S2(g),下列說法錯誤的是
TaI4(g) + S2(g),下列說法錯誤的是
| A.在不同溫度區(qū)域,TaI4 的量不同 |
| B.在提純過程中,S2 的量不斷增多 |
| C.該反應(yīng)的平衡常數(shù)不隨TaI4 和S2 的濃度增大而增大 |
| D.在提純過程中,I2 的作用是將TaS2 從高溫區(qū)轉(zhuǎn)移到低溫區(qū) |
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:單選題
在一體積可變的密閉容器中,加入一定量的X、Y,發(fā)生反應(yīng)mX(g) nY(g) △H=Q kJ·mol-1;反應(yīng)達到平衡時,X的物質(zhì)的量濃度與溫度、氣體體積的關(guān)系如下表所示:
nY(g) △H=Q kJ·mol-1;反應(yīng)達到平衡時,X的物質(zhì)的量濃度與溫度、氣體體積的關(guān)系如下表所示:
| 容器體積/L c(X)/mol·L—1 溫度/℃ | 1 | 2 | 3 |
| 100 | 1.00 | 0.75 | 0.53 |
| 200 | 1.20 | 0. 90 | 0.63 |
| 300 | 1.30 | 1.00 | 0.70 |
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:單選題
下列反應(yīng)常溫時能自發(fā)進行,并既能用能量判據(jù)又能用熵判據(jù)解釋的是
| A.HCl(g)+NH3(g)= NH4Cl(s) |
| B.2KClO3(s)=2KCl(s)+3O2(g) |
| C.2Na2O2(s)+2H2O(l)=4NaOH(s)+O2(g) |
| D.Ba(OH)2·8H2O(s)+2NH4Cl(s)=BaCl2(s)+ 2NH3(g)+10H2O(l) |
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:單選題
鐵片與稀硫酸反應(yīng)時,下列措施不能使氫氣生成速率加快的是
| A.加幾滴濃硫酸 | B.將稀H2SO4加熱 | C.加CH3COONa(s) | D.改用鐵粉 |
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:單選題
T℃時在2L密閉容器中使X(g)與Y(g)發(fā)生反應(yīng)生成Z(g)。反應(yīng)過程中X、Y、Z的物質(zhì)的量變化如圖1所示;若保持其他條件不變,溫度分別為T1和T2時,Y的體積百分含量與時間的關(guān)系如圖2所示。則下列結(jié)論正確的是
A.容器中發(fā)生的反應(yīng)可表示為:3X(g)+Y(g)  2Z(g) 2Z(g) |
| B.反應(yīng)進行的前3 min內(nèi),用X表示的反應(yīng)速率 v(X)=0.3mol/(L·min) |
| C.其他條件不變,升高溫度,反應(yīng)的化學(xué)平衡常數(shù)K減小 |
| D.若改變反應(yīng)條件,使反應(yīng)進程如圖3所示,則改變的條件是增大壓強 |
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:單選題
N2(g)+3H2(g) 2NH3(g) +92.4 kJ。恒容時,體系中各物質(zhì)濃度隨時間變化的曲線如圖示。下列說法錯誤的是
2NH3(g) +92.4 kJ。恒容時,體系中各物質(zhì)濃度隨時間變化的曲線如圖示。下列說法錯誤的是
| A.前20分鐘反應(yīng)內(nèi)放出的熱量為46.2kJ |
| B.第25分鐘改變的條件是將NH3從反應(yīng)體系中分離出去 |
| C.若第60分鐘時反應(yīng)又達到了平衡,則時段Ⅲ改變的條件是增大壓強 |
| D.時段Ⅰ僅將初始投放的物質(zhì)濃度增至原來的2倍,則反應(yīng)物的轉(zhuǎn)化率增大,平衡常數(shù)不變 |
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:單選題
已知298 K,101 kPa時,2SO2(g)+O2(g) 2SO3(g) ΔH=-197 kJ·mol-1。在相同溫度和壓強下,向密閉容器中通入2 mol SO2和1 mol O2,達到平衡時,放出熱量為Q1,向另一個體積相同的容器中通入1 mol SO2,0.5 mol O2和1 mol SO3,達到平衡時放出熱量為Q2,則下列關(guān)系正確的是
2SO3(g) ΔH=-197 kJ·mol-1。在相同溫度和壓強下,向密閉容器中通入2 mol SO2和1 mol O2,達到平衡時,放出熱量為Q1,向另一個體積相同的容器中通入1 mol SO2,0.5 mol O2和1 mol SO3,達到平衡時放出熱量為Q2,則下列關(guān)系正確的是
| A.Q2<Q1<197 kJ·mol-1 | B.Q2=Q1=197 kJ·mol-1 |
| C.Q1<Q2<197 kJ·mol-1 | D.Q2=Q1<197 kJ·mol-1 |
查看答案和解析>>
國際學(xué)校優(yōu)選 - 練習(xí)冊列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com