
由幾種離子化合物組成的混合物,含有以下離子中的若干種:K+、NH、Ba2+、Al3+、Fe3+、Cl-、SO42-、CO32-,將該混合物溶于水后得澄清溶液,現取3份100 mL該溶液分別進行如下實驗:
| 序號 | 實驗內容 | 實驗結果 |
| 1 | 加過量鹽酸 | 無氣體產生 |
| 2 | 加足量NaOH溶液并加熱 | 收集到氣體1.12 L(已折算成標準狀況下的體積),并有紅褐色沉淀生成,將沉淀過濾洗滌、干燥、灼燒,稱重得1.60 g固體。 |
| 3 | 加足量BaCl2溶液時,對所得沉淀進行洗滌、干燥、稱量 | 第一次稱量讀數為2.33 g |
| 陰離子符號 | 物質的量濃度(mol·L-1) |
| | |
| | |
| | |
 提分百分百檢測卷系列答案
提分百分百檢測卷系列答案科目:高中化學 來源: 題型:填空題
(14分)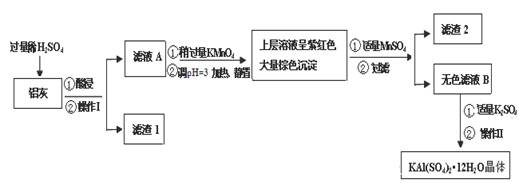
明礬[KAl(SO4)2·12H2O] 在生產、生活中有廣泛用途:飲用水的凈化;造紙工業上作施膠劑;食品工業的發酵劑等。利用煉鋁廠的廢料——鋁灰(含Al 、 Al2O3及少量SiO2和FeO ·xFe2O3)可制備明礬。工藝流程如下:
回答下列問題:
(1)明礬凈水的原理是(用離子方程表示)
(2)操作Ⅰ是 ,操作Ⅱ是蒸發濃縮、 、過濾、 干燥。
(3)檢驗濾液A中是否存在Fe2+的方法是 (只用一種試劑)
(4)在濾液A中加入高錳酸鉀的目的是 ,發生反應的離子方程式為(該條件下Fe2+轉化為Fe3+,MnO4- 轉化為Mn2+) 。
已知:生成氫氧化物沉淀的pH如下表所示
| | Al(OH)3 | Fe(OH)2 | Fe(OH)3 |
| 開始沉淀時 | 3.4 | 6.3 | 1.5 |
| 完全沉淀時 | 4.7 | 8.3 | 2.8 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
某待測溶液中可能含有SO42-、SO32-、CO32-、HCO3-、NO3-、Cl-、Br-中的若干種及一種常見金屬陽離子(Mn+),現進行如下實驗(每次實驗所用試劑均是足量的,鑒定中某些成分可能沒有給出)。
請回答下列問題:
(1)根據上述框圖信息填寫下表(不能確定的不填)。
| | 肯定存在的離子 | 肯定沒有的離子 | 沉淀D | |
| 化學式或離子符號 | | | | |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
氧化還原反應中實際上包含氧化和還原兩個過程,下面是一個還原過程的反應式:NO3-+4H++3e-=NO+2H2O,KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四種物質中的一種物質(甲)能使上述還原過程發生。
(1)寫出并配平該氧化還原反應的化學方程式:________________________。
(2)反應中硝酸體現了________、________的性質。
(3)反應中若產生0.2 mol氣體,則轉移電子的物質的量是________mol。
(4)若1 mol甲與某濃度硝酸反應時,被還原硝酸的物質的量增加,原因是_________________________________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
工業廢水中常含有一定量的Cr2O72—和CrO42—,它們會對人類及生態系統產生很大的傷害,必須進行處理。該法的工藝流程為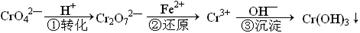
其中第①步存在平衡:2CrO42—(黃色)+2H+ Cr2O72—(橙色)+H2O
Cr2O72—(橙色)+H2O
(1)若平衡體系的pH=2,則溶液顯 色。
(2)能說明第①步反應達平衡狀態的是 。(選填編號)
| A.Cr2O72—和CrO42—的濃度相同 | B.v正(Cr2O72—) ="2v" 逆(CrO42—) |
| C.溶液的顏色不變 | D.溶液的pH值不變 |
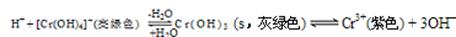
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(創新預測題)(1)①在淀粉碘化鉀溶液中,滴加少量次氯酸鈉堿性溶液,立即會看到溶液變藍色,這是因為________,離子方程式為__________________________。
②在碘和淀粉形成的藍色溶液中,滴加亞硫酸鈉堿性溶液,發現藍色逐漸消失,這是因為______________________________。離子方程式是_______________________________。
③對比①和②實驗所得的結果,將I2、ClO-、SO42—性由強到弱的順序排列為_____________________________。
(2)今有鐵片、銅片,設計實驗證明以下事實,并寫出反應的化學方程式。
①濃硫酸的氧化性比稀硫酸強。________________________________。
②氯化鐵溶液中Fe3+的氧化性比硫酸銅溶液中的Cu2+強。__________________________。
③鐵的還原性比銅強。
___________________________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
現有A、B、C、D、E、F六種常見化合物,已知它們包含的陽離子有K+、Ag+、Na+、
Ba2+、Fe2+、Al3+,陰離子有Cl-、OH-、AlO2-、NO3-、SO42-、CO32-。將它們分別配成0.1 mol/L的溶液進行如下實驗:
①測得溶液A、C、E均呈堿性,且堿性A>E>C,E的焰色呈淺紫色(透過藍色鈷玻璃觀察);②向B溶液中滴加稀氨水至過量,先生成沉淀,后沉淀全部溶解;③向F溶液中滴加稀硝酸,溶液變成棕黃色,且有無色氣體生成;④向D溶液中滴加Ba(NO3)2溶液無明顯現象。
(1)寫出A、D、E、F的化學式:
A________;D________;E________;F________。
(2)用離子方程式解釋C溶液呈堿性的原因:__________________________________。
(3)寫出實驗③中反應的離子方程式:________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
常見的五種鹽A、B、C、D、E,它們的陽離子可能是Na+、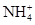 、Cu2+、Ba2+、Al3+、Ag+、Fe3+,陰離子可能是Cl-、
、Cu2+、Ba2+、Al3+、Ag+、Fe3+,陰離子可能是Cl-、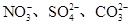 。已知:
。已知:
①五種鹽均溶于水,水溶液均為無色。
②D的焰色反應呈黃色。
③A的溶液呈中性,B、C、E的溶液呈酸性,D的溶液呈堿性。
④若在這五種鹽的溶液中分別加入Ba(NO3)2溶液,只有A、C的溶液不產生沉淀。
⑤若在這五種鹽的溶液中,分別加入氨水,E和C的溶液中生成沉淀,繼續加氨水,C中沉淀消失。
⑥把A的溶液分別加入到B、C、E的溶液中,均能生成不溶于稀硝酸的沉淀。
回答下列問題:
(1)五種鹽中,一定沒有的陽離子是_________________________________________________;
所含的陰離子相同的兩種鹽的化學式是_____________________________________________。
(2)D的化學式為_________,D溶液顯堿性的原因是(用離子方程式表示)________________。
(3)A和C的溶液反應的離子方程式是______________________________________________。
E和氨水反應的離子方程式是______________________________________________________。
(4)若要檢驗B中所含的陽離子,正確的實驗方法是__________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
某Na2CO3、NaAlO2的混合溶液中逐滴加入1 mol·L-1的鹽酸,測得溶液中的C 、HC
、HC 、Al
、Al 、Al3+的物質的量與加入鹽酸的體積變化關系如圖所示,則下列說法正確的是( )
、Al3+的物質的量與加入鹽酸的體積變化關系如圖所示,則下列說法正確的是( )
A.原混合溶液中的C 與Al 與Al 的物質的量之比為1∶2 的物質的量之比為1∶2 |
| B.V1∶V2=1∶5 |
| C.M點時生成的CO2為0.05 mol |
D.a線表示的離子方程式為:Al +H++H2O +H++H2O Al(OH)3↓ Al(OH)3↓ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com