
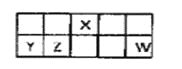
【題目】短周期元素X、Y、Z、W在元素周期表中相對位置如圖所示,其中Y所處的周期序數與族序數相等。按要求回答下列問題:
(1)寫出W的離子結構示意圖________________
(2)比較W 與Z的最高價氧化物對應水化物酸性的強弱 (寫化學式)
(3)寫出X的氫化物的電子式 ,寫出X氫化物的水溶液與X的最高價氧化物對應的水化物的水溶液反應的離子方程式_____________________
(4)已知:①C(s)+ O2(g)= CO2(g) △H="a" kJ· mol-1;
②CO2(g) +C(s)="2CO(g)" △H="b" kJ· mol-1;
③Si(s)+ O2(g)=SiO2(s) △H="c" kJ· mol-1。寫出工業生產中用碳粉還原二氧化硅制取粗硅的熱化學方程式_________________________;
【答案】(1) (2)HClO4>H2SiO3
(2)HClO4>H2SiO3
(3)![]() NH3·H2O+H+=NH4++H2O
NH3·H2O+H+=NH4++H2O
(4)2C(s)+SiO2(s)=Si(s)+2CO(g) △H=(a+b-c)kJ·mol-1
【解析】試題分析:短周期元素X、Y、Z、W在元素周期表中相對位置如圖所示,Y所處的周期序數與族序數相等,短周期元素,則Y為第三周期第ⅢA族元素,即Y為Al,由元素的位置可知,Z為Si,X為N,W為Cl;
(1)Cl原子的核電荷數為16,則Cl-的離子結構示意圖為 ;
;
(2)Cl的非金屬性比Si強,則最高價氧化物對應水化物酸性的強弱HClO4>H2SiO3;
(3)N的氫化物為NH3,其電子式為![]() ;NH3水溶液與N的最高價氧化物對應的水化物HNO3的水溶液反應生成硝酸銨的離子方程式為NH3·H2O + H+= NH4++ H2O;
;NH3水溶液與N的最高價氧化物對應的水化物HNO3的水溶液反應生成硝酸銨的離子方程式為NH3·H2O + H+= NH4++ H2O;
(4)已知①C(s)+O2(g)=CO2(g) △H=akJ·mol-1;
②CO2(g)+C(s)=2CO(g) △H=bkJ·mol-1;
③Si(s)+O2(g)=SiO2(s) △H=ckJ·mol-1,根據蓋斯定律可知①+②-③可得
2C(s)+SiO2(s)=Si(s)+2CO(g),此反應的△H=(a+b-c)kJ·mol-1,
熱化學方程式為2C(s)+SiO2(s)=Si(s)+2CO(g) △H=(a+b-c)kJ·mol-1。


 教材全解字詞句篇系列答案
教材全解字詞句篇系列答案科目:高中化學 來源: 題型:
【題目】下列關于有機化合物的說法正確的是
A. 2-甲基丁烷也稱異丁烷 B. 由乙烯生成乙醇屬于加成反應
C. C4H9Cl有3中同分異構體 D. 油脂和蛋白質都屬于高分子化合物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】反應①Fe(s)+CO2(g)![]() FeO(s)+CO(g) △H1=a kJ/mol;
FeO(s)+CO(g) △H1=a kJ/mol;
②CO(g)+1/2O2(g)![]() CO2(g) △H2=b kJ/mol
CO2(g) △H2=b kJ/mol
測得在不同溫度下,反應①的平衡常數K值隨溫度的變化如下:

(1)若500℃時進行反應①,CO2起始濃度為2 mol·L-1,CO的平衡濃度為__________。
(2)反應①中的a______0(填“大于”“小于”或“等于”)。
(3)700℃反應①達到平衡,要使該平衡正向移動,其他條件不變時,可以采取的措施有_______(填序號)
A.縮小反應器體積 B.通入CO2
C.升高溫度到900℃ D.使用合適的催化劑
(4)下列圖像符合反應①的是____(填序號)(圖中v是速率、![]() 為混合物中CO含量,T為溫度且T1> T2)
為混合物中CO含量,T為溫度且T1> T2)

(5)2Fe(s)+O2(g)![]() 2FeO(s) △H3,該反應的△H3=____________kJ/mol。(用含a、b的代數式表示)
2FeO(s) △H3,該反應的△H3=____________kJ/mol。(用含a、b的代數式表示)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列與化學反應能量變化相關的敘述正確的是
A.生成物的總能量一定低于反應物的總能量
B.拆開物質中的化學鍵一定需要吸收能量
C.應用蓋斯定律,無法計算某些難以直接測量的反應焓變
D.化學反應都伴隨著能量和其他各種現象的出現
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某研究性學習小組設計了一組實驗來探究元素周期律。甲同學根據元素非金屬性與對應最高價含氧酸之間的關系,設計了如圖裝置來一次性完成碳族元素中C與Si的非金屬性強弱比較的實驗研究;乙同學設計了如圖裝置來驗證鹵族元素性質的遞變規律。

據如圖回答:
(1)甲同學設計實驗的依據是____________________________________。
(2)寫出選用的化學試劑:B____________,其作用為___________。
(3)C中反應的離子方程式為____________________________________________。
據如圖回答:
乙同學的實驗過程:
Ⅰ.打開彈簧夾,打開活塞a,滴加濃鹽酸。
Ⅱ.當B和C中的溶液都變為黃色時,夾緊彈簧夾。
Ⅲ.當B中溶液由黃色變為棕紅色時,關閉活塞a。
Ⅳ.打開活塞b,將少量C中溶液滴入D中,關閉活塞b,取下D振蕩,靜置后CCl4層溶液變為紫紅色。
(4)寫出B處反應的離子方程式 ___________________________________________。
(5)A中驗證氯氣的氧化性強于碘的實驗現象是_____________________。
(6)過程Ⅲ實驗的目的是_________________________。
(7)綜合甲、乙兩同學的實驗得出的結論是:同主族元素從上到下元素的非金屬逐漸減弱,其原因是___________________________________________(試從原子結構角度解釋)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】分別在pH=1的酸和pH=14的NaOH溶液中加入足量的鋁,放出H2的量前者多,其原因可能是
①溶液的體積相同,酸是多元強酸
②兩溶液的體積相同,酸是一元弱酸
②酸溶液的體積大于NaOH溶液的體積
④酸是強酸,濃度比NaOH溶液的大
A.①② B.② C.②③ D.④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】X、Y、Z三種短周期元素,原子半徑的大小關系為:r(y)>r(x)>r(z),原子序數之和為16。X、Y、Z三種元素的常見單質在適當條件下可發生下圖所示變化,其中B和C均為10電子分子。下列說法不正確的是
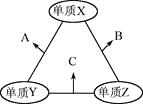
A. X元素位于ⅥA
B. A不能溶解于B中
C. B的沸點高于C的沸點
D. A和C不可能發生氧化還原反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列食品化學知識的敘述正確的是
A. 新鮮蔬菜做熟后,所含維生素C會有損失
B. 油脂、淀粉、蛋白質均為可水解的高分子化合物
C. 纖維素在人體內可水解為葡萄糖,故可作人類的營養物質
D. 磨豆漿的大豆富含蛋白質,豆漿煮沸后蛋白質變成了氨基酸
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列鹵代烴在KOH醇溶液中加熱不反應的是( )
① ![]() ② (CH3)2CHCH2Cl ③ (CH3)3CCH2Cl ④ CHCl2-CHBr2 ⑤
② (CH3)2CHCH2Cl ③ (CH3)3CCH2Cl ④ CHCl2-CHBr2 ⑤ ![]() ⑥ CH2Cl2
⑥ CH2Cl2
A.①③⑥ B.②③⑤ C.全部 D.②④
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com