
【題目】某溫度下,相同pH的兩種弱酸HA和HB分別加水稀釋,pH隨溶液體積變化的曲線如圖所示。下列判斷正確的是( )
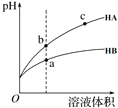
A.酸性:HB> HA
B.結合H+的能力:B->A-
C.導電能力:c > b
D.與氫氧化鈉完全反應時,消耗氫氧化鈉體積Va<Vb
科目:高中化學 來源: 題型:
【題目】鐵及碳的化合物在社會生產、生活中有著廣泛的應用。請回答下列問題:
(1)磁鐵礦是工業上冶煉鐵的原料之一。
已知:①Fe3O4(s)+4C(s)![]() 3Fe(s)+4CO(g) △H=+646.0kJmol﹣1
3Fe(s)+4CO(g) △H=+646.0kJmol﹣1
②C(s)+CO2(g)2CO(g) △H=+172.5kJmol﹣1
則Fe3O4(s)+4CO(g)![]() 3Fe(s)+4CO2(g)△H=___。
3Fe(s)+4CO2(g)△H=___。
(2)反應Fe(s)+CO2(g)![]() FeO(s)+CO(g)△H的平衡常數為K,在不同溫度下,K值如下:
FeO(s)+CO(g)△H的平衡常數為K,在不同溫度下,K值如下:
溫度/K | 973 | 1173 | 1373 | 1573 |
K | 1.47 | 2.15 | 3.36 | 8.92 |
①從表中數據可推斷,該反應是___(填“放熱”或“吸熱”)反應。
②溫度為973K時,在某恒容密閉容器中發生上述反應。下列有關說法能說明該反應已達到平衡狀態的是___(填字母)。
A.c(CO2)=c(CO)
B.v正(CO2)=v逆(CO)
C.體系壓強不變
D.混合氣體中c(CO)不變
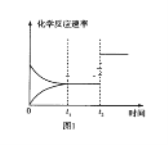
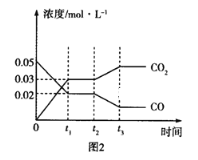
(3)如圖圖1、2表示反應:H2(g)+CO2(g)![]() CO(g)+H2O(g)△H>0有關量與反應時間之間的關系:
CO(g)+H2O(g)△H>0有關量與反應時間之間的關系:
①圖2中若t1=0.5min,則0~t1時間段內,H2O的平均反應速率v(H2O)=___molL﹣1s﹣1。
②圖1中t2時刻改變的條件是___(任寫兩種,下同);圖2中t2時刻改變的條件是___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一種零價鐵納米簇可用于水體修復,其處理三氯乙烯(![]() )所形成原電池如圖所示。水體中
)所形成原電池如圖所示。水體中![]() ,
,![]() ,
,![]() 等離子也發生反應。下列說法正確的是( )
等離子也發生反應。下列說法正確的是( )
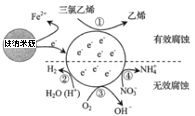
A.零價鐵納米簇發生的電極反應為:Fe-3e-=Fe3+
B.反應①在正極發生,反應②③④在負極發生
C.③的電極反應式為4OH--4e-=O2↑+2H2O
D.三氯乙烯脫去3mol Cl時反應①轉移6mol電子
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】中國科學技術名詞審定委員會已確定第116號元素Lv的名稱為鉝。關于![]() 的敘述錯誤的是( )
的敘述錯誤的是( )
A. 原子序數116B. 中子數177
C. 核外電子數116D. 相對原子質量293
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】草酸鈷用途廣泛,可用于指示劑和催化劑的制備。用含鈷廢料(主要成分為![]() ,還含有一定量的
,還含有一定量的![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 等)制備草酸鈷晶體
等)制備草酸鈷晶體![]() 的工業流程如下圖所示。請回答下列問題:
的工業流程如下圖所示。請回答下列問題:
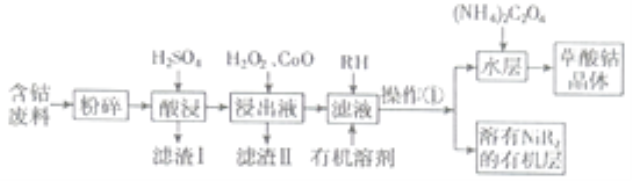
已知:①草酸鈷晶體難溶于水
②![]() 為有機物(難電離)
為有機物(難電離)
③相關金屬離子![]() 形成氫氧化物沉淀的
形成氫氧化物沉淀的![]() 范圍如下:
范圍如下:
金屬離子 |
|
|
|
|
開始沉淀的 | 7.5 | 2.7 | 3.4 | 6.9 |
沉淀完全的 | 9.0 | 3.7 | 4.7 | 8.9 |
(1)濾渣Ⅰ的成分_______。
(2)![]() 是一種綠色氧化劑,寫出加入
是一種綠色氧化劑,寫出加入![]() 后溶液中發生的主要反應的離子方程式______。
后溶液中發生的主要反應的離子方程式______。
(3)加入氧化鈷調節浸出液的![]() 的范圍是______。
的范圍是______。
(4)加入有機溶劑的目的是______。
(5)若僅從沉淀轉化角度考慮,能否利用反應![]() 將
將![]() 轉化為
轉化為![]() ____(填“能”或“不能”),說明理由:______。(已知
____(填“能”或“不能”),說明理由:______。(已知![]() ,
,![]() )
)
(6)為測定制得的草酸鈷晶體樣品的純度,現稱取樣品![]() ,先用適當試劑將其轉化,稀釋后得到純凈的草酸銨溶液
,先用適當試劑將其轉化,稀釋后得到純凈的草酸銨溶液![]() 。移取
。移取![]() 該溶液加入過量的稀硫酸酸化,用
該溶液加入過量的稀硫酸酸化,用![]() 高錳酸鉀溶液滴定,當溶液由__________(填顏色變化),消耗高錳酸鉀溶液
高錳酸鉀溶液滴定,當溶液由__________(填顏色變化),消耗高錳酸鉀溶液![]() ,計算草酸鈷晶體樣品的純度為__________
,計算草酸鈷晶體樣品的純度為__________![]() 。(用含
。(用含![]() 、
、![]() 、
、![]() 的代數式表示)(已知
的代數式表示)(已知![]() 的摩爾質量為
的摩爾質量為![]() )
)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】X、Y、Z和W代表原子序數依次增大的四種短周期元素,它們滿足以下條件:
①元素周期表中,Z與Y相鄰,Z與W也相鄰;②Y、Z和W三種元素的原子最外層電子數之和為17。
請填空:
(1)Y、Z和W是否位于同一周期(填“是”或“否”):__________,理由是________________。
(2)Y是_______,Z是_______,W是_______。
(3)X、Y、Z和W可組成一種化合物,其原子個數比為8∶2∶4∶1,寫出該化合物的名稱及化學式: _______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鹽酸和氫氧化鈉是工業上重要的化工原料,也是實驗室里常見的化學試劑。欲測定某NaOH溶液的物質的量濃度,可用0.1000 mol·L-1 HCl標準溶液進行中和滴定(用酚酞作指示劑)。請回答下列問題:
(1)滴定時,盛裝待測NaOH溶液的儀器名稱為_____。
(2)堿式滴定管用蒸餾水洗凈后,接下來應該進行的操作是_________。
(3)若甲學生在實驗過程中,記錄滴定前滴定管內液面讀數為0.50 mL,滴定后液面如圖,則此時消耗標準溶液的體積為_____。
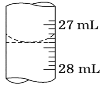
乙學生做了三組平行實驗,數據記錄如下:
實驗序號 | 待測NaOH溶液的體積/mL | 0.1000mol·L-1HCl溶液的體積/mL | |
滴定前刻度 | 滴定后刻度 | ||
1 | 25.00 | 0.11 | 25.10 |
2 | 25.00 | 1.56 | 33.30 |
3 | 25.00 | 0.21 | 25.22 |
(4)選取上述合理數據,計算出待測NaOH溶液的物質的量濃度為______(保留四位有效數字)。
(5)下列哪些操作會使測定結果偏高_____ (填序號)。
A.錐形瓶用蒸餾水洗凈后再用待測液潤洗
B.酸式滴定管用蒸餾水洗凈后再用標準液潤洗
C.滴定前酸式滴定管尖端氣泡未排除,滴定后氣泡消失
D.滴定前讀數正確,滴定后俯視滴定管讀數
(6)滴定達到終點的標志是________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現有部分短周期元素的原子結構如下表:
元素編號 | 元素原子結構 |
X | 原子結構示意圖為 |
Y | 最外層電子數是次外層電子數的2倍 |
Z | 原子核內含有12個中子,且其離子的結構示意圖為 |
(1)寫出X的元素符號:____________,元素Y的最簡單氫化物的化學式為______________。
(2)Z元素原子的相對原子質量為____________。
(3)X和Z兩種元素的最高價氧化物對應的水化物相互反應的離子方程式為______________。
(4)Y和Z兩種元素的最高價氧化物發生氧化還原反應的化學方程式為__________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】冠醚分子中有空穴 ,能夠與金屬離子形成穩定的絡合物,該物質在有機工業中發揮著重要的作用。二環己烷并一18一冠一6(III )的制備原理如圖,下列相關說法錯誤的是
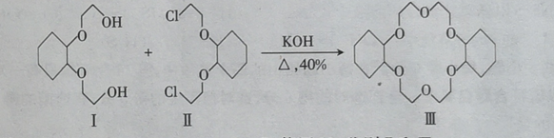
A.反應是取代反應B.能用Na鑒別I和III
C.I不能使酸性高錳酸鉀溶液褪色D.III的一溴取代物有5種
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com