
【題目】A、B、C、D、E、F為原子序數依次增大的前36號元素,其中只有兩種金屬元素。A與C同主族,B與E同主族;B與C能形成兩種常見化合物;C與F最外層只有1個電子,且內層均已排滿;基態D原子成對電子數是未成對電子數的4倍。
請問答下列問題:
(1)基態B原子的軌道表達式為______,其最高能級的電子云有_____個不同的伸展方向。
(2)B、C、E原子半徑由大到小的順序為_________(用元素符號表示)。
(3)D和E中第一電離能較大的是_______(填元素符號),原因為___________。
(4)A與B形成的最簡單化合物比A與E形成的最簡單化合物的熔點______(填“高“或“低”),原因為___________。
(5)D的最高價氧化物對應的水化物中,D原子的雜化軌道類型為______,已知該分子中除氫外其他原子均滿足最外層8電子穩定結構,則其結構式為________。
(6)單質F及其同族元素P、Q的堆積模型均為面心立方最密堆積,三種原子的半徑分別為128pm、144pm、144pm,其中P和Q的相對原子質量分別為Mτ(P)、Mτ(Q)。
①單質F中的配位數為______;密度為_____g/cm3(用NA表示阿伏加德羅常數的值,列式即可)。
②單質P和Q的密度之比為________[用含Mτ(P)、Mτ(Q)的代數式表示]。
【答案】 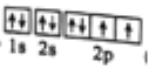 3 Na>S>O P P的3p軌道處于半充滿狀態,較難失去1各電子 高 水分子間較易形成氫鍵 sp3
3 Na>S>O P P的3p軌道處于半充滿狀態,較難失去1各電子 高 水分子間較易形成氫鍵 sp3 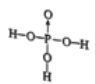 12
12 ![]()
![]()
【解析】根據題意可推斷A、B、C、D、E、F分別為H、O、Na、P、S、Cu。
(1)基態B原子的軌道表達式為![]() 其最高能級的電子云有3個不同的伸展方向。
其最高能級的電子云有3個不同的伸展方向。
(2)根據電子層數和核內質子數的關系可得原子半徑:r(Na)>r(S)>r(O)。
(3)P的3p軌道處于半充滿狀態,較難失去一個電子,所以第一電離能較大。
(4)水分子間較易形成氫鍵,所以熔點較高。
(5)D的最高價氧化物對應的水化物為H3PO4,分子的中心P原子為sp3雜化,除氫外其他原子均滿足最外層8電子穩定結構,可知P與O之間形成了一個配位鍵,結構式為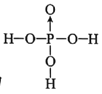 。
。
(6)①面心立方最密堆積的配位數為12;其密度為![]() 。
。
②P與Q的堆積方式相同,原子半徑相同,所以密度之比即為摩爾質量之比,即相對原子質量之比。


科目:高中化學 來源: 題型:
【題目】Ⅰ.下面列出了幾組物質,請將物質的合適序號填寫在空格上。
①金剛石和石墨 ②D和T ③12C和13C ④O2和O3
⑤CH4和CH3CH2CH3 ⑥CH2=CHCH3和CH2=CH2
⑦CH3CH(CH3)CH2CH3和CH3(CH2)3CH3 ⑧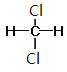 和
和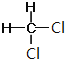
同系物____________;同分異構體____________。
Ⅱ.籃烷分子的鍵線式如圖所示,試回答:
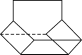
籃烷的一氯代物的種數為________種(不考慮立體異構)。
Ⅲ.在一定溫度下,體積為2 L的恒容密閉容器中,NO2和N2O4之間發生反應2NO2(g) ![]() N2O4(g),如圖所示。
N2O4(g),如圖所示。
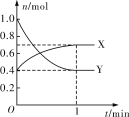
(1)曲線____________ (填“X”或“Y”)表示NO2的物質的量隨時間的變化曲線。
(2)該反應達到限度時,Y的轉化率是__________,反應開始時與反應達到平衡狀態時的壓強之比為__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將CO2轉化為甲醇的原理為 CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H<0.500℃時,在體積為1L 的固定容積的密閉容器中充入1mol CO2、3mol H2 , 測得CO2濃度與CH3OH 濃度隨時間的變化如圖所示,從中得出的結論錯誤的是( ) 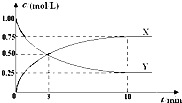
A.曲線X可以表示CH3OH(g) 或H2O(g) 的濃度變化
B.從反應開始到10min時,H2的反應速率v(H2)=0.225mol/(L﹒min)
C.平衡時H2 的轉化率為75%
D.500℃時該反應的平衡常數K=3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A、B、C、D、E為原子序數依次增大的短周期元素,對應單質為a、b、c、d、e。B、C、D的最外層電子數之和為10,對應的最高價氧化物的水化物分別為m、n、p;q為B和E形成的二元化合物。上述物質發生的轉化關系如圖所示(部分產物已略去)。下列說法不正確的是
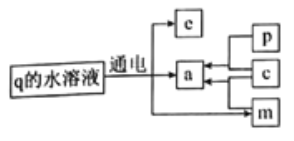
A. 可通過電解熔融狀態的q制備b和e
B. 原子半徑:B>C>D>E>A
C. n既能溶解在m的水溶液中,又能溶解在p的水溶液中
D. d可以保存在CS2中
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據問題填空:
(1)2SO2(g)+O2(g)2SO3(g)反應過程的能雖變化如圖所示.己知1mol SO2(g)氧化為1mol SO3(g)的△H=﹣99kJ/mol. 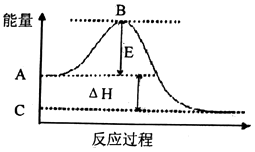
請回答下列問題:
①E的大小對該反應的反應熱(填“有”或“無”)影構.
②圖中△H=kJ/mol.
(2)由氫氣和氧氣反應生成1mol水蒸氣,放出241.8kJ熱量(25℃、101kPa下測得) ①寫出該反應的熱化學方程式: .
②若lmol水蒸氣轉化為液態水放熱45kJ,則反應H2(g)+ ![]() O2(g)=H2O(l)的△H=kJ/mol.
O2(g)=H2O(l)的△H=kJ/mol.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖是一個化學過程的示意圖. 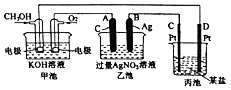
(1)通入O2的電極名稱、C(Pt)電極的名稱是 .
(2)寫出通入O2的電極上的電極反應式是 .
(3)寫出通入CH3OH的電極上的電極反應式是 .
(4)若丙池是電解飽和食鹽水溶液,則陽極的電極反應為 , 陰極的電極反應為 . 在(陽極或陰極)附近滴入酚酞溶液變紅.
(5)乙池中反應的化學方程式為 .
(6)當乙池中B(Ag)極的質里增加5.40g時,甲池中理論上消耗O2mL(標準狀況下);若丙池中飽和食鹽水溶液的體枳為500mL,電解后,溶液的pH= . (25℃,假設電解前后溶液的體積無變化).
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學反應A2+B2=2AB的能量變化如圖所示,則下列說法正確的是( ) 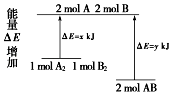
A.該反應的反應熱△H=x﹣y kJ/mol
B.斷裂1 mol A﹣A鍵和1 mol B﹣B鍵放出x kJ能量
C.2 mol AB的總能量高于1 mol A2和1 mol B2總能量
D.該反應是吸熱反應
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com