
在2 L密閉容器中進行反應:mX(g)+nY(g) pZ(g)+qQ(g),式中m、n、p、q為化學計量數。在0~3 min內,各物質物質的量的變化如下表所示:
pZ(g)+qQ(g),式中m、n、p、q為化學計量數。在0~3 min內,各物質物質的量的變化如下表所示:
| 物質 時間 | X | Y | Z | Q |
| 起始/mol | 0.7 | | 1 | |
| 2 min末/mol | 0.8 | 2.7 | 0.8 | 2.7 |
| 3 min末/mol | | | 0.8 | |
 暑假銜接教材期末暑假預習武漢出版社系列答案
暑假銜接教材期末暑假預習武漢出版社系列答案 假期作業暑假成長樂園新疆青少年出版社系列答案
假期作業暑假成長樂園新疆青少年出版社系列答案科目:高中化學 來源: 題型:填空題
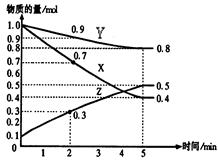
某溫度時,在2L容器中X、Y、Z三種物質隨時間的變化關系曲線如下圖所示。
(1)由圖中的數據分析,該反應的化學方程式為 ;
(2)反應開始至2min時Z的平均反應速率為 ;
(3)下列關于化學反應速率與化學反應限度的敘述不正確的是 ( )
| A.反應限度是一種平衡狀態,此時反應已經停止 |
| B.達到平衡狀態時,正反應速率和逆反應速率相等 |
| C.達到平衡狀態時,反應物和生成物濃度都不再改變 |
| D.化學反應速率理論是研究怎樣在一定時間內快出產品 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
在溶液中,反應A+2B C分別在三種不同實驗條件下進行,它們的起始濃度均為c(A)=0.100 mol/L、c(B)=0.200 mol/L及c(C)=0 mol/L。反應物A的濃度隨時間的變化如下圖所示。
C分別在三種不同實驗條件下進行,它們的起始濃度均為c(A)=0.100 mol/L、c(B)=0.200 mol/L及c(C)=0 mol/L。反應物A的濃度隨時間的變化如下圖所示。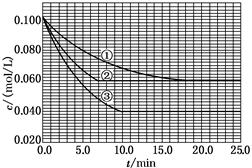
請回答下列問題:
(1)與①比較,②和③分別僅改變一種反應條件。所改變的條件和判斷的理由是:
②______________________________________________;
③______________________________________________;
(2)實驗②平衡時B的轉化率為________;實驗③平衡時C的濃度為________________;
(3)該反應的ΔH________0,其判斷理由是_________________________________;
(4)該反應進行到4.0 min時的平均反應速率:
實驗②:vB=________;
實驗③:vC=________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
在一定體積的密閉容器中,進行如下化學反應:CO2(g)+H2(g) CO(g)+H2O(g),其化學平衡常數K和溫度t的關系如下表所示:
CO(g)+H2O(g),其化學平衡常數K和溫度t的關系如下表所示:
| t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
一定溫度下某容積固定的密閉容器中加入2 mol A和1 mol B,發生如下反應:2A(g)+B(g)  3C(g)+D(s) ΔH=-Q kJ·mol-1(Q>0),當反應達到平衡后,反應放出的熱量為Q1 kJ,物質A的轉化率為α。請回答下列問題:
3C(g)+D(s) ΔH=-Q kJ·mol-1(Q>0),當反應達到平衡后,反應放出的熱量為Q1 kJ,物質A的轉化率為α。請回答下列問題:
(1)Q1________Q(填“<”、“>”或“=”),理由是__________________________。
(2)A的轉化率α=________(用含Q、Q1的代數式表示);平衡后,若加入少量物質D,A的轉化率會________(填“增大”、“減小”或“不變”)。
(3)反應達到平衡后,若升高溫度,K________(填“增大”、“減小”或“不變”),混合氣體的平均相對分子質量________(填“增大”、“減小”或“不變”)。
(4)維持溫度不變,若起始時向容器中加入的物質如下列四個選項,則反應達到平衡后放出的熱量仍為Q1 kJ的是(稀有氣體不參與反應)________(填字母)。
A.2 mol A、1 mol B、1 mol Ar
B.3 mol C、1 mol D
C.1 mol A、0.5 mol B、1.5 mol C、0.5 mol D
D.2 mol A、1 mol B、1 mol D
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
某火電廠的脫硫尾氣通入飽和K2CO3溶液吸收池后,經分解池制得純凈的CO2,再在合成塔與H2反應生成甲醇。其工藝藝流程示意圖如下:
(1)吸收池中飽和K2CO3溶液吸收CO2的離子方程式是 。
(2)流程示意圖中循環使用的物質是 。
(3)300℃時,合成塔中的反應為CO2(g)+3H2(g) CH3OH(g)+H2O(g),在密閉條件下,下列示意圖能說明反應進行到t1時刻時達到平衡狀態的是 (填字母序號)
CH3OH(g)+H2O(g),在密閉條件下,下列示意圖能說明反應進行到t1時刻時達到平衡狀態的是 (填字母序號)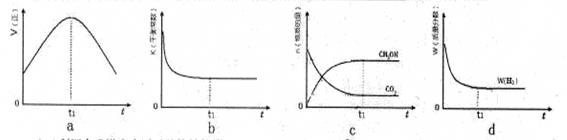
(4)利用合成塔中失活后的鉻鋅觸媒可制得含有Cl- 和CrO42- 的溶液,其濃度均為0.01mol/L,向該溶液中逐滴加入0.01mol/L的AgNO3溶液時,首先產生沉淀的陰離子是 (已知:Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=9.0×10-12)
(5)合成塔中失活的鉻鋅觸媒可用于制備鋅錳電池。在堿性條件下,該電池的總反應為:Zn(s) +2MnO2(s) +H2O(l) = Zn(OH)2(s) +Mn2O3(s) ,該電池正極的電極反應式是 。若用電池電解(惰性電極)足量的Mg(NO3)2和NaCl的混合溶液,電解過程中陰極的現象是 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
將一定量NO2和N2O4的混合氣體通入體積為2 L的恒溫密閉容器中,各物質濃度隨時間變化的關系如圖1所示。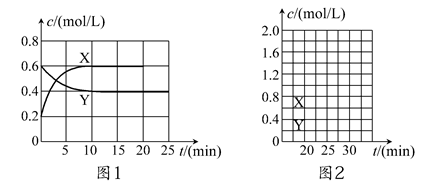
請回答:
(1)圖l中,曲線________(填“X”或“Y”)表示NO2濃度隨時間的變化情況;前10 min內v(NO2)=________mol/(L·min)。
(2)下列選項中不能說明該反應已達到平衡狀態的是________(填選項字母)。
| A.容器內混合氣體的壓強不隨時間變化而改變 |
| B.容器內混合氣體的密度不隨時間變化而改變 |
| C.容器內混合氣體的顏色不隨時間變化而改變 |
| D.容器內混合氣體的平均相對分子質量不隨時間變化而變化 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
10000C時,硫酸鈉可與氫氣發生反應:

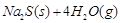 。請回答下列問題:
。請回答下列問題:
(1)上述反應的平衡常數表達式為: 。
(2)上述反應在三個不同條件下進行,其中H2的濃度隨時間的變化如圖所示。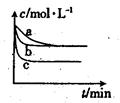
①與曲線a比較,b和c分別僅改變一種反應條件,則曲線b改變的條件為
②該反應的△H___0(填“>”、“<”或“=”),其判斷理由是 。
(3)該溫度下,向2L盛有1.42g Na2SO4的密閉容器中通入H2,5min后測得
固體質量為1.10g。則該時間范圍內的平均反應速率v(H2)= 。
(4)能說明該反應已達到平衡狀態的是 (填字母,下同)。
a.容器內壓強保持不變
b.容器內氣體密度保持不變
c.c(H2)=c(H2O)d.v正(H2)=v逆(H2O)
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
下列可以證明H2(g)+I2(g) 2HI(g)已達平衡狀態的是 。
2HI(g)已達平衡狀態的是 。
①單位時間內生成n mol H2的同時,生成n mol HI
②一個H—H鍵斷裂的同時有兩個H—I鍵斷裂
③百分含量w(HI)=w(I2)
④反應速率v(H2)=v(I2)=v(HI)
⑤c(HI)∶c(H2)∶c(I2)=2∶1∶1
⑥溫度和體積一定時,生成物濃度不再變化
⑦溫度和體積一定時,容器內壓強不再變化
⑧條件一定,混合氣體的平均相對分子質量不再變化
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com