
科目: 來源: 題型:
【題目】為驗證“加熱碳酸氫銨”所發生的變化和產物,兩同學分別用甲、乙所示裝置進行實驗。

(1)甲實驗中的現象是_______________。
(2)乙實驗中試管口略向下傾斜的原因是_______________。乙實驗中燒杯內反應化學方程式為_______________;實驗中棉花逐漸變紅色,則可說明反應產物中有_______________;相對于甲實驗來說,乙實驗的優點有(寫一條)_______________。
(二)將一定量的K2CO3溶液與BaCl2溶液混合,過濾反應后的混合物。某興趣小組的同學們欲探究濾液中溶質的組成。請你一同參與探究并回答有關問題:
[查閱資料]K2CO3溶液顯堿性; BaCl2、 KCl溶液顯中性。
[提出猜想]猜想1:濾液溶質是KCl;
猜想2:濾液溶質是_______________。
猜想3:濾液溶質是KCl和K2CO3。
[實驗探究]
實驗操作 | 實驗現象 | 實驗結論 |
① 取少量濾液于試管中,滴幾滴無色酚酞試液,振蕩 | 無明顯現象 | ①猜想_________不成立 |
② 另取少量濾液于另一支試管中,滴加K2CO3溶液 | ______________ | ②猜想2成立。 寫出相關的化學方程式 _____________ |
[問題討論]小麗同學認為要證明猜想2成立也可改用AgNO3溶液,你認為小麗同學不能達到實驗目的,你的理由是_______________。
[反思拓展]實驗結束后,組內同學認為K2CO3是鹽而其水溶液卻顯堿性,這可能與它的構成微粒有關,微粒符號是_______________。
查看答案和解析>>
科目: 來源: 題型:
【題目】某實驗小組利用廢硫酸溶液制備K2SO4的流程如下:

(1)將CaCO3研成粉末的目的是___________________。
(2)上述流程中可循環使用的物質有CO2和__________________(填寫化學式);
(3)洗滌反應Ⅲ所得晶體不用水而用飽和K2SO4溶液的目是___________________。
(4)檢驗反應Ⅲ所得晶體是否洗干凈的方法是:取最后次洗滌液, 先加入過量的Ba(NO3)2溶液,振蕩、過濾,再向濾液中滴加_______________, 如果沒有白色沉淀,說明洗滌干凈。
查看答案和解析>>
科目: 來源: 題型:
【題目】實驗室中用如下實驗來研究鐵、鋁、銅三種金屬活動順序及其在活動順序表中相對氫的位置。
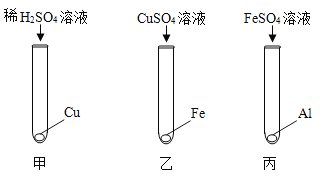
(1)乙實驗的現象為___________________。
(2)丙實驗中反應的化學方程式___________________。
(3)若將上述實驗之一替換掉一種藥品,即可達成實驗目的.說明具體的改進方法:___________________。
(4)按如圖實驗結束后,將乙、丙實驗后的剩余物傾倒至一個燒杯中, 充分反應。然后將甲實驗的剩余物倒入此燒杯,無氣泡產生。以下說法正確的是___________________。
A 最后燒杯中的溶液不可能是無色的
B 乙實驗中,CuSO4溶液一定是過量的
C 乙、丙混合過程中,可能沒有發生化學反應
D 最后燒杯中的溶液,一定含有Al2 (SO4) 3,可能含有FeSO4。
查看答案和解析>>
科目: 來源: 題型:
【題目】請用你具備的化學知識回答下面問題:
(1)收集二氧化碳不能用排水法原因是_____________________。
(2)夏天鐵軌之間的縫隙變小的微觀原因是_____________________。
(3)“潔廁靈”與“漂白精”不能混用,兩者若混合易產生一種有毒氣體X。 反應原理為:![]() ,則X的化學式為_____________________。
,則X的化學式為_____________________。
(4)暖氣片表面常刷“銀粉”(主要成分是鋁)利用的是_____________________。
查看答案和解析>>
科目: 來源: 題型:
【題目】請按要求用符號完成下面問題:
(1)標出硫酸銨中氮元素的化合價__________________________。
(2) 由H、C、O、Na四種元素組成的一種鹽的化學式_____________________。
(3)由60個碳原子構成的單質分子_____________________。
(4) 黃銅的主要成分_____________________。
查看答案和解析>>
科目: 來源: 題型:
【題目】甲、乙兩種物質的溶解度曲線如圖所示,下列說法正確的是()

A.t1°C時, 甲、乙兩種溶液中溶質的質量相等
B.要將甲溶液的狀態由a點轉化為b點,可以加適量溶劑
C.t1°C時,100g 甲物質的飽和溶液中溶質的質量是20g
D.分別將t2°C時兩種物質的飽和溶液降溫至t1°C,均有晶體析出
查看答案和解析>>
科目: 來源: 題型:
【題目】工業純堿中常含有少量的氯化鈉。某學習小組對其組成展開探究。現取24g純堿樣品,加入100g水使其完全溶解,再加入96g過量的氯化鈣溶液.完全反應后,過濾洗滌、干燥得沉淀20g。完成下列問題:
(1)反應后溶液中含有的溶質是_____________(寫 化學式);
(2)通過已知數據能求出的量有_____________( 寫字母序號);
A反應后溶液的總質量
B參加反應的氯化鈣的質量
C樣品中碳酸鈉的質量分數
D氯化鈣溶液中溶質的質量分數
(3)計算純堿樣品中氯化鈉的質量__________ (寫出計算過程)。.
查看答案和解析>>
科目: 來源: 題型:
【題目】(1)實驗室制取二氧化碳是中學化學的一個重要實驗,同學們在制出二氧化碳后又進行了相關的系列實驗,實驗裝置如圖:
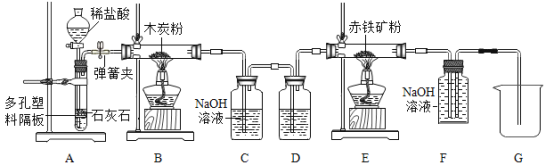
①B裝置中反應的化學方程式為_____________________。
②用A裝置制氣體的最大優點是___________________。
③C裝置的作用是__________________,D裝置的作用是___________________。
④E裝置中發生反應的實驗現象為___________________。
⑤F裝置除了吸收CO2外,還可以起到的作用是___________________。
(2)在化學實驗探究課上,化學老師交給某學習小組一包白色粉末,并提示該粉末由Na2SO4、NaNO2(亞硝酸鈉)、NaCl 中的一種或幾種組成。該小組同學們探究該白色粉末組成的實驗過程如下:
[查閱資料]1亞硝酸鹽能溶于水
2Na2SO4、NaNO2、NaCl的部分性質如表:
化學式 | 水溶液的酸堿性 | 與稀鹽酸作用 | 毒性 |
NaNO2 | 堿性 | 產生棕紅色氣體 | 有 |
NaCl | 中性 | 不反應 | 無 |
Na2SO4 | 中性 | 不反應 | 無 |
[實驗探究]
限用以下試劑:蒸餾水、酚酞試液、氯化鋇溶液、硝酸鋇溶液、硝酸銀溶液、稀鹽酸、稀硝酸
步驟 | 實驗操作 | 實驗現象 | 實驗結論 |
步驟一 | 取少量白色粉末加入試管中,加蒸餾水溶解,滴加____________。 | 無現象 | 白色粉末中不含有NaNO2 |
步驟二 | 另取少量白色粉末加入試管中,加蒸餾水溶解,______________。 | _____________ | 白色粉末中含有Na2SO4和NaCl |
步驟三 | _______________ | _____________ |
查看答案和解析>>
科目: 來源: 題型:
【題目】無水氯化鈣在工業上有廣泛的用途。以石灰石礦粉(含有SiO2、Fe2O3 、MgSO4等雜質)為原料,生產無水氯化鈣的流程如圖:
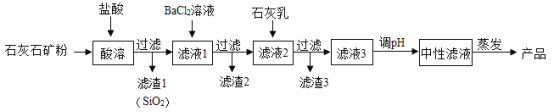
回答下列問題:
(1)從流程圖中推知:SiO2具有的化學性質是________________。
(2)加入鹽酸的主要作用是______________ ( 寫化學方程式);
(3)濾渣3中除有Ca(OH)2外、還有_______________。(填化學式);
(4)產品中的雜質除極少量H2O外,最可能含的是______________ (填化學式)。
查看答案和解析>>
科目: 來源: 題型:
【題目】“見著知微,見微知著”是化學思維方法,觀察下圖,回答問題。
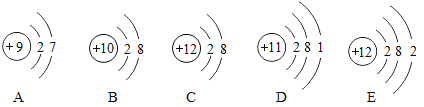
(1)微粒D次外層的電子數是__________________。
(2)屬于同種元素的微粒是_______________ (填符號);
(3)微粒A、B、C、D、E中,對應單質化學性質最穩定的是______________(填編號);
(4)微粒C位于第______________周期。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com