
科目: 來源: 題型:
【題目】雞蛋主要由蛋殼、蛋殼膜、蛋白、蛋黃等幾個部分組成,其中蛋殼的主要成分是CaCO3,里面覆蓋一層蛋殼膜。化學活動興趣小組的同學開展了以下探究活動:
【提出問題】蛋殼中的CaCO3含量是多少?

【查閱資料】
a、蛋殼經過科學檢測其中含CaCO3的質量分數約為82%~85%,含蛋白質質量分數約14-17%。
b、蛋殼膜中蛋白質含量約為90%~93%。
c、Ba(OH)2是一種堿,化學性質與Ca(OH)2相似。
【設計方案】
方案一:用“灼燒法”,將該蛋殼放在空氣中充分灼燒并采集相關數據進行測定。
方案二:用“酸處理法”,將蛋殼與稀鹽酸反應后再進行吸收轉變為碳酸鋇進行測量處理。
【進行實驗】
方案一:稱取12.0 g蛋殼研磨成粉末置于通風櫥中,灼燒至質量不再減少,再稱量剩余固體的質量為7.16 g。
方案二:用下圖所示的連接實驗裝置,稱取12 g蛋殼樣品進行實驗(假設其他成分均不與HCl反應,裝置內試劑均足量。)
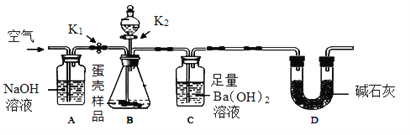
【實驗步驟】
① 按上圖連接好裝置后,并檢查裝置的氣密性;
② 向B裝置中加入蛋殼樣品后,先通入一會兒空氣;
③ 關閉K1,打開K2,向蛋殼樣品中滴入10%的鹽酸,直到__________為止;
④ 關閉K2,打開K1,再緩緩通入空氣一會兒,至裝置C中不再產生沉淀為止;
⑤ 將裝置C中的固液混合物進行過濾、__________、烘干后稱量其質量;
⑥ 重復上述實驗。
【數據處理】
方案一:產生的CO2質量__________g,蛋殼中的CaCO3的質量分數為__________%。(保留一位小數)
方案二:重復3次實驗,記錄數據如下:
實驗次數 | 第1次 | 第2次 | 第3次 |
裝置C中沉淀質量(/g) | 19.68 | 19.75 | 19.67 |
方案二:實驗測得蛋殼中的CaCO3的質量分數__________(寫出計算過程,)
(已知:Mr(CaCO3):100 Mr(BaCO3):197)
【評價反思】
(1)方案二中裝置D的作用是__________。
(2)方案一測定值與科學檢測的數據有較大誤差,主要原因是__________。
查看答案和解析>>
科目: 來源: 題型:
【題目】硫鐵礦燒渣(主要成份Fe2O3、Fe3O4、FeO、SiO2等,鐵的氧化物均能與鹽酸反應,SiO2不與酸反應)是工業生產硫酸的廢渣,利用硫鐵礦燒渣制備鐵紅(Fe2O3)等產品的部分流程如圖所示:

(1)焙燒時C與O2不完全燃燒產生的氣體都能將鐵的多種氧化物還原成鐵。試寫出該氣體與Fe3O4反應的化學方程式__________。
(2)酸浸、過濾后濾液中的溶質主要是__________。(填化學式)
(3)在空氣中煅燒FeCO3即FeCO3與空氣中的O2反應生成Fe2O3和CO2,試寫出該反應的化學反應方程式為:__________。
(4)若產品a的主要成分是K2SO4,得到產品a時加入的試劑X為__________。由此判斷在此條件下K2SO4的溶解度__________NH4Cl的溶解度(選填“<”或“>”或“=”)。
(5)可選用下列__________(填字母)洗滌產品a。
A.KCl飽和溶液 B.水 C.飽和K2SO4溶液.
查看答案和解析>>
科目: 來源: 題型:
【題目】實驗室有鹽酸、白醋和檸檬酸三種溶液,回答下列問題:
(1)向氧化鐵中放入足量鹽酸,振蕩,充分反應后,觀察到的現象是_________________,反應的化學方程式是________________________________________。
(2)白醋、檸檬酸溶液也能與氧化鐵發生類似反應,說明白醋、檸檬酸溶液和鹽酸中都含有的離子是__________。
(3)理論上溶解3.2g氧化鐵,需要36.5%鹽酸__________g。
查看答案和解析>>
科目: 來源: 題型:
【題目】請結合下圖回答問題:
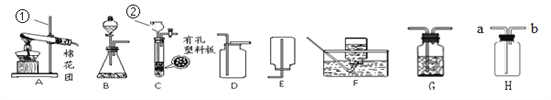
(1)寫出圖中有標號儀器的名稱:①__________,② __________。
(2)用加熱高錳酸鉀的方法制取氧氣,應選用的發生裝置是(填字母編號)__________,裝入藥品前應先__________,寫出該反應化學方程式__________。
(3)用B、D裝置組合制取二氧化碳氣體的化學方程式__________。 若要獲得干燥的該氣體,除發生、收集裝置外,還應選用G裝置,并在該裝置中盛放__________(填名稱)。如果用H裝置收集該氣體,則氣體從__________端進入(填“a”或“b”)。
(4)實驗室用鋅粒和稀硫酸反應制取H2的化學方程式__________,常選用裝置B或C, C與B相比較,C的優點是__________。
(5)實驗室使用的稀硫酸通常都是將濃硫酸用水稀釋而成的。現欲用98%的硫酸(密度為1.84g/mL)配置19.6%的稀硫酸100 g,需要濃硫酸的體積為__________mL(保留到小數點后一位),量取水時應選用規格(從10mL、50mL、100mL中選取)為__________mL的量筒。稀釋濃硫酸的操作為:__________,并用玻璃棒不斷攪拌。最后將稀硫酸轉移到試劑瓶中,貼上標簽備用,在標簽上可以不必注明的是__________(填字母序號)。
A.100 g B.19.6% C.稀硫酸
查看答案和解析>>
科目: 來源: 題型:
【題目】碲(Te)被譽為“現代工業、國防與尖端技術的維生素,創造人間奇跡的橋梁”。實驗室模擬提取碲的一個實驗是:取某含碲溶液于燒瓶中,加入適量NaCl,加熱到一定溫度,持續通入SO2,待反應一定時間,過濾得到粗碲。
(1)反應的總化學方程式為: ![]() ,則X為__________(填化學式)。
,則X為__________(填化學式)。
(2)為探究獲得較高粗碲沉淀率的反應條件,某研究小組在控制NaCl濃度和SO2流量不變的條件下,進行下述對比試驗,數據如下:
實驗 | 溫度/℃ | 反應時間/h | 粗碲沉淀率 |
a | 65 | 3.0 | 65.0 |
b | 80 | 3.0 | 98.9 |
c | 80 | 2.0 | 98.9 |
d | 90 | 2.0 | 97.0 |
①該小組研究的反應條件是____________________和____________________。
②實驗a和b的目的是__________________________________________________。
③在上述四組實驗中,最佳的反應條件是__________℃和__________h。
④為了提升設備利用效率和節約能源,可進一步優化反應條件測定粗碲沉淀率。若再設計對比實驗,選擇的反應條件還可以是__________(填選磺)。
A.80℃,1.5h B.80℃,2.5h C.70℃,2.0h D.95℃,2.0h
查看答案和解析>>
科目: 來源: 題型:
【題目】粗鹽中除NaCl外還含有泥沙等雜質。初步提純粗鹽的實驗流程如下:

(1)“濾渣”是粗鹽中含有的______________________________。
(2)實驗過程中多次用到玻璃棒,分別是:
第一次:____________________________________________________________;
第二次:____________________________________________________________;
第三次:蒸發結晶時不斷攪拌,防止液體和固體小顆粒飛濺;
第四次:將粗鹽從蒸發皿轉移出來。
(3)本實驗從濾液得到精鹽,采用的是蒸發溶劑的方法而不用降低溶液溫度的方法,參照所給溶解度曲線圖分析其原因是:__________________________________________________。

(4)看圖可知,20℃時NaCl的溶解度為__________g,本實驗溶解5.4g的粗鹽,蒸餾水的最佳使用量約為__________ml(水的密度為1g/mL)。
查看答案和解析>>
科目: 來源: 題型:
【題目】實驗室部分裝置如圖所示,請回答下列問題。
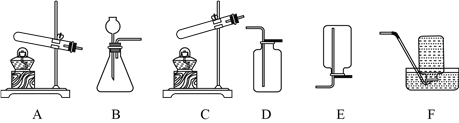
選用試劑 | 發生裝置 | 收集裝置 |
H2O2溶液、MnO2 | _____________ | ____________ |
KMnO4 |
(2)如果用MnO2與濃H2SO4加熱制備O2,可選用的發生裝置是__________(填字母)。
(3)選用F裝置收集氣體時,下列實驗操作正確的是__________(填序號)。
①反應前,將集氣瓶注滿水,用玻璃片蓋著瓶口,倒立在盛水的水槽中
②開始反應后,等到氣泡連續且均勻時,再將導管口移入集氣瓶
③收集氣體后,將集氣瓶蓋上玻璃片再移出水槽
(4)實驗室用KMnO4制備O2的化學方程式是______________________________。若需制備3.2g O2,至少需要消耗__________g KMnO4。(已知KMnO4的相對分子質量為158)
查看答案和解析>>
科目: 來源: 題型:
【題目】某同學做了以下兩個實驗:
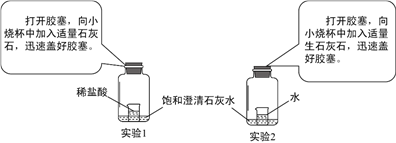
(1)實驗1中澄清石灰水的現象是________________________________________。產生此現象的原因是(用化學方程式表示)__________________________________________________。
(2)實驗2中澄清石灰水的現象是________________________________________。產生此現象的原因是(用文字表述)__________________________________________________。
查看答案和解析>>
科目: 來源: 題型:
【題目】2017年《科學報告》一篇文章稱,只需在普通口罩上添加氯化鈉涂層,就能將其轉化為“特效口罩”。口罩使用過程中,涂層中的氯化鈉會溶解于病毒自身攜帶的水中,形成溶液,殺死病毒;殺死病毒后,水分蒸發,氯化鈉再次析出。
(1)鈉原子轉化為鈉離子,其核外電子數__________(填“變大”或“變小”),常溫下,氯化鈉的飽和溶液中,氯化鈉與水的質量比為__________(已知:常溫下,氯化鈉的溶解度為36g)。
(2)構成氯化鈉的陽離子符號為__________,口罩使用過程中,氯化鈉溶液中溶質質量分數__________(填“改變”或“不變”)。
查看答案和解析>>
科目: 來源: 題型:
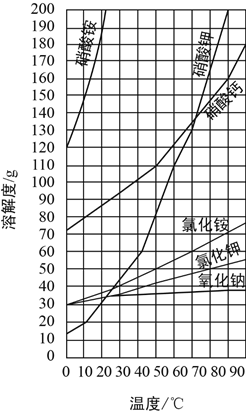
【題目】一些物質的溶解度同線如圖,回答下列問題:
(1)70℃時,在100g水中加入110g硝酸鉀固體,所形成的溶液是__________溶液(填“飽和”或“不飽和”)。
(2)將上述溶液降溫到10℃時,析出的晶體質量是__________g。
(3)工業上將硝酸鉀和氯化鈉的熱混合溶液(兩者均已達飽和)冷卻至室溫,析出晶體。
①析出的晶體含有的物質是____________________(填化學式)。
②關于剩余溶液,下列說法正確的是__________。
A.只含有氯化鈉,不含硝酸鉀,且氯化鈉達到飽和
B.含有氯化鈉,又含有硝酸鉀,且只有氯化鈉達到飽和
C.含有氯化鈉,又含有硝酸鉀,且兩者都達到飽和
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com