
分析 (1)根據二氧化錳是過氧化氫分解的催化劑,二氧化錳在化學反應前后質量不變進行分析;
(2)根據質量守恒定律計算生成氧氣的質量;
(3)根據生成氧氣的質量計算參加反應的過氧化氫的質量,然后計算過氧化氫的質量分數.
解答 解:(1)二氧化錳是過氧化氫分解的催化劑,二氧化錳在化學反應前后質量不變進,所以反應后二氧化錳的質量1g;
(2)生成氧氣的質量為:340g+1g-325g=16g;
(3)設參加反應的過氧化氫的質量為x
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
68 32
x 16g
$\frac{68}{x}$=$\frac{32}{16g}$
x=34g
所以過氧化氫溶液中溶質的質量分數是:$\frac{34g}{340g}$×100%=10%.
故答案為:(1)1g;
(2)16g;
(3)10%.
點評 掌握化學方程式的計算格式和規范性,學會使用質量守恒定律是解答本題的關鍵.


科目:初中化學 來源: 題型:實驗探究題
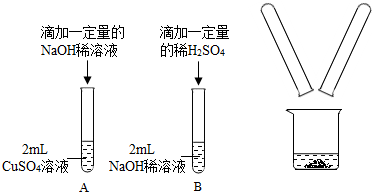
| 實驗步驟 | 預期的實驗現象 | 實驗結論 |
| 取少量濾液于試管中,滴入 無色酚酞試液 | 無色酚酞試液變紅色 | 小光的猜想正確 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題

查看答案和解析>>
科目:初中化學 來源: 題型:填空題
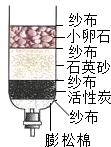 水資源的保護和合理利用已受到人們的普遍關注.請你討論下列有關問題.
水資源的保護和合理利用已受到人們的普遍關注.請你討論下列有關問題.查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | ①② | B. | ②③ | C. | ②③⑤ | D. | ③④⑤ |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
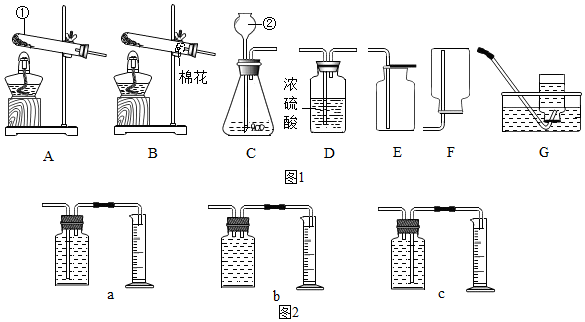
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com