
【題目】A-H是初中化學常見物質,如圖為這些物質的相互轉化關系圖,其中E為黑色固體,H為一種不溶于水的藍色固體,其中部分生成物與反應條件已省略。回答下列問題:

(1)F的化學式為_____;
(2)E→C化學方程式為_____;
(3)反應F+G→H的基本反應類型為_____;
(4)反應E→G在生產、生活中對應的一種用途_____。
【答案】NaOH CO+CuO![]() Cu+CO2 復分解反應 硫酸銅溶液可以殺菌消毒
Cu+CO2 復分解反應 硫酸銅溶液可以殺菌消毒
【解析】
本題屬于推斷題,根據題目給出的流程圖和信息:如圖為這些物質的相互轉化關系圖,已知碳酸鈣在高溫的條件下生成氧化鈣和二氧化碳,氧化鈣和水反應生成氫氧化鈣,氫氧化鈣和碳酸鈉反應生成碳酸鈣白色沉淀和氫氧化鈉,因此A是碳酸鈣,B是氧化鈣,C是二氧化碳,D是氫氧化鈣,F是氫氧化鈉;其中E為黑色固體,H為一種不溶于水的藍色固體,氧化銅和一氧化碳在加熱的條件下生成銅和二氧化碳,氧化銅和硫酸反應生成硫酸銅和水,硫酸銅和氫氧化鈉反應生成氫氧化銅藍色沉淀和硫酸鈉,因此E是氧化銅,G是硫酸銅,H是氫氧化銅。
(1)如圖為這些物質的相互轉化關系圖,已知碳酸鈣在高溫的條件下生成氧化鈣和二氧化碳,氧化鈣和水反應生成氫氧化鈣,氫氧化鈣和碳酸鈉反應生成碳酸鈣白色沉淀和氫氧化鈉,因此A是碳酸鈣,B是氧化鈣,C是二氧化碳,D是氫氧化鈣,F是氫氧化鈉;故答案為:NaOH;
(2)氧化銅和一氧化碳在加熱的條件下生成銅和二氧化碳,配平即可;故答案為:CO+CuO![]() Cu+CO2;
Cu+CO2;
(3)硫酸銅和氫氧化鈉反應生成氫氧化銅藍色沉淀和硫酸鈉,屬于復分解反應;故答案為:復分解反應;
(4)氧化銅和硫酸反應生成硫酸銅和水,硫酸銅溶液可以殺菌消毒,故答案為:硫酸銅溶液可以殺菌消毒。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:初中化學 來源: 題型:
【題目】實驗室常用于制取氧氣的方法有:a、加熱氯酸鉀晶體和二氧化錳粉末;b、加熱高錳酸鉀固體;c、用二氧化錳粉末作催化劑使過氧化氫溶液分解產生水和氧氣。
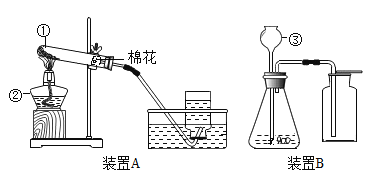
(1)寫出指定的儀器名稱:①_____②_____③_____。
(2)請仔細分析裝置A的特點,推測其所用的制氧氣的方法是_____(填a、b或c) 。
(3)采用方法c制取氧氣應該選用裝置_____(填“A”或“B”)。為檢驗裝置B中氧氣是否收集滿,可用帶火星的木條放在_____,這是利用了氧氣_____的性質。
(4)利用裝置A制氧氣,在結束實驗時要先撤離導管出水面,再熄滅酒精燈,其目的是_____;利用裝置B制氧氣時,儀器③的下端要插入液面以下,其目的是_____。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】結合下圖所示實驗,請回答下列問題.

實驗一的目的是利用濃氨水的堿性和揮發性,驗證了分子是______;
實驗二中,證明呼出的氣體比空氣中氧氣含量少的操作是向兩瓶中分別______;
實驗三中,通過測定鹽酸和碳酸鈉粉末反應前后的質量來驗證質量守恒定律,前后兩次稱量結果不一致,原因是沒有稱量______的質量.
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】已知,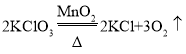 ,如圖表示一定質量的
,如圖表示一定質量的![]() 和
和![]() 固體混合物受熱過程中,某變量y隨時間的變化趨勢,縱坐標表示的是
固體混合物受熱過程中,某變量y隨時間的變化趨勢,縱坐標表示的是
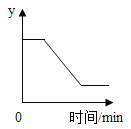
A. 固體中氧元素的質量B. 生成![]() 的質量
的質量
C. 固體中![]() 的質量D. 固體中鉀元素的質量分數
的質量D. 固體中鉀元素的質量分數
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】為測定空氣中氧氣的含量,小華同學打算設計如下圖所示的實驗方案:
在一個隔熱效果良好的容器上方安裝一個可自由上下移動的活塞(活塞質量忽略不計,起始位置在5刻度處)。加熱容器,使容器溫度達到80℃(已知白磷燃燒所需的最低溫度為40℃)。請回答:
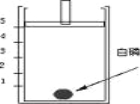
(1)實驗過程中,可以觀察到:白磷劇烈燃燒,產生大量白煙,活塞先向 __ 移動,再向 移動,最后停在刻度 處。
(2)發生反應的表達式為________ __。
(3)有位同學做此實驗時活塞最終停在4.5處,請你分析造成這一現象的原因是____________ 。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】用化學用語完成下列問題:
(1)硫酸根離子________;
(2)兩個氧原子_________;
(3)氦氣__________;
(4)五個二氧化碳分子_________;
(5)正二價的鈣元素________;
(6)2Fe2+中右上角的“2”表示_________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】能源與環境已成為人們日益關注的問題。
(1)目前人們利用最多的能源是煤、_______和天然氣等化石燃料。
(2)充分燃燒1000 g天然氣和煤所產生的CO2和SO2氣體的質量如下圖所示,根據圖示分析,下列說法正確的是_______。
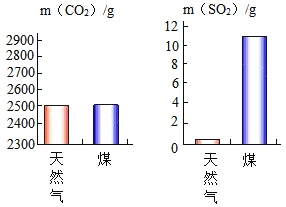
A 煤燃燒產生的氣體更易導致酸雨 B 該天然氣中不含硫元素
C 煤燃燒對環境影響較小 D 煤和天然氣的燃燒都有溫室氣體產生
(3)人們正在利用和開發其他能源,如太陽能、______、_________等。
(4)寫出天然氣燃燒的化學方程式_____________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】早在春秋戰國時期,我國就開始生產和使用鐵器。工業煉鐵把鐵礦石和焦炭、石灰石一起加入高爐,在高溫下,利用焦炭與氧氣反應生成的一氧化碳把鐵從鐵礦石里還原出來。
一氧化碳還原氧化鐵的化學方程式為: 。其中,石灰石起的作用是 。
(一)甲組同學在學習煉鐵的相關內容時,對煉鐵時還原劑的選擇進行了如下探究。
【提出問題】
單質碳也具有還原性,碳還原氧化鐵的化學方程式為 。為什么工業上不用焦炭作為還原劑直接還原鐵礦石?
【猜想與假設】
焦炭和鐵礦石都是固體,接觸面積小,反應不易完全。
【進行實驗】
①稱取兩份相同質量的氧化鐵粉末。一份與足量的碳粉均勻混合放入圖1裝置A的試管中;另一份放入圖1裝置B的玻璃管中。
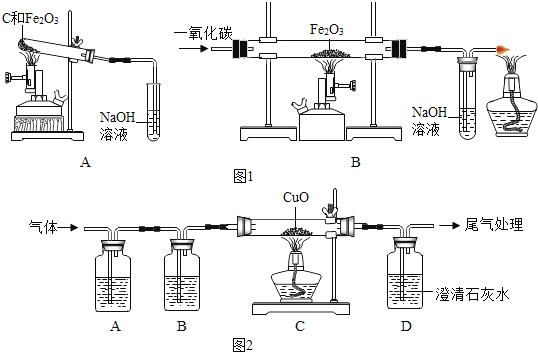
②圖1裝置A和B兩組實驗同時開始進行。在圖1裝置B的反應中,實驗開始前應先 (選填“通CO”或“加熱”); 實驗結束后應繼續通入CO直至冷卻至室溫,其原因是 。
【實驗現象】
當圖1裝置B的玻璃管中固體完全由 時(選填“紅色變為黑色”或“黑色變為紅色”),圖1裝置A的試管中仍有 。
【解釋與結論】
焦炭和鐵礦石都是固體,接觸面積小,反應確實不易完全,這可能是工業上不用焦炭作為還原劑直接還原鐵礦石的一個原因。
【完善實驗】
聯想到單質碳的一些化學性質,甲同學認為在碳還原氧化鐵的反應中可能還會有CO產生。為了證明碳還原氧化鐵所得的氣體中含有CO和CO2,將該氣體通過圖2的檢驗裝置。圖2A裝置中的試劑是(寫名稱,下同) ,圖2B裝置中的試劑是氫氧化鈉溶液,用以吸收二氧化碳(2NaOH+CO2═Na2CO3+H2O );證明原混合氣體中CO2存在的化學方程式 ;證明原混合氣體中CO存在的實驗現象是 ;經過檢驗,證實碳還原氧化鐵所得的氣體中確實含有CO和CO2。
(二)精還原鐵粉是一種重要的化工原料,某興趣小組對其進行下列研究:
【物質制備】
利用綠礬制備精還原鐵粉的工藝流程如下:
![]()
粗還原鐵粉中還含有少量鐵的氧化物和Fe3C雜質,可用氫氣在高溫下進一步還原,其反應方程式為
FexOy+yH2![]() xFe+yH2O,Fe3C+2H2
xFe+yH2O,Fe3C+2H2![]() 3Fe+CH4。
3Fe+CH4。
【含量測定】
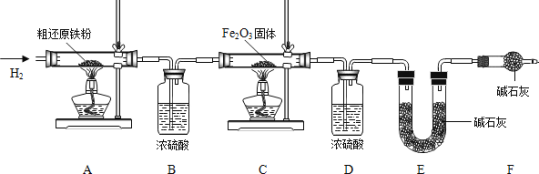
為得到精還原鐵粉并測定粗還原鐵粉中氧和碳元素的質量分數,按圖裝置進行實驗。
已知3CH4+4Fe2O3![]() 3CO2+6H2O+8Fe(假設每步反應都完全,且不考慮裝置內原有空氣對測定結果的影響)。
3CO2+6H2O+8Fe(假設每步反應都完全,且不考慮裝置內原有空氣對測定結果的影響)。
(1)主要實驗步驟如下:
①按順序組裝儀器,檢查裝置的氣密性,稱量樣品和必要裝置的質量;
②緩緩通入純凈干燥的H2;
③點燃酒精燈, (填“先點A處,后點C處”或“先點C處,后點A處”);
④分別熄滅A處、C處酒精燈;
⑤再緩緩通入少量H2;
⑥再次稱量必要裝置的質量
(2)步驟②的目的是 ,驗證該步驟目的達到的實驗方法是 ;
(3)若缺少裝置D,則所測氧元素的質量分數將 (填“偏大”,“偏小”或“不變”)。
(4)粗還原鐵粉樣品的質量為15.000g,裝置B、E分別增重0.270g和0.330g,則計算樣品出中碳、氧元素的質量分數分別是 。(列出計算過程,2分)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com