
【題目】貴陽某校探究小組對空氣中氧氣含量的測定進行了如下實驗探究。
將數顯設備、三種傳感器(氣體壓強、溫度、氧氣濃度)和其它裝置按圖1連接,裝置氣密性良好。實驗開始,打開并調試好傳感器和數顯設備,用酒精燈將足量紅磷點燃,立即將燃燒匙伸入瓶中并塞緊橡皮塞。各傳感器測得的數據如圖2所示,橫坐標為時間,縱坐標表示該段時間內氣體壓強、溫度、氧氣濃度對應的變化情況。

(1)寫出紅磷燃燒的化學方程式:_____。
(2)根據圖2中壓強變化曲線,bc段壓強升高的原因是_____。實驗結束打開活塞的過程中,壓強曲線中對應的線段是_____。
(3)圖2中X曲線表示的是_____(填“溫度”或“氧氣濃度”)變化情況。
(4)實驗結束測得裝置內氧氣濃度為8.85%后改用足量白磷實驗測得氧氣濃度為3.21%,而拉瓦錫采用汞作為消耗氧氣的反應物,結果發現實驗后氧氣的濃度幾乎為0%。
①若采用教材裝置測定空氣中氧氣含量時,改用白磷能使測定結果較準確的原因是_____。
②請從優缺點兩方面評價拉瓦錫測定空氣中氧氣的含量與課本采用的紅磷測定空氣中氧氣含量的方案
拉瓦錫實驗優點:_____、拉瓦錫實驗不足_____;
課本實驗優點:_____、課本實驗不足_____。
【答案】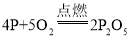 紅磷燃燒放熱,使裝置內氣體受熱膨脹,壓強變大 de 溫度 足量的白磷燃燒消耗的氧氣的更多 能將密閉裝置內空氣中的氧氣幾乎耗盡 汞蒸氣有毒,可能造成污染或傷害人體 產物為無毒固體五氧化二磷,實驗較為環保 不能將瓶內氧氣完全消耗
紅磷燃燒放熱,使裝置內氣體受熱膨脹,壓強變大 de 溫度 足量的白磷燃燒消耗的氧氣的更多 能將密閉裝置內空氣中的氧氣幾乎耗盡 汞蒸氣有毒,可能造成污染或傷害人體 產物為無毒固體五氧化二磷,實驗較為環保 不能將瓶內氧氣完全消耗
【解析】
(1)磷與氧氣在點燃的條件下反應生成五氧化二磷,反應的化學方程式為: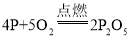 ;
;
(2)紅磷燃燒放熱,使裝置內氣體受熱膨脹,壓強變大,所以bc段壓強升高;由于紅磷燃燒消耗了氧氣造成裝置內的壓強減小,但實驗結束打開活塞的過程中,壓強又變大,恢復到反應前的壓強;故填:紅磷燃燒放熱,使裝置內氣體受熱膨脹,壓強變大;de;
(3)圖2中X曲線隨著反應的進行慢慢變大,反應結束后,又慢慢變小,最后恢復至反應前的水平,所以這條曲線表示的是溫度;若是氧氣的濃度就會越來越小;故填:溫度;
(4)①足量的白磷燃燒消耗的氧氣的更多,所以采用教材裝置測定空氣中氧氣含量時,改用白磷能使測定結果較準確;故填:足量的白磷燃燒消耗的氧氣的更多;
②拉瓦錫實驗優點:能將密閉裝置內空氣中的氧氣幾乎耗盡;
拉瓦錫實驗不足:汞蒸氣有毒,可能造成污染或傷害人體;
課本實驗優點:產物為無毒固體五氧化二磷,實驗較為環保;
課本實驗不足:不能將瓶內氧氣完全消耗。


科目:初中化學 來源: 題型:
【題目】在高效復習課堂中,同學們利用“鹽酸、硝酸鈣、氫氧化鈉、碳酸鈉”四種物質的溶液對“復分解反應發生的條件”進行再探究.
(知識回放)通過判斷上述四種溶液兩兩之間能否發生反應,若能寫出其中符合下列條件的兩個化學方程式:
①一個中和反應 _____________________;
②一個有沉淀生成的反應_________________。
(挖掘實質)
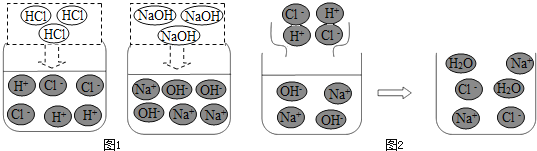
①圖1是HCl和NaOH在水中解離出離子的示意圖,小麗發現HCl在水中會解離出H+和 Cl-,NaOH在水中會解離出Na+和OH-,以此類推硝酸鋇在水中會解離出的離子是________(填離子符號)。
②圖2是稀鹽酸和氫氧化鈉溶液發生化學反應的微觀過程示意圖,該化學反應的實質可以表示為H++OH-= H2O,我也能用同樣的方式表示上述四種溶液兩兩之間發生反應時有氣體生成的反應的實質______________。
(實踐運用)
①通過上述探究發現,在溶液中H+和OH-不能大量共存,我還發現在溶液中______和_____(填離子符號)也不能大量共存。
②利用上述四種物質的溶液完成實驗后,將所得物質混合并過濾,得到一種無色溶液,經測定,該溶液顯酸性,則在該溶液中一定含有的離子是___________ 。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】某班化學興趣小組對催化劑的問題做了以下兩類探究,請你一起參與他們的探究年活動,并填寫下列空白:
(1)甲同學探究“催化劑的種類對氯酸鉀分解速率的影響”,設計了以下兩組對比實驗:
I將3.0g氯酸鉀和0.5g二氧化錳粉末均勻混合加熱;
II將3.0g氯酸鉀和Xg氧化銅粉末均勻混合加熱;
在相同條件下比較上述兩組實驗產生氧氣的快慢。寫出實驗I中發生反應的文字表達式________________;實驗Ⅱ中X的值應為_____________。
(2)乙同學探究“紅磚粉末是否也可以作為氧化氫分解的催化劑”
(提出問題)紅磚粉末能不能做氧化氫分解的催化劑呢?
(做出猜想)紅磚粉末能做氧化氫分解的催化劑
(實驗驗證)
實驗步驟 | 實驗現象 | 實驗結論 |
①將帶火星的木條伸入裝有過氧化氫溶液的試管中 | 木條不復燃 | 常溫下過氧化氫很難分解 |
②在上述試管中加入0.2g紅磚粉末,然后將帶火星的木條伸入試管中 | 木條復燃 | ________________________ |
③待上述試管反應停止時,重新加入過氧化氫溶液,并把帶火星的木條伸入試管 | 紅磚粉末的_______沒有改變 |
(實驗討論)有同學認為:僅憑上述實驗還不能證明紅磚粉末能做氧化氫分解的催化劑,還需要增加一個實驗“將實驗后剩余固體提純后稱量,如果所得固體的質量_____0.2g(選填“大于、小于或者等于”),則說明紅磚粉末可以作為氧化氫分解的催化劑”。
(實驗拓展)查閱資料得知:硫酸銅、豬肝、土豆等也可以做過氧化氫溶液分解的催化劑。下列有關催化劑的說法中正確的是______________。
A催化劑能增加生成物的量
B酶一種重要的生物催化劑,在工農業生產中起到極大的作用
C催化劑只能加快化學反應的速率
D同一個化學反應可以有多種催化劑
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】探究一: 某同學發現將帶火星的木條伸入氧氣含量約占40%的空氣樣品中就能復燃,那么能使帶火星的木條復燃的氧氣含量的最低值是多少呢?小亮同學設計了如下實驗進行探究:
第一組實驗:取5只集氣瓶,編號為①、②、③、④、⑤,分別裝入其總容積10%、20%、30%、40%、50%的水。用排水法收集氧氣,恰好把5只集氣瓶中的水排去。將帶火星的木條依次插入①~⑤號瓶中,記錄實驗現象。
小亮在前一組實驗的基礎上又做了第二組和第三組實驗,并進行了記錄。
第一組 | 第二組 | 第三組 | |||||||||
集氣瓶編號 | ① | ② | ③ | ④ | ⑤ | ① | ② | ③ | ④ | ⑤ | ① |
收集的氧氣占集氣瓶的體積分數 | 10 | 20 | 30 | 40 | 50 | 31 | 33 | 35 | 37 | 39 | 34 |
帶火星木條的狀況 | 微亮 | 亮 | 很亮 | 復燃 | 復燃 | 很亮 | 很亮 | 復燃 | 復燃 | 復燃 | 很亮 |
請回答下列問題:
(1)用帶火星的木條驗滿氧氣的方法是否說明氧氣肯定收集滿?________(填“是”或“否”)。
(2)寫出鐵在氧氣中燃燒的文字或符號表達式:____________________。
(3)采取“半值法”探究能減少實驗次數。例如:第一組實驗若按③、④的編號順序進行實驗,即可確定下一組實驗收集的氧氣占容積的體積分數應在30%~40%之間,從而省去編號①、②、⑤的實驗。同理,第二組實驗可以省去的實驗編號為______________。
(4)實驗數據收集的氧氣占集氣瓶容積的體積分數最低為35%時,可使帶火星的木條復燃,這時集氣瓶中氧氣體積分數約為___________%(計算結果保留整數)。
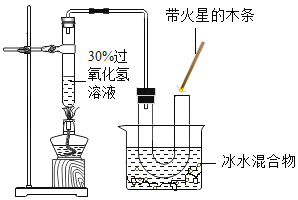
(5)用帶火星的木條直接檢驗雙氧水受熱分解產生的氧氣時,往往難以復燃,這是因為在加熱生成氧氣的同時產生大量水蒸汽所致,此時混合氣體中氧氣的體積分數隨溫度變化的曲線如圖所示.若只考慮氧氣的體積分數對實驗結果的影響,欲使帶火星的木條復燃,應將加熱雙氧水的最高溫度控制在大約_________℃。
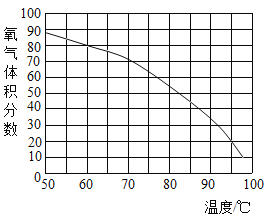
某同學改用如圖裝置后能使帶火星的木條復燃其原因是_________________。
探究二
(提出問題)過氧化氫溶液分解速率與哪些因素有關?
在常溫下,在相同質量、相同濃度的過氧化氫溶液中,分別加入1.5g二氧化錳和x g氧化銅,測量各生成一瓶(相同體積)氧氣所需的時間。實驗數據記錄如下:
實驗編號 | Ⅰ | Ⅱ |
反應物 | 5%過氧化氫溶液20mL | 5%過氧化氫溶液20mL |
催化劑 | 1.5 g 二氧化錳 | x g 氧化銅 |
時 間 | 46 s | 84 s |
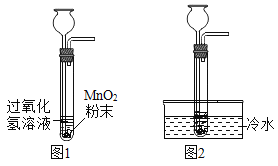
實驗Ⅱ中x的值應為___________。小張同學在上述實驗中發現用二氧化錳作催化劑制氧氣時(如圖1),發現反應放熱且過于劇烈,不易控制。后在老師的指導下,把發生裝置(如圖2)放在冷水中能獲得平穩的氣流。通過上述實驗,小張發現影響過氧化氫分解速率的因素有____________、 ___________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】為了測定能使帶火星的木條復燃時氧氣的最低含量是多少,課外活動小組的同學們將氧氣和空氣按不同的體積比收集在集氣瓶里。收集方法是:在100mL集氣瓶里裝滿水,塞緊膠塞并關閉活塞b,打開活塞a通入氧氣,把瓶里的水排入量筒,當量筒內的水達到設定的體積后立即關閉活塞a,然后打開活塞b通入空氣,把瓶里的水全部排入量筒。若要收集一瓶含氧氣的體積分數約為60%的氣體,則通入氧氣和空氣的體積約是( )

A. 20mL和80mLB. 40mL和60mL
C. 50mL和50mLD. 60mL和40mL
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】氣體的的制備是科學實驗基本技能之一。實驗室制取二氧化碳所需藥品是________和________,反應的文字表達式為______________。
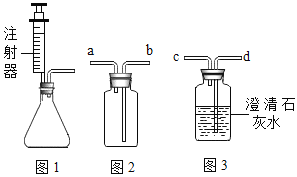
(1)若圖1裝置制取二氧化碳,其優點是______________。
(2)若圖2裝置收集二氧化碳,應將氣體發生裝置的導管與圖2裝置的導管_______(選填“a”或“b”)相連接。檢驗該裝置中二氧化碳已收集滿的操作是_______________。
(3)若用圖3裝置檢驗二氧化碳,應將氣體發生裝置的導管與圖3裝置的導管_________ (選填“c”或“d”)相連接。寫出用澄清石灰水檢驗二氧化碳的文字表達式_______。
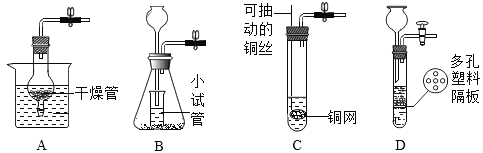
(4)下列二氧化碳的制備裝置中,不能起到“能控制反應發生和停止”效果的是________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】如圖中的①、②分別是鈉元素、;氯元素在元素周期表中的信息,A、B、C是三種粒子的結構示意圖.
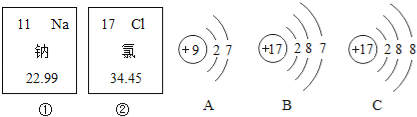
試回答下列問題:
(1)鈉元素的原子序數為 ,畫出它的原子結構示意圖 ;
(2)A、B、C中屬于同種元素的粒子是 ;
(3)A和B兩種粒子的相同,所以它們具有相似的化學性質 ;
(4)鈉原子和氯原子反應所形成的化合物是由 (填“分子”、“原子”、“離子”)構成的.
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】維生素C(C6H8O6)主要存在于蔬菜、水果中,它能促進人體生長發育,增強人體對疾病的抵抗力。下列關于維生素C的說法中不正確的是
A. 維生素C中C、H、O三種元素的質量比為9:1:12
B. 1個維生素C分子由6個碳原子、8個氫原子、6個氧原子構成
C. 維生素C的相對分子質量為174
D. 維生素C中氫元素的質量分數為4.5%
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】實驗室現有氯酸鉀、二氧化錳、石灰石、蠟燭、火柴及以下儀器(如圖),請回答:
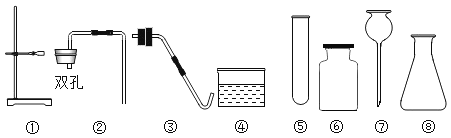
(1)儀器⑦的名稱是____________;
(2)若補充一種常見儀器,并利用上述部分儀器和藥品可制取一種氣體,該反應的化學方程式是_______________。
(3)若補充一種藥品,還能制取二氧化碳,并探究其性質(如圖)
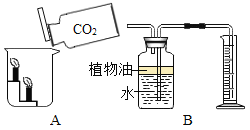
①補充的藥品是_________________;
②圖A觀察到的現象說明二氧化碳具有的化學性質是______________;B中可用來測量生成二氧化碳氣體的體積,其中在水面上放一層植物油的原因是______。
(4)2018年4月28日某媒體題為“排污工程施工,毒氣放倒三人”的報道,引起某興趣小組同學的思考。
(提出問題)排污管道中的毒氣有什么成分?
(查閱資料)
I.排污管道中的大部分有機物在一定條件下發酵會產生CO、CO2、H2S、CH4等。
II.H2S氣體能與CuSO4溶液反應生成黑色沉淀。
(提出猜想)小組同學對排污管道氣含有上述氣體中最少3種成分的猜想如下:
猜想1:有CO、CO2、H2S; 猜想2:有CO、CO2、CH4;
猜想3:有CO、H2S、CH4; 猜想4:有CO、CO2、H2S、CH4。
(實驗方案)小組同學共同設計了如圖所示的裝置并進行探究(夾持儀器已省略)。
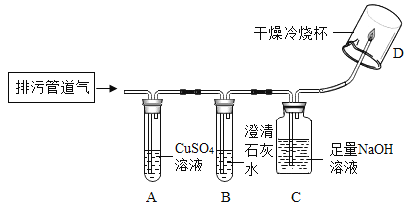
(問題討論)
①如果A裝置沒有明顯變化,則猜想__________成立;如果B裝置沒有明顯變化,則猜想_________成立。
②要確證猜想4中是否有CH4,某同學認為圖示裝置有不足之處,需要在裝置C與D之間加一個____________裝置。改進后,若氣體燃燒,且D裝置內壁出現__________,證明氣體中一定含有CH4。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com