
| 實驗步驟 | 實驗操作 | 預期現象及結論 |
| 1 | 取少量所得溶液于試管中,滴入過量的稀鹽酸 | 證明原溶液中不含有Na2CO3 |
| 2 | 另取少量所得溶液于試管中,滴入碳酸鈉溶液 | 沒有沉淀生成,證明原溶液中不含有氫氧化鈣結合步驟1,猜想一成立 |
分析 (1)根據碳酸鈉與氫氧化鈣反應的生成物分析;
(2)根據反應的量分析反應后溶液的成分;
(3)根據碳酸鈉能與稀鹽酸、氫氧化鈣反應分析判斷.
解答 解:(1)碳酸鈉和氫氧化鈣反應生成了碳酸鈣沉淀和氫氧化鈉,能發生復分解反應的理由是:有沉淀生成,符合復分解反應的條件.
(2)碳酸鈉和氫氧化鈣發生反應生成了碳酸鈣沉淀和氫氧化鈉,當碳酸鈉和氫氧化鈣恰好反應時,溶液中只含有含NaOH;當碳酸鈉過量時,溶液中NaOH和Na2C03;當氫氧化鈣過量是時,溶液中含有NaOH和Ca(OH)2,所以猜想三是:NaOH和Ca(OH)2.
(3)由碳酸鈉能與鹽酸反應生成了二氧化碳氣體,能與氫氧化鈣反應生成碳酸鈣沉淀,所以實驗的操作和現象見下表:
| 實驗步驟 | 實驗操作 | 預期現象及結論 |
| 1 | 取少量所得溶液于試管中,滴入過量的稀鹽酸 | 沒有氣泡放出證明原溶液中不含有Na2C03 |
| 2 | 另取少量所得溶液于試管中,滴入碳酸鈉溶液 | 沒有沉淀生成,證明原溶液中不含有氫氧化鈣,結合步驟1,猜想一成立 |
| 實驗步驟 | 實驗操作 | 預期現象及結論 |
| 1 | 滴入過量的稀鹽酸 | |
| 2 | 滴入碳酸鈉溶液 | 沒有沉淀生成,證明原溶液中不含有氫氧化鈣 |
點評 本題主要考查了復分解反應的條件、碳酸鈉的性質,難度不大;在分析化學反應后所得物質的成分時,除了考慮生成物外還需考慮反應物是否有剩余.


 孟建平小學滾動測試系列答案
孟建平小學滾動測試系列答案科目:初中化學 來源: 題型:選擇題
 如圖為甲、乙兩種物質的溶解度曲線.下列說法正確的是( )
如圖為甲、乙兩種物質的溶解度曲線.下列說法正確的是( )| A. | 40℃時,100g乙的飽和溶液中含有60g乙 | |
| B. | 甲中混有少量乙,可采用降溫結晶提純 | |
| C. | 20℃時,甲、乙兩種物質的溶解度相同 | |
| D. | 同溫時,飽和溶液的溶質質量分數:乙>甲 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | +3 | B. | +2 | C. | -2 | D. | +5 |
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
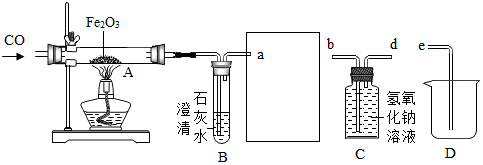
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
| 序號 | 化學方程式 | 屬于的基本反應類型 |
| ① | Fe+S $\frac{\underline{\;\;△\;\;}}{\;}$ FeS | 化合反應 |
| ② | Cu(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CuO+H2O | 分解反應 |
| ③ | H2+CuO $\frac{\underline{\;\;△\;\;}}{\;}$ Cu+H2O | 置換反應 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| 物質 | a | b | c | d |
| 反應前的質量/g | 20 | 20 | 0 | 0 |
| 反應一段時間后的質量/g | 12 | 4 | 6 | ① |
| 反應后的質量/g | ② | 0 | ③ | ④ |
| A. | ④為22.5g | B. | ②為8g | C. | ③為12g | D. | ①為22g |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 3Fe+2O2═Fe3O4(分解反應) | |
| B. | 2Zn+3H2SO4═Zn2(SO4)3+3H2↑ (置換反應) | |
| C. | Cu(OH)2+2HCl═CuCl2+2H2O (復分解反應) | |
| D. | H2CO3═H2O+CO2↑ (化合反應) |
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 銀水銀Ag | B. | 碳酸鈉純堿Na2CO3 | ||
| C. | 氧化鈣生石灰CaO | D. | 氫氧化鈉苛性鈉NaOH |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com