
ĪŠŅ}─┐Ī┐─│┼d╚żąĪĮM═¼īWī”īŹ“×╩ęųŲč§ÜŌĄ─Śl╝■▀Mąą╚ńŽ┬╠ĮŠ┐Ż║
Ż©aŻ®×ķ╠ĮŠ┐┤▀╗»ä®Ą─ĘNŅÉī”┬╚╦ßŌøĘųĮŌ╦┘┬╩Ą─ė░ĒæŻ¼╝ūįOėŗęįŽ┬ī”▒╚īŹ“ׯ║
ó┘īó3.0g┬╚╦ßŌø║═1.0gČ■č§╗»ÕiŠ∙ä“╗ņ║Ž╝ė¤ßŻ╗
ó┌īóxg┬╚╦ßŌø║═1.0gč§╗»Ń~Š∙ä“╗ņ║Ž╝ė¤ßĪŻ
į┌ŽÓ═¼£žČ╚Ž┬Ż¼▒╚▌^ā╔ĮMīŹ“׫a╔·č§ÜŌĄ─┐ņ┬²ĪŻ
ó┘ųąĘ┤æ¬Ą─╗»īWĘĮ│╠╩Į╩Ū__________________________Ż╗ó┌ųąxĄ─ųĄæ¬×ķ_____ĪŻ
Ż©▓┬ŽļŻ®│²Č■č§╗»ÕiŻ¼č§╗»Ń~═ŌŻ¼Fe2O3ę▓┐╔ęįū÷┬╚╦ßŌøĘųĮŌĄ─┤▀╗»ä®ĪŻ
░┤Ž┬▒Ē▀MąąīŹ“ׯ║£yČ©ĘųĮŌ£žČ╚Ż©ĘųĮŌ£žČ╚įĮĄ═Ż¼┤▀╗»ą¦╣¹įĮ║├Ż®
īŹ“׊Ä╠¢ | īŹ“×╦ÄŲĘ | ĘųĮŌ£žČ╚/Īµ |
ó┘ | ┬╚╦ßŌø | 580 |
ó┌ | ┬╚╦ßŌøĪóČ■č§╗»ÕiŻ©┘|┴┐▒╚1Ī├1Ż® | 350 |
ó█ | ┬╚╦ßŌøĪóč§╗»Ń~Ż©┘|┴┐▒╚1Ī├1Ż® | 370 |
ó▄ | ┬╚╦ßŌøĪóFe2O3Ż©┘|┴┐▒╚1Ī├1Ż® | 390 |
ė╔īŹ“×________┼cīŹ“×ó▄ī”▒╚Ż¼ūC├„▓┬Žļ║Ž└ĒĪŻīŹ“×╦∙ė├Ą─╚²ĘNĮī┘č§╗»╬’Ż¼┤▀╗»ą¦╣¹ūŅ║├Ą─╩Ū___ĪŻ
Ż©bŻ®ęę╠ĮŠ┐┴╦ė░Ēæ▀^č§╗»Üõ╚▄ę║ĘųĮŌ╦┘┬╩Ą──│ĘNę“╦žĪŻīŹ“×ėøõø╚ńŽ┬Ż║
▀^č§╗»Üõ╚▄ę║Ą─┘|┴┐ | ▀^č§╗»ÜõĄ─ØŌČ╚ | Č■č§╗»ÕiĄ─┘|┴┐ | ŽÓ═¼Ģrķgā╚«a╔·VO2 | |
ó┘ | 50.0g | 1% | 0.1g | 9mL |
ó┌ | 50.0g | 2% | 0.1g | 16mL |
ó█ | 50.0g | 4% | 0.1g | 31mL |
īŹ“×ĮYšōŻ║į┌ŽÓ═¼Śl╝■Ž┬Ż¼_______________________________Ż¼▀^č§╗»ÜõĘųĮŌĄ├įĮ┐ņĪŻ▒ŠīŹ“×ųą£y┴┐O2¾wĘeĄ─čbų├Ż©╚ńłDŻ®æ¬įō▀xō±Ż║_______ĪŻŻ©╠Ņūų─ĖŻ®
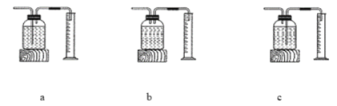
ĪŠ┤░ĖĪ┐2KClO3![]() 2KCl + 3O2Ī³ 3.0 ó┘ Č■č§╗»Õi ▀^č§╗»ÜõĄ─ØŌČ╚įĮ┤¾Ż¼ĘųĮŌ╦┘┬╩įĮ┐ņ c
2KCl + 3O2Ī³ 3.0 ó┘ Č■č§╗»Õi ▀^č§╗»ÜõĄ─ØŌČ╚įĮ┤¾Ż¼ĘųĮŌ╦┘┬╩įĮ┐ņ c
ĪŠĮŌ╬÷Ī┐
Ż©1Ż®┬╚╦ßŌøį┌Č■č§╗»Õiū„┤▀╗»ä®Ą─Śl╝■Ž┬╝ė¤ßĘ┤æ¬╔·│╔┬╚╗»Ōø║═č§ÜŌŻ¼Ę┤æ¬Ą─╗»īWĘĮ│╠╩Į×ķŻ║2KClO3![]() 2KCl + 3O2Ī³ĪŻ
2KCl + 3O2Ī³ĪŻ
Ż©2Ż®Ė∙ō■╠ĮŠ┐┤▀╗»ä®Ą─ĘNŅÉī”┬╚╦ßŌøĘųĮŌ╦┘┬╩Ą─ė░Ēææ¬įō┐žųŲŲõ╦³Śl╝■ŽÓ═¼Ż¼Č°┤▀╗»ä®Ą─ĘNŅÉ▓╗═¼Ż¼╦∙ęįó┌ųąxĄ─ųĄæ¬×ķ3.0ĪŻė╔īŹ“×ó┘┼cīŹ“×ó▄ī”▒╚┐╔ų¬Ż¼Fe2O3ę▓┐╔ęįū÷┬╚╦ßŌøĘųĮŌĄ─┤▀╗»ä®ĪŻīŹ“×╦∙ė├Ą─╚²ĘNĮī┘č§╗»╬’Ż¼┤▀╗»ą¦╣¹ūŅ║├Ą─╩ŪČ■č§╗»ÕiĪŻ
Ż©3Ż®ė╔īŹ“×öĄō■┐╔ų¬Ż¼į┌ŽÓ═¼Ą─Śl╝■Ž┬Ż¼▀^č§╗»ÜõĄ─ØŌČ╚įĮ┤¾Ż¼ĘųĮŌ╦┘┬╩įĮ┐ņĪŻ▒ŠīŹ“×čbų├▒žĒÜ▒ŻūC┼┼│÷╦«Ą─ī¦╣▄æ¬ĮėĮ³╝»ÜŌŲ┐Ą─Ąū▓┐Ż¼ė╔ė┌č§ÜŌĄ─├▄Č╚▒╚╦«Ą─├▄Č╚ąĪŻ¼╣╩č§ÜŌæ¬įōėąČ╠╣▄═©╚ļŻ¼╣╩▀xcĪŻ


 ▒Č╦┘ė¢ŠÜĘ©ų▒═©ųą┐╝┐╝³cŽĄ┴ą┤░Ė
▒Č╦┘ė¢ŠÜĘ©ų▒═©ųą┐╝┐╝³cŽĄ┴ą┤░Ė ę╗ŠĒĖŃČ©ŽĄ┴ą┤░Ė
ę╗ŠĒĖŃČ©ŽĄ┴ą┤░Ė ├¹ąŻū„śI▒ŠŽĄ┴ą┤░Ė
├¹ąŻū„śI▒ŠŽĄ┴ą┤░Ė ▌pŪ╔ŖZ╣┌ų▄£yį┬┐╝ų▒═©├¹ąŻŽĄ┴ą┤░Ė
▌pŪ╔ŖZ╣┌ų▄£yį┬┐╝ų▒═©├¹ąŻŽĄ┴ą┤░Ė
| ─Ļ╝ē | Ė▀ųąšn│╠ | ─Ļ╝ē | │§ųąšn│╠ |
| Ė▀ę╗ | Ė▀ę╗├Ō┘Mšn│╠═Ų╦]ŻĪ | │§ę╗ | │§ę╗├Ō┘Mšn│╠═Ų╦]ŻĪ |
| Ė▀Č■ | Ė▀Č■├Ō┘Mšn│╠═Ų╦]ŻĪ | │§Č■ | │§Č■├Ō┘Mšn│╠═Ų╦]ŻĪ |
| Ė▀╚² | Ė▀╚²├Ō┘Mšn│╠═Ų╦]ŻĪ | │§╚² | │§╚²├Ō┘Mšn│╠═Ų╦]ŻĪ |
┐Ų─┐Ż║│§ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐╝ūłD╩Ūę╗č§╗»╠╝▀ĆįŁč§╗»ĶFĄ─čbų├,ęęłD╩Ū¤ÆĶFĖ▀Āt╩ŠęŌłD,Ž┬┴ąöó╩÷ųąš²┤_Ą─╩Ū
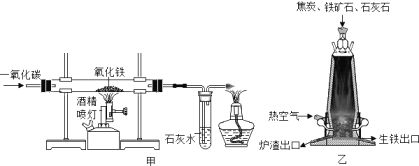
A. ╝ūłDųąīŹ“×ķ_╩╝Ģr欎╚³c╚╝╝ė¤ßč§╗»ĶFĄ─ŠŲŠ½ćK×┐,į┘³c╚╝ŠŲŠ½¤¶
B. ęęłD¤ÆĶFųąįŁ┴ŽĮ╣╠┐Ą─ū„ė├ų╗╩Ū╠ß╣®¤ß┴┐
C. ¤ÆĶFĄ─ų„ę¬įŁ└Ē╩Ū: Fe2O3+3CO ![]() 2Fe+3CO2
2Fe+3CO2
D. łDųąę╗č§╗»╠╝ģó┼cĄ─╗»īWĘ┤權∙¾w¼F┴╦![]() Ą─▀ĆįŁąį
Ą─▀ĆįŁąį
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║│§ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐Ž┬łD╩Ū─│╗»īWĘ┤æ¬Ą─╬óė^─ŻöM╩ŠęŌłDŻ¼├┐éĆąĪŪ“┤·▒Ēę╗ĘNį¬╦žĄ─įŁūėĪŻŽ┬┴ąšfĘ©š²┤_Ą─╩Ū
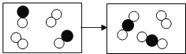
A. įōĘ┤æ¬Ū░║¾į¬╦žĄ─ĘNŅÉ░l╔·┴╦Ė─ūā
B. ╗»īWĘ┤æ¬ųąŻ¼Ę┤æ¬╬’Īó╔·│╔╬’Ą─╬ó┴ŻéĆöĄ▒╚×ķ2Ż║2Ż║2Ż║1
C. įōłD╩Ššf├„╗»īWūā╗»ųąĘųūėĪóįŁūėČ╝┐╔Ęų
D. įōĘ┤æ¬╩Ūę╗éĆ╗»║ŽĘ┤æ¬
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║│§ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐īŹ“×╩ęėąę╗Ų┐┼õųŲöĄ╠ņĄ─Na2SO3╚▄ę║Ż¼¼Fį┌ī”Ųõ│╔Ęų▀MąąÖz£yŻ║
Ż©│╔Ęų▓┬ŽļŻ®▓┬Žļę╗Ż║ų╗ėąNa2SO3Ż╗
▓┬ŽļČ■Ż║_____Ż╗
▓┬Žļ╚²Ż║╝╚ėąNa2SO3Ż¼ę▓ėąNa2SO4ĪŻ
Ż©▓ķķå┘Y┴ŽŻ®ó┘Na2SO3ęū▒╗┐šÜŌųąĄ─č§ÜŌč§╗»╔·│╔Na2SO4Ż«ó┌BaSO4▓╗╚▄ė┌ŽĪ¹}╦ß║═ŽĪ┴“╦ßĪŻó█Na2SO3║═¹}╦ßĪó┴“╦ßĘ┤權∙╔·│╔SO2ĪŻ
Ż©ĘĮ░ĖįOėŗŻ®
ĘĮ░Ė | īŹ“×▓┘ū„ | īŹ“×¼FŽ¾ | ĮYšō |
ę╗ |
ó┘╝ė╚ļūŃ┴┐Ą─ŽĪ¹}╦ß ó┌į┘╝ė╚ļūŃ┴┐Ą─BaCl2╚▄ę║ | _____ | ▓┬Žļ╚²š²┤_ |
Č■ | ó┘╝ė╚ļūŃ ó┌į┘╝ė╚ļūŃ┴┐Ą─BaCl2╚▄ę║ | ėąÜŌ¾w║═░ū╔½│┴ĄĒ╔·│╔ | ▓┬Žļę╗╗“▓┬Žļ╚²š²┤_ |
Ż©ĘĮ░ĖĘų╬÷Ż®
Ż©1Ż®ĘĮ░Ėę╗ųąĄ─īŹ“×¼FŽ¾×ķ_____Ż╗ĘĮ░Ėę╗ųą╝ė╚ļBaCl2╚▄ę║║¾░l╔·Ę┤æ¬Ą─╗»īWĘĮ│╠╩Į×ķ_____ĪŻ
Ż©2Ż®ĘĮ░ĖČ■Ą─įOėŗ╩Ūʱ║Ž└ĒŻ║_____Ż©╠ŅĪ░║Ž└ĒĪ▒╗“Ī░▓╗║Ž└ĒĪ▒Ż®Ż╗╚¶▓╗║Ž└ĒĪŻ└Ēė╔╩Ū_____ĪŻ
Ż©īŹ“×ĮYšōŻ®═©▀^Ęų╬÷▒╚▌^Ż¼ĘĮ░ĖįOėŗ_____Ż©╠ŅĪ░ę╗Ī▒╗“Ī░Č■Ī▒Ż®║Ž└ĒĪŻ
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║│§ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐╚Ī┬╚╦ßŌø║═Č■č§╗»ÕiĄ─╗ņ║Ž╬’12┐╦ųŲ╚Īč§ÜŌŻ¼╝ė¤ßę╗Č╬Ģrķg║¾Ż¼£yĄ├50ŻźĄ─┬╚╦ßŌøĘųĮŌŻ¼īó╩ŻėÓĄ─╣╠¾w└õģs║¾ĘQ┴┐Ż¼Ųõ┘|┴┐×ķ10Ż«08┐╦Ż¼Ū¾įŁ╗ņ║Ž╬’ųą┬╚╦ßŌø║═Č■č§╗»ÕiĖ„ČÓ╔┘┐╦Ż┐
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║│§ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐īŹ“×äōą┬╩ŪųąīW╔·ūŅ×ķųžę¬Ą─┐ŲīW╦žBŻ¼ęįŽ┬╩Ū╗»īW┼d╚żąĪĮMĄ─═¼īWį┌īW┴ĢĪ░Č■č§╗»Õi┤▀╗»▀^č§╗»ÜõĘųĮŌųŲč§ÜŌīŹ“×Ī▒║¾Ż¼ī”īŹ“ץ─äōą┬įOėŗĪŻ
īŹ“×ę╗Ż║įOėŗą┬Ą─īŹ“×čbų├
īŹ“×▀^│╠╚ńŽ┬Ż║
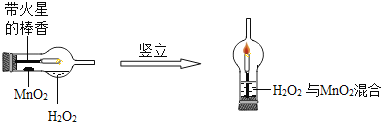
ó┘īóę╗ų¦Ū“ą╬Ė╔į’╣▄╦«ŲĮĘ┼ų├Ż¼ė├Ą╬╣▄╬³╚Ī3mL(├▄Č╚×ķ1g/mL)┘|┴┐ĘųöĄ×ķ5%Ą─H2O2╝ė╚ļĖ╔į’╣▄Ą─Ū“┼▌ųąŻ¼į┘ė├╦Ä│ū╚Ī0.2gMnO2Ę█─®Ż¼╝ėį┌Ė╔į’Ą─▀MÜŌ╣▄Ą─╣▄▒┌╔ŽŻ╗ó┌³c╚╝Ž─z╚¹╔Ž╣╠Č©Ą─░¶ŽŃ║¾Ż¼╚¹ŠoĖ╔į’╣▄▓óīóŲõžQ┴óŻ¼ė^▓ņ¼FŽ¾Ż╗
Ż©1Ż®┐╔ė^▓ņĄĮĦ╗ąŪĄ─░¶ŽŃ┴ó╝┤___Ż╗
Ż©2Ż®Ž┬┴ąĖ„ĒŚ╩Ū═¼īWéāī”įōäōą┬īŹ“ץ─įuārŻ¼─ŃšJ×ķįuār▓╗║Ž└ĒĄ─╩Ū___(╠Ņą“╠¢)
A. īŹ“×╦∙ė├Ą─āxŲ„Īó▓─┴Ž╝░╦ÄŲĘŠ∙ęūĄ├ĄĮ
B. īŹ“×╩ęė├Ą─╦ÄŲĘė├┴┐╠½┤¾
C. Ę┤æ¬╦┘Č╚╠½┬²Ż¼Ąóš`Ģrķg
D. īŹ“×¼FŽ¾├„’@Ż¼š¹éĆčbų├║├╦Ų³c╚╝Ą─¤¶╦■Ż¼╚ż╬ČąįÅŖ
īŹ“×Č■Ż║īżšęą┬Ą─┤▀╗»ä®
Ż©īŹ“×╠ĮŠ┐Ż®
īŹ“×▓Į¾E | īŹ“×¼FŽ¾ |
IĪóĘųäe┴┐╚Ī5mL5%▀^č§╗»Üõ╚▄ę║Ę┼╚ļA.Bā╔ų¦įć╣▄ųąŻ¼Ž“Aįć╣▄ųą╝ė╚ļagč§╗»ĶFĘ█─®Ż¼▓óĘųäeį┌A.Bā╔ų¦įć╣▄ųą▓Õ╚ļĦ╗ąŪĄ──ŠŚlŻ¼ė^▓ņ¼FŽ¾ĪŻ | Aįć╣▄ųą«a╔·ÜŌ┼▌Ż¼Ä¦╗ąŪ─ŠŚlÅ═╚╝.Bįć╣▄ųą¤o├„’@¼FŽ¾ĪŻ |
ó“Īó┤²Aįć╣▄ųąø]ėą¼FŽ¾░l╔·ĢrŻ¼ųžą┬╝ė╚ļ▀^č§╗»Üõ╚▄ę║Ż¼▓ó░čĦ╗ąŪĄ──ŠŚl╔ņ╚ļįć╣▄Ż¼╚ń┤╦Ę┤Å═ČÓ┤╬įć“ׯ¼ė^▓ņ¼FŽ¾ĪŻ | įć╣▄ųąŠ∙«a╔·ÜŌ┼▌Ż¼Ä¦╗ąŪ─ŠŚlŠ∙Å═╚╝ĪŻ |
ó¾Īóīóįć“×IIųąĄ─╩ŻėÓ╬’ąĪą─▀^×VŻ¼▓óīó╦∙Ą├×Vį³▀MąąŽ┤£ņĪóĖ╔į’Ż¼ĘQ┴┐ĪŻ | ╦∙Ą─╣╠¾w┘|┴┐×ķ___ |
IVĪóĘųäe┴┐╚Ī5ml5%▀^č§╗»Üõ╚▄ę║Ę┼╚ļC.Dā╔ų¦įć╣▄ųąŻ¼Ž“Cįć╣▄ųą╝ė╚ļagč§╗»ĶFĘ█─®Ż¼Ž“Dįć╣▄ųą╝ė╚ļagČ■č§╗»ÕiĘ█─®Ż¼ė^▓ņ¼FŽ¾ĪŻ |
Ż©īŹ“×ĮYšōŻ®
Ż©1Ż®Aųą«a╔·Ą─ÜŌ¾w╩Ū___Ż╗
Ż©2Ż®īŹ“×ó“Īóó¾┐╔ęįūC├„Ż║___Ż¼į┘ĮY║ŽīŹ“×I║═ó¾Ą─ĮYšō┐╔ęįūC├„č§╗»ĶF┐╔ęįū„×ķ▀^č§╗»ÜõĘųĮŌĄ─┤▀╗»ä®ĪŻ
Ż©3Ż®īæ│÷č§╗»ĶF(Fe2O3)┤▀╗»▀^č§╗»ÜõĘųĮŌĄ─╗»īWĘĮ│╠╩ĮŻ║___________________Ż╗
Ż©īŹ“×įuārŻ®
Ż©1Ż®įOėŗīŹ“×IVĄ──┐Ą─╩Ū___Ż╗
Ż©2Ż®╚¶īŹ“×IVė^▓ņĄĮDįć╣▄ųą«a╔·ÜŌ┼▌Ą─╦┘┬╩Ė³┐ņŻ¼ė╔┤╦─Ń┐╔ęįĄ├ĄĮĄ─ĮYšō╩Ū___.
Ż©īŹ“×═žš╣Ż®
▓ķķå┘Y┴ŽĄ├ų¬Ż║CuOĪóCuSO4ĪóžiĖ╬Īó±RŌÅ╩ĒĄ╚ę▓┐╔ū÷▀^č§╗»Üõ╚▄ę║ĘųĮŌĄ─┤▀╗»ä®Ż¼Ž┬┴ąėąĻP┤▀╗»ä®Ą─šfĘ©š²┤_Ą─╩Ū___
A.MnO2ų╗─▄ū„×ķ▀^č§╗»Üõ╚▄ę║ĘųĮŌĄ─┤▀╗»ä®
B. ═¼ę╗éĆ╗»īWĘ┤æ¬┐╔ęįėąČÓĘN┤▀╗»ä®
C. ┤▀╗»ä®─▄╩╣įŁ▒Š▓╗░l╔·Ą─Ę┤æ¬ę▓─▄┐ņ╦┘▀Mąą
D. ė├ū„┤▀╗»ä®Ą─╬’┘|▓╗┐╔─▄╩ŪŲõ╦³Ę┤æ¬Ą─Ę┤æ¬╬’╗“╔·│╔╬’
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║│§ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐─│ąŻčąŠ┐ąįīW┴ĢąĪĮMė├Ž┬łDčbų├▀MąąµVŚlį┌┐šÜŌųą╚╝¤²Ą─īŹ“ׯ¼╚╝¤²Īó└õģs║¾┤“ķ_ų╣╦«ŖAŻ¼▀M╚ļ╝»ÜŌŲ┐ųą╦«Ą─¾wĘe╝sš╝╝»ÜŌŲ┐¾wĘeĄ─70%ĪŻ
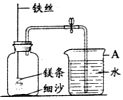
Ż©1Ż®łDųąAāxŲ„Ą─├¹ĘQ╩Ū________Ż¼╚╝¤²Īó└õģs║¾┤“ķ_ų╣╦«ŖAŻ¼╦«─▄▀M╚ļ╝»ÜŌŲ┐Ą─įŁę“╩Ū_____________ĪŻ
Ż©2Ż®╚ń╣¹µVŚlų╗║═┐šÜŌųąĄ─č§ÜŌĘ┤æ¬Ż¼ät▀M╚ļ╝»ÜŌŲ┐ųą╦«Ą─¾wĘeūŅČÓ▓╗│¼▀^Ųõ╚▌ĘeĄ─_____%ĪŻ¼F▀M╚ļ╝»ÜŌŲ┐ųą╦«Ą─¾wĘe╝s×ķŲõ╚▌ĘeĄ─70%Ż¼Ė∙ō■┐šÜŌĄ─ĮM│╔┐╔═Ų│÷£p╔┘Ą─ÜŌ¾wųąėąĄ¬ÜŌĪŻ
Ż©░l¼Få¢Ņ}Ż®Ą¬ÜŌ╩Ūį§śė£p╔┘Ą──žŻ┐
Ż©╝┘įOę╗Ż®Ą¬ÜŌ┼cµVŚlĘ┤æ¬Č°£p╔┘ĪŻ
Ż©╝┘įOČ■Ż®__________ĪŻ
Ż©▓ķķå┘Y┴ŽŻ®µVŚlį┌Ą¬ÜŌųą─▄╚╝¤²Ż¼«a╬’×ķĄ¬╗»µVŻ©Mg3N2Ż®╣╠¾wĪŻĄ¬╗»µVųąĄ¬į¬╦žĄ─╗»║Žār×ķ_________ĪŻ
µVŚl▀Ć┐╔ęįį┌Č■č§╗»╠╝ÜŌ¾wųą╚╝¤²╔·│╔╠╝║═č§╗»µVŻ¼įōĘ┤æ¬╗»īWĘĮ│╠╩Į╩Ū__________ĪŻ
Ż©═žš╣čė╔ņŻ®ė╔┤╦─Ńī”╚╝¤²Ą─ą┬šJūR________
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║│§ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐Å─Ž┬┴ąłD╩Š┐╔ęį┴╦ĮŌĄ─ą┼ŽóųąŻ¼š²┤_Ą─╩Ū(ĪĪĪĪ)
A. ![]() Ż║┤╦łD╩Ūę╗ĘNįŁūėĄ─ĮYśŗ╩ŠęŌłD
Ż║┤╦łD╩Ūę╗ĘNįŁūėĄ─ĮYśŗ╩ŠęŌłD
B.  Ż║┤╦łDųąį¬╦žĄ─ŽÓī”įŁūė┘|┴┐×ķ18
Ż║┤╦łDųąį¬╦žĄ─ŽÓī”įŁūė┘|┴┐×ķ18
C. ![]() Ż║╚¶Ī░
Ż║╚¶Ī░![]() Ī▒▒Ē╩Šč§įŁūėŻ¼ät┤╦łD┐╔▒Ē╩Šč§ÜŌĘųūė
Ī▒▒Ē╩Šč§įŁūėŻ¼ät┤╦łD┐╔▒Ē╩Šč§ÜŌĘųūė
D. ![]() Ż║▒Ē╩Šå╬┘|ŌcųąŌcį¬╦žĄ─╗»║Žār×ķŻ½1ār
Ż║▒Ē╩Šå╬┘|ŌcųąŌcį¬╦žĄ─╗»║Žār×ķŻ½1ār
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║│§ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
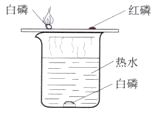
ĪŠŅ}─┐Ī┐├µĘ█╝ė╣żÅSĄ─▄ćķg└’╚¶æęĖĪų°▌^ČÓĄ─├µĘ█Ę█ēmŻ¼ė÷├„╗Š═ėą▒¼š©Ą─╬ŻļUŻ¼▀@╩Ūę“×ķ├µĘ█Ę█ēm┼c┐šÜŌ│õĘųĮėė|║¾Ż¼ė÷ĄĮ├„╗╝▒äĪ╚╝¤²Ż¼į┌Č╠Ģrķgā╚Š█╝»┤¾┴┐Ą─¤ßŻ¼╩╣ÜŌ¾wĄ─¾wĘeį┌ėąŽ▐┐šķgā╚čĖ╦┘┼“├øŻ¼Å─Č°ę²Ų▒¼š©ĪŻŽ┬├µ╩Ū─ŻöMĘ█ēm▒¼š©Ą─ę╗éĆīŹ“ׯ║╚ńŽ┬łD╦∙╩ŠŻ¼į┌¤o╔wąĪ╦▄┴Ž═▓└’Ę┼╚ļĖ╔į’├µĘ█Ż¼³c╚╝Ž×ĀTŻ¼ė├╦▄┴Ž╔w╔wūĪĮī┘═▓Ż¼čĖ╦┘╣─╚ļ┤¾┴┐┐šÜŌŻ¼▓╗Š├▒ŃĢ■┬ĀĄĮĪ░┼ķĪ▒Ą─ę╗┬ĢŻ¼▒¼š©Ą─ÜŌ└╦īóĮī┘═▓Ą─╦▄┴Ž╔wŽŲŲĪŻįćå¢Ż║
(1)īŹ“×ųąŻ¼╣─╚ļ┐šÜŌĄ──┐Ą─╩Ū________________ĪŻ
(2)Ž┬┴ąŪķørŽ┬Ż¼▓╗Ģ■░l╔·▒¼š©Ą─╩Ū________(╠Ņą“╠¢)ĪŻ
ó┘Įī┘═▓▓╗╝ė╔wĢr ó┌Ž×ĀTø]ėą³c╚╝Ģr ó█¤o╔wąĪ╦▄┴Ž═▓ųąčbĄ─╩ŪĖ╔į’├║Ę█Ģr
(3)├µĘ█ÅS×ķ┴╦▒▄├Ō▒¼š©╩┬╣╩░l╔·Ż¼æ¬▓╔╚ĪĄ─░▓╚½┤ļ╩®╩Ū_______________(ę╗ĘN╝┤┐╔)ĪŻ

▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
ć°ļHīWąŻā×▀x - ŠÜ┴Ģāį┴ą▒Ē - įćŅ}┴ą▒Ē
║■▒▒╩Ī╗ź┬ōŠW▀`Ę©║═▓╗┴╝ą┼Žó┼eł¾ŲĮ┼_ | ŠW╔Žėą║”ą┼Žó┼eł¾īŻģ^ | ļŖą┼įp“_┼eł¾īŻģ^ | ╔µÜv╩Ę╠ō¤oų„┴xėą║”ą┼Žó┼eł¾īŻģ^ | ╔µŲ¾ŪųÖÓ┼eł¾īŻģ^
▀`Ę©║═▓╗┴╝ą┼Žó┼eł¾ļŖįÆŻ║027-86699610 ┼eł¾Ó]ŽõŻ║58377363@163.com