
題目列表(包括答案和解析)
(16分)化學(xué)發(fā)展史上,有許多偶然事件引起科學(xué)發(fā)現(xiàn)的事例,碘的發(fā)現(xiàn)也得益于Courtoris對意外現(xiàn)象的注意。碘是人類發(fā)現(xiàn)的第二個(gè)生物必需微量元素,它以碘化物形式存在于海水、海藻及人體甲狀腺中。人類缺碘會引起甲狀腺腫大,我國已全面實(shí)施加碘鹽方案。
3-1 單質(zhì)碘的制備方法之一是在酸性條件下通Cl2于NaI溶液中,指出運(yùn)用該法時(shí)應(yīng)注意的問題?分析其原因,寫出有關(guān)反應(yīng)方程式。
3-2 在100%硫酸中,I2可被HIO3氧化成I3+,寫出配平的離子方程式。
3-3 為什么在日照強(qiáng)、溫度高的海區(qū),表層水碘濃度往往要低一些?
3-4 人體缺碘會影響正常的生命活動。兒童缺碘會造成身體畸形,智力低下。成年人缺碘會因新陳代謝能力降低而導(dǎo)致全身無力,提早出現(xiàn)衰老現(xiàn)象。為提高人體素質(zhì),食物補(bǔ)碘已引起人們的重視。據(jù)報(bào)道,人從食物中攝取碘后便在甲狀腺中積存下來,通過一系列化學(xué)反應(yīng)形成甲狀腺素。甲狀腺素的結(jié)構(gòu):
(1)寫出甲狀腺素的化學(xué)式 ;
(2)在甲狀腺內(nèi),甲狀腺素的主要合成過程如下:
A(氨基酸)![]() B
B![]() 甲狀腺素+C(氨基酸)
甲狀腺素+C(氨基酸)
請寫出A、B、C的結(jié)構(gòu)簡式。
3-5 科研表明,人的一生只要能攝入一小茶匙的碘就能正常發(fā)育,健康生活。目前預(yù)防缺碘的有效辦法是食用含碘食鹽。目前國內(nèi)食鹽加碘加的主要是碘酸鉀。
(1)寫出工業(yè)上以KI為原料制備碘酸鉀的化學(xué)方程式;
(2)如何用簡易操作檢驗(yàn)食鹽是否加碘。寫出離子反應(yīng)方程式。
3-6 已知反應(yīng)H2+I(xiàn)2![]() 2HI,分兩步完成I2
2HI,分兩步完成I2![]() 2I H2+2I
2I H2+2I![]() 2HI
2HI
式中k,k1,k2,k3是分別為各反應(yīng)相應(yīng)的速率常數(shù),若用Ea,E1,E2,E3分別表示各反應(yīng)相應(yīng)的活化能,請找出Ea和E1,E2,E3間的關(guān)系。已知公式如下:
①對于反應(yīng)aA+bB→eE+f F,反應(yīng)速率為:v=k[A]a[B]b
②速率常數(shù)與活化能之間滿足阿侖尼烏斯公式:k=Ae-Ea/RT
③對于反應(yīng)I2![]() 2I滿足:v正=v逆
2I滿足:v正=v逆
(20分)選修四模塊的平衡理論主要包括:化學(xué)平衡、電離平衡、水解平衡和溶解平衡四種,且均符合勒夏特列原理。請回答下列問題:
(1) 一定溫度下,在一個(gè)固定容積的密閉容器中,可逆反應(yīng) A(g) +2B(g)  4C (g) △H >0 達(dá)到平衡時(shí),c(A) ="2" mol·L-1,c ( B) =" 7" mol·L-1,c ( C) =" 4" mol·L-1。試確定B的起始濃度c (B)的取值范圍是 ;若改變條件重新達(dá)到平衡后體系中C的質(zhì)量分?jǐn)?shù)增大,下列措施可行的是 。
4C (g) △H >0 達(dá)到平衡時(shí),c(A) ="2" mol·L-1,c ( B) =" 7" mol·L-1,c ( C) =" 4" mol·L-1。試確定B的起始濃度c (B)的取值范圍是 ;若改變條件重新達(dá)到平衡后體系中C的質(zhì)量分?jǐn)?shù)增大,下列措施可行的是 。
A. 增加C的物質(zhì)的量 B. 加壓
C. 升溫 D.使用催化劑
(2)常溫下,取 pH=2的鹽酸和醋酸溶液各100mL, 向其中分別加入適量的Zn粒,反應(yīng)過程中兩溶液的pH變化如右圖所示。則圖中表示醋酸溶液中pH變化曲線的是 ( 填“A”或“B”)。 設(shè)鹽酸中加入的Zn質(zhì)量為m1,醋酸溶液中加入的Zn質(zhì)量為 m2。 則
m1 m2 ( 選填“<”、“=”、“>”)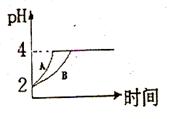
(3) 在體積為3L的密閉容器中,CO與H2在一定條件下反應(yīng)生成甲醇:CO ( g) + 2H2( g) → CH3OH(g) ΔH= —91kJ·mol-1。反應(yīng)達(dá)到平衡時(shí),平衡常數(shù)表達(dá)式K= ,升高溫度,K值 (填“增大”、“減小”或“不變”)。
(4) 難溶電解質(zhì)在水溶液中也存在溶解平衡。在常溫下,溶液里各離子濃度以它們化學(xué)計(jì)量數(shù)為方次的乘積是一個(gè)常數(shù),叫溶度積常數(shù)。例如: Cu(OH)2(s) Cu2+ (aq) + 2OH - ( aq),Ksp =" c" (Cu2+ ) c 2(OH - ) =" 2×10" -20。當(dāng)溶液中各離子濃度計(jì)量數(shù)方次的乘積大于溶度積時(shí),則產(chǎn)生沉淀。若某CuSO4溶液里c( Cu2+) ="0.02" mol·L-1,如果生成Cu(OH)2沉淀,應(yīng)調(diào)整溶液pH,使pH大于 ; 要使0.2 mol·L-1的CuSO4溶液中Cu2+沉淀較為完全 ( 使Cu2+濃度降至原來的萬分之一)則應(yīng)向溶液里加NaOH溶液,使溶液pH等于 。
Cu2+ (aq) + 2OH - ( aq),Ksp =" c" (Cu2+ ) c 2(OH - ) =" 2×10" -20。當(dāng)溶液中各離子濃度計(jì)量數(shù)方次的乘積大于溶度積時(shí),則產(chǎn)生沉淀。若某CuSO4溶液里c( Cu2+) ="0.02" mol·L-1,如果生成Cu(OH)2沉淀,應(yīng)調(diào)整溶液pH,使pH大于 ; 要使0.2 mol·L-1的CuSO4溶液中Cu2+沉淀較為完全 ( 使Cu2+濃度降至原來的萬分之一)則應(yīng)向溶液里加NaOH溶液,使溶液pH等于 。
(5) 常溫下,某純堿(Na2CO3) 溶液中滴入酚酞,溶液呈紅色。則該溶液呈 性。在分析該溶液遇酚酞呈紅色原因時(shí),甲同學(xué)認(rèn)為是配制溶液所用的純堿樣品中混有NaOH 所致;乙同學(xué)認(rèn)為是溶液中Na2CO3電離出的CO32-水解所致。請你設(shè)計(jì)一個(gè)簡單的實(shí)驗(yàn)方案用來評判甲乙兩位同學(xué)的觀點(diǎn)是否正確(包括操作、現(xiàn)象和結(jié)論) 。
(20分)選修四模塊的平衡理論主要包括:化學(xué)平衡、電離平衡、水解平衡和溶解平衡四種,且均符合勒夏特列原理。請回答下列問題:
(1) 一定溫度下,在一個(gè)固定容積的密閉容器中,可逆反應(yīng)
A(g) +2B(g)  4C (g) △H >0 達(dá)到平衡時(shí),c(A) ="2" mol·L-1,c ( B) =" 7" mol·L-1,c ( C) =" 4" mol·L-1。試確定B的起始濃度c (B)的取值范圍是 ;若改變條件重新達(dá)到平衡后體系中C的質(zhì)量分?jǐn)?shù)增大,下列措施可行的是 。
4C (g) △H >0 達(dá)到平衡時(shí),c(A) ="2" mol·L-1,c ( B) =" 7" mol·L-1,c ( C) =" 4" mol·L-1。試確定B的起始濃度c (B)的取值范圍是 ;若改變條件重新達(dá)到平衡后體系中C的質(zhì)量分?jǐn)?shù)增大,下列措施可行的是 。
A. 增加C的物質(zhì)的量 B. 加壓
C. 升溫 D.使用催化劑
(2)常溫下,取 pH=2的鹽酸和醋酸溶液各100mL, 向其中分別加入適量的Zn粒,反應(yīng)過程中兩溶液的pH變化如右圖所示。則圖中表示醋酸溶液中pH變化曲線的是 ( 填“A”或“B”)。 設(shè)鹽酸中加入的Zn質(zhì)量為m1,醋酸溶液中加入的Zn質(zhì)量為 m2。 則
m1 m2 ( 選填“<”、“=”、“>”)

(3) 在體積為3L的密閉容器中,CO與H2在一定條件下反應(yīng)生成甲醇:CO ( g) + 2H2( g) → CH3OH(g) ΔH= —91kJ·mol-1。反應(yīng)達(dá)到平衡時(shí),平衡常數(shù)表達(dá)式K= ,升高溫度,K值 (填“增大”、“減小”或“不變”)。
(4) 難溶電解質(zhì)在水溶液中也存在溶解平衡。在常溫下,溶液里各離子濃度以它們化學(xué)計(jì)量數(shù)為方次的乘積是一個(gè)常數(shù),叫溶度積常數(shù)。例如: Cu(OH)2(s) Cu2+ (aq) + 2OH - ( aq),Ksp =" c" (Cu2+ ) c 2(OH
- ) =" 2×10" -20。當(dāng)溶液中各離子濃度計(jì)量數(shù)方次的乘積大于溶度積時(shí),則產(chǎn)生沉淀。若某CuSO4溶液里c( Cu2+) ="0.02" mol·L-1,如果生成Cu(OH)2沉淀,應(yīng)調(diào)整溶液pH,使pH大于 ;
要使0.2 mol·L-1的CuSO4溶液中Cu2+沉淀較為完全 ( 使Cu2+濃度降至原來的萬分之一)則應(yīng)向溶液里加NaOH溶液,使溶液pH等于 。
Cu2+ (aq) + 2OH - ( aq),Ksp =" c" (Cu2+ ) c 2(OH
- ) =" 2×10" -20。當(dāng)溶液中各離子濃度計(jì)量數(shù)方次的乘積大于溶度積時(shí),則產(chǎn)生沉淀。若某CuSO4溶液里c( Cu2+) ="0.02" mol·L-1,如果生成Cu(OH)2沉淀,應(yīng)調(diào)整溶液pH,使pH大于 ;
要使0.2 mol·L-1的CuSO4溶液中Cu2+沉淀較為完全 ( 使Cu2+濃度降至原來的萬分之一)則應(yīng)向溶液里加NaOH溶液,使溶液pH等于 。
(5) 常溫下,某純堿(Na2CO3) 溶液中滴入酚酞,溶液呈紅色。則該溶液呈 性。在分析該溶液遇酚酞呈紅色原因時(shí),甲同學(xué)認(rèn)為是配制溶液所用的純堿樣品中混有NaOH 所致;乙同學(xué)認(rèn)為是溶液中Na2CO3電離出的CO32-水解所致。請你設(shè)計(jì)一個(gè)簡單的實(shí)驗(yàn)方案用來評判甲乙兩位同學(xué)的觀點(diǎn)是否正確(包括操作、現(xiàn)象和結(jié)論) 。
選修四模塊的平衡理論主要包括:化學(xué)平衡、電離平衡、水解平衡和溶解平衡四種,且均符合勒夏特列原理。請回答下列問題:
(1) 一定溫度下,在一個(gè)固定容積的密閉容器中,可逆反應(yīng) A(g) +2B(g) ![]() 4C (g) △H >0 達(dá)到平衡時(shí),c(A) =2 mol·L-1,c ( B) = 7 mol·L-1,c ( C) = 4 mol·L-1。試確定B的起始濃度c (B)的取值范圍是 ;若改變條件重新達(dá)到平衡后體系中C的質(zhì)量分?jǐn)?shù)增大,下列措施可行的是 。
4C (g) △H >0 達(dá)到平衡時(shí),c(A) =2 mol·L-1,c ( B) = 7 mol·L-1,c ( C) = 4 mol·L-1。試確定B的起始濃度c (B)的取值范圍是 ;若改變條件重新達(dá)到平衡后體系中C的質(zhì)量分?jǐn)?shù)增大,下列措施可行的是 。
 A. 增加C的物質(zhì)的量 B. 加壓
A. 增加C的物質(zhì)的量 B. 加壓
C. 升溫 D. 使用催化劑
(1)常溫下,取 pH=2的鹽酸和醋酸溶液各100mL, 向其中分別加入適量的Zn粒,反應(yīng)過程中兩溶液的pH變化如右圖所示。則圖中表示醋酸溶液中pH變化曲線的是 ( 填“A”或“B”)。 設(shè)鹽酸中加入的Zn質(zhì)量為m1,醋酸溶液中加入的Zn質(zhì)量為 m2。 則
m1 m2 ( 選填“<”、“=”、“>”)
(3) 在體積為3L的密閉容器中,CO與H2在一定條件下反應(yīng)生成甲醇:CO ( g) + 2H2( g) → CH3OH(g) ΔH= —91kJ·mol-1。反應(yīng)達(dá)到平衡時(shí),平衡常數(shù)表達(dá)式K= ,升高溫度,K值 (填“增大”、“減小”或“不變”)。
(4) 難溶電解質(zhì)在水溶液中也存在溶解平衡。在常溫下,溶液里各離子濃度以它們化學(xué)計(jì)量數(shù)為方次的乘積是一個(gè)常數(shù),叫溶度積常數(shù)。例如: Cu(OH)2(s)![]() Cu2+ (aq) + 2OH - ( aq),Ksp = c (Cu2+ ) c 2(OH - ) = 2×10 -20。當(dāng)溶液中各離子濃度計(jì)量數(shù)方次的乘積大于溶度積時(shí),則產(chǎn)生沉淀。若某CuSO4溶液里c( Cu2+) =0.02 mol·L-1,如果生成Cu(OH)2沉淀,應(yīng)調(diào)整溶液pH,使pH大于 ; 要使0.2 mol·L-1的CuSO4 溶液中Cu2+沉淀較為完全 ( 使Cu2+濃度降至原來的萬分之一)則應(yīng)向溶液里加NaOH溶液,使溶液pH等于 。
Cu2+ (aq) + 2OH - ( aq),Ksp = c (Cu2+ ) c 2(OH - ) = 2×10 -20。當(dāng)溶液中各離子濃度計(jì)量數(shù)方次的乘積大于溶度積時(shí),則產(chǎn)生沉淀。若某CuSO4溶液里c( Cu2+) =0.02 mol·L-1,如果生成Cu(OH)2沉淀,應(yīng)調(diào)整溶液pH,使pH大于 ; 要使0.2 mol·L-1的CuSO4 溶液中Cu2+沉淀較為完全 ( 使Cu2+濃度降至原來的萬分之一)則應(yīng)向溶液里加NaOH溶液,使溶液pH等于 。
(5) 常溫下,某純堿(Na2CO3) 溶液中滴入酚酞,溶液呈紅色。則該溶液呈 性。在分析該溶液遇酚酞呈紅色原因時(shí),甲同學(xué)認(rèn)為是配制溶液所用的純堿樣品中混有NaOH 所致;乙同學(xué)認(rèn)為是溶液中Na2CO3電離出的CO32-水解所致。請你設(shè)計(jì)一個(gè)簡單的實(shí)驗(yàn)方案用來評判甲乙兩位同學(xué)的觀點(diǎn)是否正確(包括操作、現(xiàn)象和結(jié)論) 。
 4C (g) △H >0 達(dá)到平衡時(shí),c(A) ="2" mol·L-1,c ( B) =" 7" mol·L-1,c ( C) =" 4" mol·L-1。試確定B的起始濃度c (B)的取值范圍是 ;若改變條件重新達(dá)到平衡后體系中C的質(zhì)量分?jǐn)?shù)增大,下列措施可行的是 。
4C (g) △H >0 達(dá)到平衡時(shí),c(A) ="2" mol·L-1,c ( B) =" 7" mol·L-1,c ( C) =" 4" mol·L-1。試確定B的起始濃度c (B)的取值范圍是 ;若改變條件重新達(dá)到平衡后體系中C的質(zhì)量分?jǐn)?shù)增大,下列措施可行的是 。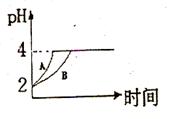
 Cu2+ (aq) + 2OH - ( aq),Ksp =" c" (Cu2+ ) c 2(OH - ) =" 2×10" -20。當(dāng)溶液中各離子濃度計(jì)量數(shù)方次的乘積大于溶度積時(shí),則產(chǎn)生沉淀。若某CuSO4溶液里c( Cu2+) ="0.02" mol·L-1,如果生成Cu(OH)2沉淀,應(yīng)調(diào)整溶液pH,使pH大于 ; 要使0.2 mol·L-1的CuSO4溶液中Cu2+沉淀較為完全 ( 使Cu2+濃度降至原來的萬分之一)則應(yīng)向溶液里加NaOH溶液,使溶液pH等于 。
Cu2+ (aq) + 2OH - ( aq),Ksp =" c" (Cu2+ ) c 2(OH - ) =" 2×10" -20。當(dāng)溶液中各離子濃度計(jì)量數(shù)方次的乘積大于溶度積時(shí),則產(chǎn)生沉淀。若某CuSO4溶液里c( Cu2+) ="0.02" mol·L-1,如果生成Cu(OH)2沉淀,應(yīng)調(diào)整溶液pH,使pH大于 ; 要使0.2 mol·L-1的CuSO4溶液中Cu2+沉淀較為完全 ( 使Cu2+濃度降至原來的萬分之一)則應(yīng)向溶液里加NaOH溶液,使溶液pH等于 。高三化學(xué)
第I卷(選擇題,共48分)
一.選擇題(本題包括24小題,每小題2分,共48分。每小題只有一個(gè)選項(xiàng)符合題意。)
題號
1
2
3
4
5
6
7
8
9
10
答案
C
C
D
B
C
D
C
A
C
B
題號
11
12
13
14
15
16
17
18
19
20
答案
D
C
B
A
C
D
C
B
A
A
題號
21
22
23
24
答案
B
B
C
D
第II卷(共52分)
二.簡答題(本大題包括5小題,共45分。)
【考生注意】第25題分A、B兩題,考生可任選一題。若兩題均做,一律按A題計(jì)分。
25.(A題,8分)(1)畫出金屬元素與非金屬元素的分界線(2分)
Na
Cl
(2) IVA 族。(1分,其他答案均不給分)
(3)①見表中“Na”和“Cl”(各1分,寫成名稱或位置寫錯均不給分)。
② 氯 (填名稱,1分),化學(xué)反應(yīng)方程式 Cl2+H2S=2HCl+S(2分,其他合理答案也給分) 。
25.(B題,8分)
Mg
Al