
題目列表(包括答案和解析)
海底蘊藏著大量的“可燃冰”。用甲烷制水煤氣(CO、H2),再合成甲醇來代替日益供應緊張的燃油。
已知:① CH4(g)+H2O (g)=CO (g)+3H2 (g) △H1=+206.2kJ·mol-1
② CH4(g)+ O2(g)=CO(g)+2H2(g)
△H2=-35.4 kJ·mol-1
O2(g)=CO(g)+2H2(g)
△H2=-35.4 kJ·mol-1
③ CH4 (g)+2H2O (g)=CO2 (g)+4H2 (g) △H3=+165.0 kJ·mol-1
(1)CH4(g)與CO2 (g)反應生成CO(g)和H2(g)的熱化學方程式為 。
(2)從原料、能源利用的角度,分析反應②作為合成甲醇更適宜方法的原因是 。
(3)水煤氣中的H2可用于生產NH3,在進入合成塔前常用[Cu(NH3)2]Ac溶液來吸收其中的CO,防止合成塔中的催化劑中毒,其反應是: [Cu(NH3)2]Ac
+ CO + NH3  [Cu(NH3)3]Ac·CO
△H<0
[Cu(NH3)3]Ac·CO
△H<0
[Cu(NH3)2]Ac溶液吸收CO的適宜生產條件應是 。
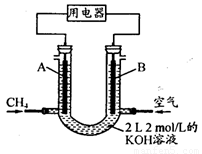
(4)將CH4設計成燃料電池,其利用率更高,裝置示意如下圖(A、B為多孔性石墨棒)。持續通入甲烷,在標準狀況下,消耗甲烷體積VL。0<V≤44.8 L時,電池總反應方程式為 。
② 44.8 L<V≤89.6 L時,負極電極反應為 。
③ V=67.2 L時,溶液中離子濃度大小關系為 。
(14分)氮是地球上含量豐富的一種元素,氮元素的
單質及其化合物在工農業生產、生活中有著重要作用。
(1)根據右側能量變化示意圖,請寫出NO2和CO反應
的熱化學方程式 。
(2)在固定體積的密閉容器中,進行如下化學反應:
N2(g)+3H2(g)2NH3(g) △H < 0 ,
其平衡常數K與溫度T的關系如下表:
| T/K | 298 | 398 | 498 |
| 平衡常數K | 4.1×106 | K1 | K2 |
①該反應的平衡常數表達式:K=
②試判斷K1 K2(填寫“>”,“=”或“<”)
③下列各項能說明該反應已達到平衡狀態的是 (填字母)
a.容器內N2、H2、NH3的濃度之比為1∶3∶2 b.v(N2)正 = 3v(H2)逆
c.容器內壓強保持不變 d.混合氣體的密度保持不變
(3)對反應N2O4(g)2NO2(g) △H > 0 ,在溫度分別為T1、T2時,平衡體系中NO2的體積分數隨壓強變化曲線如右圖所示,下列說法正確的是 。
a.A、C兩點的反應速率:A>C
b.A、C兩點的化學平衡常數:A>C
c.A、C兩點N2O4的轉化率:A>C
d.由狀態B到狀態A,可以用加熱的方法
(4)一定溫度下,在1L密閉容器中充入1molN2和3molH2并發生反應。若容器容積恒定,10min達到平衡時,氣體的總物質的量為原來的7/8,則N2的轉化率a(N2)= , 以NH3表示該過程的反應速率v(NH3)= 。
(14分)甲烷可制成合成氣(CO、H2),再制成甲醇,代替日益供應緊張的燃油。
已知:① CH4 (g) + H2O (g) = CO(g)+3H2 (g) △H1=+206.2kJ·mol-1
② CH4(g)+![]() O2(g)=CO(g)+2H2(g) △H2=-35.4 kJ·mol-1
O2(g)=CO(g)+2H2(g) △H2=-35.4 kJ·mol-1
③ CH4 (g) + 2H2O (g) =CO2 (g) +4H2 (g) △H3=+165.0 kJ·mol-1
(1)CH4(g)與CO2 (g)反應生成CO(g)和H2(g)的熱化學方程式為 。
(2)從原料選擇和能源利用角度,比較方法①和②,為合成甲醇,用甲烷制合成氣的適宜方法為 (填序號),其原因是 。
(3)合成氣中的H2可用于生產NH3,在進入合成塔前常用Cu(NH3)2Ac溶液來吸收其中的CO,防止合成塔中的催化劑中毒,其反應是:
Cu(NH3)2Ac + CO + NH3 [Cu(NH3)3]Ac·CO △H<0
Cu(NH3)2Ac溶液吸收CO的適宜生產條件應是 。
(4)將CH4設計成燃料電池,其利用率更高,裝置示意如右圖(A、B為多孔性碳棒)。持續通入甲烷,在標準狀況下,消耗甲烷體積VL。
① O<V≤44.8 L時,電池總反應方程式為 ;
② 44.8 L<V≤89.6 L時,負極電極反應為 ;
③V=67.2 L時,溶液中離子濃度大小關系為 。
(14分)甲烷可制成合成氣(CO、H2),再制成甲醇,代替日益供應緊張的燃油。
已知:① CH4 (g) + H2O (g) = CO (g)+3H2 (g) △H1=+206.2kJ·mol-1
② CH4(g)+ O2(g)=CO(g)+2H2(g) △H2=-35.4 kJ·mol-1
O2(g)=CO(g)+2H2(g) △H2=-35.4 kJ·mol-1
③ CH4 (g) + 2H2O (g) =CO2 (g) +4H2 (g) △H3=+165.0 kJ·mol-1
(1)CH4(g)與CO2 (g)反應生成CO(g)和H2(g)的熱化學方程式為 。
(2)從原料選擇和能源利用角度,比較方法①和②,為合成甲醇,用甲烷制合成氣的適宜方法為 (填序號),其原因是 。
(3)合成氣中的H2可用于生產NH3,在進入合成塔前常用Cu(NH3)2Ac溶液來吸收其中的CO,防止合成塔中的催化劑中毒,其反應是:
Cu(NH3)2Ac + CO + NH3  [Cu(NH3)3]Ac·CO △H<0
[Cu(NH3)3]Ac·CO △H<0
Cu(NH3)2Ac溶液吸收CO的適宜生產條件應是 。
(4)將CH4設計成燃料電池,其利用率更高,裝置示意如右圖(A、B為多孔性碳棒)。持續通入甲烷,在標準狀況下,消耗甲烷體積VL。

① O<V≤44.8 L時,電池總反應方程式為 ;
② 44.8 L<V≤89.6 L時,負極電極反應為 ;
③ V=67.2 L時,溶液中離子濃度大小關系為 。
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com