
Ņ}─┐┴ą▒Ē(░³└©┤░Ė║═ĮŌ╬÷)
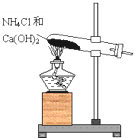 īŹ“×╩ę═©│Żė├╚ńłD╦∙╩ŠĄ─čbų├üĒųŲ╚Ī░▒ÜŌŻ«╗ž┤Ž┬┴ąå¢Ņ}Ż║
īŹ“×╩ę═©│Żė├╚ńłD╦∙╩ŠĄ─čbų├üĒųŲ╚Ī░▒ÜŌŻ«╗ž┤Ž┬┴ąå¢Ņ}Ż║░č×V╝łė├ĄĒĘ█║═ĄŌ╗»ŌøĄ─╚▄ę║Į■┼▌Ż¼┴└Ė╔║¾╝┤Ą├ĄĒĘ█ĄŌ╗»Ōøįć╝łĪŻīóįć╝łØÖر║¾Ż¼Ę┼į┌╩óėą┬╚ÜŌĄ─╝»ÜŌŲ┐┐┌Ż¼ė^▓ņĄĮĄ─¼FŽ¾╩Ū Ż¼įŁę“╩ŪŻ©ė├╗»īWĘĮ│╠╩Į║═▒žę¬Ą─╬─ūųšf├„Ż® ĪŻ

Ż©1Ż®╝ū═¼īW╚Ī║ŽĮśėŲĘ14.0 g╝ė╚ļAųąŻ¼╚╗║¾īóčbų├AĪóBŽÓ▀BŻ¼▓óŽ“Aųą╝ė╚ļ13.0 molĪżL-1Ą─Ž§╦ß25.0 mL│õĘųĘ┤æ¬║¾£yĄ├╔·│╔ÜŌ¾wĄ─¾wĘe×ķ2.24 L(ś╦£╩ĀŅørŽ┬)Ż¼╝░Ę┤æ¬║¾╚▌Ų„Aųą╚▄ę║H+ØŌČ╚×ķ1.0 molĪżL-1(╝┘įOĘ┤æ¬║¾╚▄ę║¾wĘe▓╗ūā)ĪŻ└¹ė├ęį╔ŽöĄō■Ż¼─ŃšJ×ķ╝ū═¼īW─▄Ą├ĄĮ║ŽĮųąŃ~Ą─┘|┴┐ĘųöĄå߯┐╚ń╣¹─▄Ż¼šłīæ│÷ėŗ╦Ń▀^│╠╝░ĮY╣¹Ż╗╚ń╣¹▓╗─▄Ż¼šł║å╩÷└Ēė╔ĪŻ
Ż©2Ż®ęę═¼īWīóčbų├AĪóCŽÓ▀BŻ¼Ž“Aųą╝ė╚ļw g║ŽĮśėŲĘ║═ūŃ┴┐ØŌŽ§╦ß│õĘųĘ┤æ¬Ż¼īó╔·│╔Ą─ÜŌ¾w║åå╬ū„┴╦╬³╩š╠Ä└Ē║¾Ż¼▒ŃŽ“Ę┤æ¬║¾Ą─A╚▄ę║ųą╝ė╚ļę╗ĘN│ŻęŖįć䮯¼│õĘųĘ┤æ¬║¾Ż¼į┘Įø▀^║åå╬Ą─īŹ“×▓┘ū„Š═▀_ĄĮ┴╦─┐Ą─ĪŻšł─Ń║å╩÷╦¹Ą─īŹ“×╦╝┬ĘĪŻ
Ż©3Ż®▒¹═¼īWīóčbų├AĪóDŽÓ▀BŻ¼Ž“Aųą╝ė╚ļę╗Č©┘|┴┐Ą─║ŽĮśėŲĘ║═ūŃ┴┐ØŌŽ§╦߯¼│õĘųĘ┤æ¬║¾ė├┼┼╦«╝»ÜŌĘ©£yČ©┴╦╔·│╔ÜŌ¾wĄ─¾wĘeŻ¼ę▓▀_ĄĮ┴╦īŹ“×─┐Ą─ĪŻ
ó┘Dųą░l╔·Ę┤æ¬Ą─╗»īWĘĮ│╠╩ĮŻ║______________________________________________ĪŻ
ó┌╝┘įOęčų¬║ŽĮųąCuĪóAgĄ─┐é╬’┘|Ą─┴┐×ķa mol,╦«Ž┤║¾ÜŌ¾wĄ─¾wĘe╩Ūb L(ś╦£╩ĀŅørŽ┬)Ż¼ät║ŽĮųąCuĄ─╬’┘|Ą─┴┐╩Ū___________ĪŻŻ©ĮY╣¹▓╗▒ž║å╗»Ż®
| ||
| ||
| ||
| ||
| ||
| ||
ć°ļHīWąŻā×▀x - ŠÜ┴Ģāį┴ą▒Ē - įćŅ}┴ą▒Ē
║■▒▒╩Ī╗ź┬ōŠW▀`Ę©║═▓╗┴╝ą┼Žó┼eł¾ŲĮ┼_ | ŠW╔Žėą║”ą┼Žó┼eł¾īŻģ^ | ļŖą┼įp“_┼eł¾īŻģ^ | ╔µÜv╩Ę╠ō¤oų„┴xėą║”ą┼Žó┼eł¾īŻģ^ | ╔µŲ¾ŪųÖÓ┼eł¾īŻģ^
▀`Ę©║═▓╗┴╝ą┼Žó┼eł¾ļŖįÆŻ║027-86699610 ┼eł¾Ó]ŽõŻ║58377363@163.com