
題目列表(包括答案和解析)
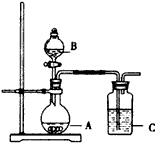
某研究性學習小組的同學為驗證濃硫酸與銅能反應而稀硫酸不能,設計了如圖所示裝置進行探究:將6.4 g 銅片和含0.2 moL溶質的18.4 mol/L濃硫酸放在圓底燒瓶中共熱,直到無氣體生成為止。(假定在此過程溶液體積不變)

(1)甲同學認為要證實上述結論,還應進行稀硫酸與銅片混合加熱實驗,你認為有無必要,并說明理由:________________
(2)下列試劑中能夠用來進一步證明反應結束后的燒瓶中確有余酸的是:_____
A.鐵粉 ?????? B.鈉 ???? ?? C.氯化鋇溶液 ???????? D.銀粉
(3)為定量測定余酸的物質的量濃度,甲、乙兩位同學進行了如下設計:
Ⅰ甲同學設想:在A裝置增加一個導管通氮氣驅趕氣體(假定生成的氣體全部逸出),先測定生成的SO2的量,然后計算剩余硫酸的濃度。他設計了如下二種方案來測定SO2的量:
方案① 將產生的氣體緩緩通入足量用稀硫酸酸化的KMnO4溶液,再加入足量BaCl2溶液,過濾、洗滌、干燥、稱量沉淀。
方案② 將氣體緩緩通入足量硝酸鋇溶液中,然后過濾、洗滌、干燥、稱量沉淀。
經仔細分析后,發現有不合理之處,請填寫下表(可以不填滿):
序號 | 不合理的原因 | 誤差 (偏低或偏高) | 改變措施 |
方案① |
|
|
|
方案② |
|
|
|
Ⅱ乙學生設計的方案是:分離出反應后的溶液并加蒸餾水稀釋至1000 mL,取20.00 mL于錐形瓶中,滴入2~3滴酚酞指示劑,用標準NaOH溶液進行滴定(已知氫氧化銅開始沉淀的pH約為5),這種方法能否求出余酸的濃度,理由是_______________________________________。
(4)請再設計其他可行的實驗方案,來測定余酸的物質的量濃度,簡要寫出操作步驟及需要測定的數據(不必計算,不必寫操作細節)_____________________________________________________。
某研究性學習小組的同學為驗證濃硫酸與銅能反應而稀硫酸不能,設計了如圖所示裝置進行探究:將6.4 g銅片和含0.2 moL溶質的18.4 mol/L濃硫酸放在圓底燒瓶中共熱,直到無氣體生成為止。(假定在此過程溶液體積不變)
(1)甲同學認為要證實上述結論,還應進行稀硫酸與銅片混合加熱實驗,你認為有無必要,并說明理由:________________
(2)下列試劑中能夠用來進一步證明反應結束后的燒瓶中確有余酸的是:_____
| A.鐵粉 | B.鈉 | C.氯化鋇溶液 | D.銀粉 |
| 序號 | 不合理的原因 | 誤差 (偏低或偏高) | 改變措施 |
| 方案① | | | |
| 方案② | | | |

| A.鐵粉 | B.鈉 | C.氯化鋇溶液 | D.銀粉 |
| 序號 | 不合理的原因 | 誤差 (偏低或偏高) | 改變措施 |
| 方案① | | | |
| 方案② | | | |
某校興趣小組對氫氧化鈉溶液和稀鹽酸混合后的有關問題,進行了如下探究:
Ⅰ.(1)甲同學為了證明氫氧化鈉溶液與稀鹽酸能夠發生反應,設計并完成了如下圖所示實驗.
X溶液是________,滴入的量一般為________.

(2)乙同學也設計完成了另一個實驗,證明氫氧化鈉溶液與鹽酸能夠發生反應.在盛有氫氧化鈉溶液的試管中,用膠頭滴管慢慢滴入稀鹽酸,不斷振蕩溶液,同時測定溶液的pH,直至鹽酸過量.①寫出測定溶液pH的方法:_________________________.
②下圖中哪個圖像符合該同學的記錄________(填序號).

(3)你認為甲、乙兩位同學的實驗中,________(填“甲同學”、“乙同學”、“甲乙兩同學”)的實驗能充分證明氫氧化鈉溶液與鹽酸發生了反應,請說明理由:
____________________________________.
Ⅱ.丙同學利用“保溫瓶式量熱計”(圖略),測出10 mL 10% NaOH溶液和不同體積的10%鹽酸溶液混合過程中,溶液的溫度變化見下表(假設兩溶液密度相同).

就此實驗回答:
(1)鹽酸和氫氧化鈉的反應是________(填“吸熱”或“放熱”)反應.
(2)請在圖中繪制出溶液的溫度上升與加入鹽酸體積之間的變化關系圖,并在曲線上畫出能表示兩者之間恰好完全反應的點,并用字母P表示.

Ⅲ.丁同學為測定標示質量分數為32%的鹽酸的實際質量分數,用pH測定儀組成實驗裝置.實驗時先在燒杯中加入20 g 40%的氫氧化鈉溶液,再逐滴加入該鹽酸,測定儀打印出加入鹽酸的質量與燒杯中溶液的pH關系圖.

(1)請以此次測定的結果,列式計算該鹽酸的實際質量分數.
(2)請分析你的計算結果與標簽標示的質量分數不一致的可能原因.
一、選擇題(本題包括9小題,每小題3分,共27分,每小題只有一個選項符合題意)
1. B 2.A 3.C 4.B 5.B 6.D 7.B 8.D 9. C
二、選擇題(本題9小題,每小題4分,共36分。每小題有一個或兩個選項符合題意)
10.AD 11.C 12.BC 13.D 14.AC 15.AD 16.A D 17.C 18.D
三、本題包括3小題,共34分)
19.(11分)NaCl+NH3+CO2+H2O = NaHCO3↓+NH4Cl(1分)
(1) 漏斗中與試管中的液面差保持不再變化或漏斗中的液面不再下降(2分)
(2) a, 氯化氫或HCl; 否 (3分)
(3) NH3; CO2; ①; (3分)
(4) 過濾 2NaHCO3 =Na2CO3+H2O+CO2↑ (2分)
20 . (11分)
Ⅰ. (1)酚酞(1分) 1~2滴(1分);
(2)①用干凈的玻璃棒蘸取待測液滴到pH試紙上,半分鐘后,將試紙的顏色與標準比色卡對照,讀出溶液的pH即可。(2分) ② C(1分)
(3)乙同學。(1分)
甲同學的實驗不能充分說明鹽酸的氫氧化鈉發生了反應,有可能是鹽酸和紅色物質反應生成了無色物質。乙同學的實驗,隨著滴加鹽酸,溶液的pH由大于7逐漸減少到7,這充分證明溶液中的氫氧化鈉因反應而消耗了;(2分)
Ⅱ. (4)29.2%;(2分) (5)鹽酸具有揮發性。(1分)
21. (12分)
(1)銅鋅及濃鹽酸一起組成了原電池,加快了反應速率 (2分)
(2)① 否(1分); 因為H2本身難溶于水 (1分);
②
驗證方法
預測現象及結論
將銅片加入稀硫酸中,并微熱(1分)
若無氣體放出,則不含鋅等活潑金屬雜質;
若有氣體則有鋅等雜質(1分)
(3)(任選一種方法即可)
驗證方法
預測現象及結論
向白色沉淀中加入稀HNO3等強氧化劑(1分)
溶液變藍色,說明是一價銅(1分)
向氯化亞銅懸濁液中加入氯化鉀溶液(1分)
如白色沉淀消失且得無色溶液,則原溶液為氯化亞銅,否則不是(1分)
(4).files/image064.gif) (2分);
(2分);
加水稀釋后,.files/image066.gif) <K,平衡向生成CuCl(s)的方向移動 (2分)
<K,平衡向生成CuCl(s)的方向移動 (2分)
四、(本題包括3小題,共34分)
22. (10分) (1).files/image068.gif)
(2)II因為濾液A是偏鋁酸鈉和氫氧化鈉溶液,按途徑I直接向A中加入鹽酸得到的AlCl3溶液中含有大量的氯化鈉雜質;按途徑II通入二氧化碳氣體,得Al(OH)3沉淀,將Al(OH)3溶解于鹽酸中得到的是純凈的AlCl3溶液。所以途徑II合理。
(3)蒸發濃縮、冷卻結晶
(4).files/image070.gif)
或.files/image072.gif)
(5)不合理 因為該方案操作步驟多、時間長,消耗試劑量大
(除(4)、(5)中第一個空每空1分以外,其余每空2分)
23、(共11分)
(1)BaSO4(s)+
(2)S2- + H2O .files/image073.jpg) HS- + OH-(2分)
HS- + OH-(2分)
(3)計算過程 :設每次用
BaSO4+CO32-=BaCO3+SO42-
(2.0-x) mol•L-1 x mol•L-1
.files/image075.gif) == 0.042 (2分)
== 0.042 (2分)
X = 0.081(0.084也給分) (1分);
處理次數 = 0.2mol/0.081mol=2.5(1分)(2.38也給分)。
答:至少處理3次 (1分)
(4)節能,環保 (各1分,共2分。合理答案就可得分)
24.(共13分)
(1)0.15(2分) 2(1-1/a) (3分) (2)N2+6e-+6H+=2NH3 (2分)
(3)N2 (1分) 生成NO的反應為放熱反應,升高溫度轉化率下降 (2分)
進一步與NO反應生成硝酸(1分)
(4) NO+NO2+H2O=2HNO2;(1分) CO (NH2)2+2HNO2=CO2+2N2+3H2O(1分)
五、(本題包括1小題,9分)
25.(9分)
(1)羧基、羥基(2分)
(2).files/image077.jpg) (2分)
(2分)
(3)消去反應;NaOH(或Na2CO3等其它合理答案)(2分)
(4)1、4
(5) .files/image079.jpg)
.files/image081.jpg)
.files/image083.jpg)
.files/image085.jpg) (1分)
(1分)
六、選擇題(本題包括2小題,每小題10分)
26. (10分)
(1)醛比酮容易發生該反應;
苯基酮極難發生該反應;
羰基所連的碳上氫原子越少或取代基越多或取代基的碳原子數越多,越難反應;
取代基為兩個乙基時,難以發生該反應。 (各1分,任寫三條)
(2) HCl、NaOH(或Na2CO3、Cl2能降低NaHSO3濃度的試劑 )(2分)
(3)①(CH3)2CHCOCH3 + 3Cl2 + 3NaOH → (CH3)2CHCOCCl3 + 3NaCl + 3H2O(2分)
②(CH3)2CHCOONa(1分)
(4) 氧化還原反應 (氧化反應、還原反應、歧化反應 )(1分)
萃取(或蒸餾)(1分)
27. (1)MgO>CaO>NaCl>KCl (2分)
(2) ①1s22s22p63s23p63d104s1或[Ar] 3d104s1 (1分) C(1分)
② 水的熔、沸點較高,結冰時密度減小(2分)
③正四面體(2分)
(3)B
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com