
題目列表(包括答案和解析)
(12分)某探究小組將一批廢棄的線路板簡單處理后,得到含70%Cu、25%Al、4%Fe及少量Au、Pt等金屬的混合物,并設計出如下制備硫酸銅和硫酸鋁晶體的路線: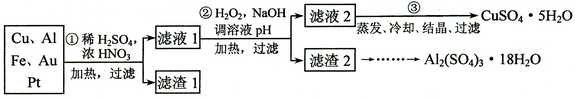
請回答下列問題:
⑴第①步Cu與酸反應的離子方程式______________ 。
⑵第②步加H2O2的作用是_______________;調溶液pH的目的是使____________生成沉淀。
⑶用第③步所得CuSO4·5H2O制備無水CuSO4的方法是______________。
⑷由濾渣2制取Al2(SO4)3·18H2O ,探究小組設計了三種方案: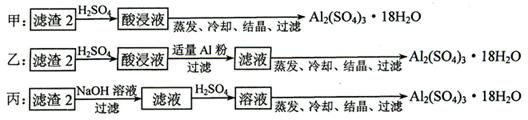
上述三種方案中,_______方案不可行,原因是_____________________________;
從原子利用率角度考慮,___________方案更合理。
⑸探究小組用滴定法測定CuSO4·5H2O含量。取a g試樣配成100 mL溶液,每次取20.00 mL,消除干擾離子后,用c mol /L EDTA(H2Y2-)標準溶液滴定至終點,平均消耗EDTA溶液6 mL。滴定反應如下:Cu2+ + H2Y2-= CuY2- + 2H+
寫出計算CuSO4·5H2O質量分數的表達式ω= _____________________________ ;
下列操作會導致CuSO4·5H2O含量的測定結果偏高的是_____________。
a.未干燥錐形瓶
b.滴定終點時滴定管尖嘴中產生氣泡
c.未除凈可與EDTA反應的干擾離子
(12分)某探究小組將一批廢棄的線路板簡單處理后,得到含70%Cu、25%Al、4%Fe及少量Au、Pt等金屬的混合物,并設計出如下制備硫酸銅和硫酸鋁晶體的路線:
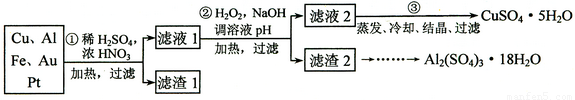
請回答下列問題:
⑴ 第①步Cu與酸反應的離子方程式______________ 。
⑵ 第②步加H2O2的作用是_______________;調溶液pH的目的是使____________生成沉淀。
⑶ 用第③步所得CuSO4·5H2O制備無水CuSO4的方法是______________。
⑷ 由濾渣2制取Al2(SO4)3·18H2O ,探究小組設計了三種方案:
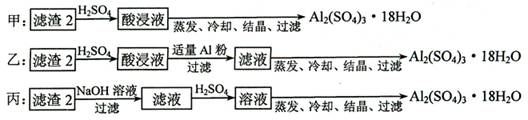
上述三種方案中,_______方案不可行,原因是_____________________________;
從原子利用率角度考慮,___________方案更合理。
⑸ 探究小組用滴定法測定CuSO4·5H2O含量。取a g試樣配成100 mL溶液,每次取20.00 mL,消除干擾離子后,用c mol /L EDTA(H2Y2-)標準溶液滴定至終點,平均消耗EDTA溶液6 mL。滴定反應如下:Cu2+ + H2Y2- = CuY2- + 2H+
寫出計算CuSO4·5H2O質量分數的表達式ω= _____________________________ ;
下列操作會導致CuSO4·5H2O含量的測定結果偏高的是_____________。
a.未干燥錐形瓶
b.滴定終點時滴定管尖嘴中產生氣泡
c.未除凈可與EDTA反應的干擾離子
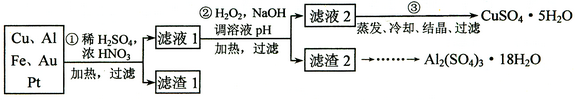
信息時代產生的大量電子垃圾對環境構成了極大的威脅。某“變廢為寶”學生探究小組將一批廢棄的線路板簡單處理后,得到含70%Cu、25%Al、4%Fe及少量Au、Pt等金屬的混合物,并設計出如下制備硫酸銅和硫酸鋁晶體的路線:

請回答下列問題:
⑴ 第①步Cu與酸反應的離子方程式為___________________________________;
⑵ 第②步加H2O2的作用是把Fe2+氧化為Fe3+,使用H2O2的優點是___________________;
⑶ 用第③步所得CuSO4·5H2O制備無水CuSO4的方法是____________________________(填儀器名稱和操作方法)。
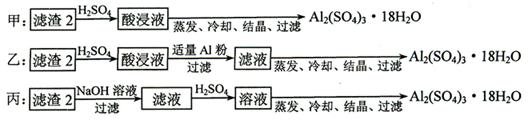
⑷ 由濾渣2制取Al2(SO4)3·18H2O ,探究小組設計了三種方案:

上述三種方案中,______方案不可行,從原子利用率角度考慮,_______方案更合理。
⑸ 探究小組用滴定法測定CuSO4·5H2O (Mr=250)含量。取a g試樣配成100 mL溶液,每次取20.00 mL,消除干擾離子后,用c mol· L-1 EDTA(H2Y2-)標準溶液滴定至終點,平均消耗EDTA溶液6 mL。滴定反應如下:Cu2+ + H2Y2- = CuY2- + 2H+
在往滴定管中裝入標準液之前,滴定管應該先經過 ,再用水清洗干凈,
然后再 ,方可裝入標準液。排除酸式滴定管尖嘴處氣泡的方法是 。在滴定時, 手操作滴定管活塞。
(6)寫出計算CuSO4·5H2O質量分數的表達式(要求帶單位)ω= _____________ ;
(7)下列操作會導致CuSO4·5H2O含量的測定結果偏高的有_____________。
a.未干燥錐形瓶
b.滴定終點時滴定管尖嘴中產生氣泡 ks5u
c.未除凈可與EDTA反應的干擾離子
d.讀取滴定管中待測液的初始體積時仰視
取一定量的Fe、Cu的混合物粉末,平均分成五等份,分別向每一份中加入一定量的稀硝酸,實驗中收集到的NO氣體(惟一還原產物)的體積及所得剩余物的質量記錄如下(所有體積均在標準狀況下測定):
| 實驗序號 | 1 | 2 | 3 | 4 | 5 |
| 硝酸溶液體積 | 100 mL | 200 mL | 300 mL | 400 mL | 500 mL |
| 剩余固體的質量 | 17.2 g | 8 g | 0 g | 0 g | 0 g |
| 氣體體積 | 2.24 L | 4.48 L | 6.72 L | 7.84 L | 7.84 L |
(1)該實驗中所用稀硝酸的物質的量濃度為__________。
(2)第1次實驗后剩余固體為__________,第2次實驗后剩余固體為________。(均填寫化學式)
(3)實驗中每次所取混合物中銅的質量為________。
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com