
題目列表(包括答案和解析)
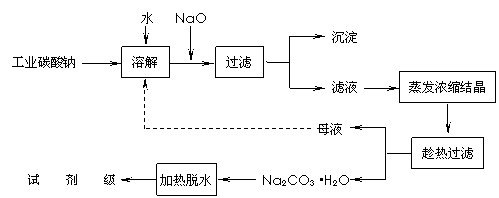
工業碳酸鈉(純度約為98%)中常含有Ca2+、Mg2+、Fe3+、Clˉ和SO42ˉ等雜質,為了提純工業碳酸鈉,并獲得試劑級碳酸鈉的工藝流程圖如下:
 |
 |
![]() (1)加入NaOH溶液時發生的離子反應方程式為 ▲ 、 ▲ 。
(1)加入NaOH溶液時發生的離子反應方程式為 ▲ 、 ▲ 。
(2)熱的Na2CO3溶液有較強的去油污能力,其原因是(用離子方程式及必要的文字加以解釋) ▲ 。
(3)“趁熱過濾”時的溫度應控制在 ▲ 。
(4)已知:Na2CO3·10 H2O(s)=Na2CO3(s)+10 H2O(g) △H=+532.36kJ·mol—1
Na2CO3·10 H2O(s)=Na2CO3·H2O(s)+9 H2O(g) △H=+473.63kJ·mol—1
寫出Na2CO3·H2O脫水反應的熱化學方程式 ▲ 。
(5)有人從“綠色化學”角度設想將“母液”沿流程圖中虛線所示進行循環使用。請你分析實際生產中是否可行 ▲ ,其理由是 ▲ 。
工業碳酸鈉(純度約為98%)中常含有Ca2+、Mg2+、Fe3+、Clˉ和SO42ˉ等雜質,為了提純工業碳酸鈉,并獲得試劑級碳酸鈉的工藝流程圖如下:
 |
 |
(1)加入NaOH溶液時發生的離子反應方程式為 ▲ 、 ▲ 。
(2)熱的Na2CO3溶液有較強的去油污能力,其原因是(用離子方程式及必要的文字加以解釋) ▲ 。
(3)“趁熱過濾”時的溫度應控制在 ▲ 。
(4)已知:Na2CO3·10 H2O(s)=Na2CO3(s)+10 H2O(g) △H=+532.36kJ·mol—1
Na2CO3·10 H2O(s)=Na2CO3·H2O(s)+9 H2O(g) △H=+473.63kJ·mol—1
寫出Na2CO3·H2O脫水反應的熱化學方程式 ▲ 。
(5)有人從“綠色化學”角度設想將“母液”沿流程圖中虛線所示進行循環使用。請你分析實際生產中是否可行 ▲ ,其理由是 ▲ 。
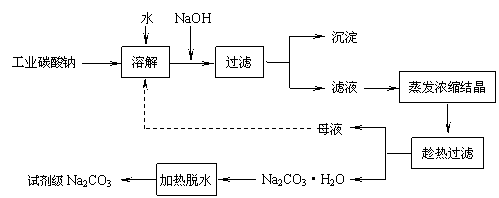
工業碳酸鈉(純度約為98%)中常含有Ca2+、Mg2+、Fe3+、Clˉ和SO42ˉ等雜質,為了提純工業碳酸鈉,并獲得試劑級碳酸鈉的工藝流程圖如下:
 |
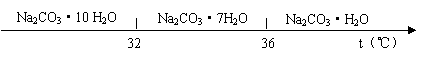 |
(1)加入NaOH溶液時發生的離子反應方程式為 ▲ 、 ▲ 。
(2)熱的Na2CO3溶液有較強的去油污能力,其原因是(用離子方程式及必要的文字加以解釋) ▲ 。
(3)“趁熱過濾”時的溫度應控制在 ▲ 。
(4)已知:Na2CO3·10 H2O(s)=Na2CO3(s)+10 H2O(g) △H=+532.36kJ·mol—1
Na2CO3·10 H2O(s)=Na2CO3·H2O(s)+9 H2O(g) △H=+473.63kJ·mol—1
寫出Na2CO3·H2O脫水反應的熱化學方程式 ▲ 。
(5)有人從“綠色化學”角度設想將“母液”沿流程圖中虛線所示進行循環使用。請你分析實際生產中是否可行 ▲ ,其理由是 ▲ 。
碳酸鈉是造紙、玻璃、紡織、制革等行業的重要原料。工業碳酸鈉(純度約98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO![]() 等雜質,提純工藝路線如下:
等雜質,提純工藝路線如下:
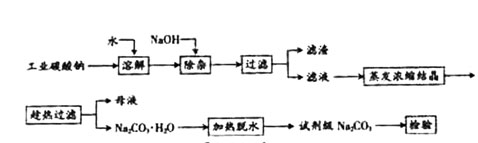
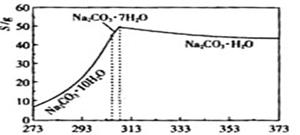 已知碳酸鈉的溶解度(S)隨溫度變化的曲線如下圖所示:
已知碳酸鈉的溶解度(S)隨溫度變化的曲線如下圖所示:
回答下列問題:
(1)濾渣的主要成分為 。
(2)“趁熱過濾”的原因是 。
(3)若在實驗室進行“趁熱過濾”,可采取的措施是 (寫出1種)。
(4)若“母液”循環使用,可能出現的問題及其原因是 。
(5)已知:
Na2CO3·10H2O(s)=Na2CO3(s)+10H2O(g) ΔH1= +532.36 kJ·mol-1
Na2CO3·10H2O(s)=Na2CO3·H2O(s)+9H??2O(g) ΔH1= +473.63 kJ·mol-1
寫出Na2CO3·H2O脫水反應的熱化學方程式 。
(12分)碳酸鈉是造紙、玻璃、紡織、制革等行業的重要原料。工業碳酸鈉(純度約98%)中含有Ca2+、Mg2+、Fe3+、Cl—和SO![]() 等雜質,提純工藝路線如下:已知碳酸鈉的溶解度(S)隨溫度變化的曲線如下圖所示。
等雜質,提純工藝路線如下:已知碳酸鈉的溶解度(S)隨溫度變化的曲線如下圖所示。
回答下列問題:
(1)濾渣的主要成分為 。
(2)“趁熱過濾”的原因是 。
(3)若“母液”循環使用,可能出現的問題及其原因是 。
(4)已知:Na2CO3·10H2O(s)=Na2CO3(s)+10H2O(g) ΔH1=+532.36 kJ·mol-1
Na2CO3·10H2O(s)=Na2CO3·H2O(s)+9H2O(g) ΔH1=+473.63kJ·mol-1
寫出Na2CO3·H2O脫水反應的熱化學方程式 。
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com