
題目列表(包括答案和解析)

| ||
| ||
硅單質及其化合物應用范圍很廣。請回答下列問題:
(1)制備硅半導體材料必須先得到高純硅。
三氯甲硅烷(SiHCl3)還原法是當前制備高純硅的主要方法,生產過程示意圖如下:
①寫出由純SiHCl3制備高純硅的化學反應方程式 。
②整個制備過程必須嚴格控制無水無氧。SiHCl3遇水劇烈反應生成H2SiO3、HCl和另一種物質,寫出配平的化學反應方程式 ;
H2還原SiHCl3過程中若混入O2,可能引起的后果是
。
(2)下列有關硅材料的說法正確的是 (填字母)。
| A.碳化硅化學性質穩定,可用于生產耐高溫水泥 |
| B.氮化硅硬度大、熔點高,可用于制作高溫陶瓷和軸承 |
| C.高純度的二氧化硅可用于制造高性能通訊材料——光導纖維 |
| D.普通玻璃是由純堿、石灰石和石英砂制成的,其熔點很高 |
硅單質及其化合物應用范圍很廣。請回答下列問題:
(1)制備硅半導體材料必須先得到高純硅。三氯甲硅烷(SiHCl3)還原法是當前制備高純硅的主要方法,生產過程示意圖如下:
![]()
①寫出由純SiHCl3制備高純硅的化學反應方程式 。
②整個制備過程必須嚴格控制無水無氧。SiHCl3遇水劇烈反應生成H2SiO3、HCl和另一種物質,寫出配平的化學反應方程式 ;H2還原SiHCl3過程中若混入O2,可能引起的后果是 。
(2)下列有關硅材料的說法正確的是 (填字母)。
A.碳化硅化學性質穩定,可用于生產耐高溫水泥
B.氮化硅硬度大、熔點高,可用于制作高溫陶瓷和軸承
C.高純度的二氧化硅可用于制造高性能通訊材料——光導纖維
D.普通玻璃是由純堿、石灰石和石英砂制成的,其熔點很高
E.鹽酸可以與硅反應,故采用鹽酸為拋光液拋光單晶硅
(3)硅酸鈉水溶液俗稱水玻璃。取少量硅酸鈉溶液于試管中,逐滴加入飽和氯化銨溶液,振蕩。寫出實驗現象并給予解釋 。
(10分)硅單質及其化合物應用范圍很廣。請回答下列問題:
(1)制備硅半導體材料必須先得到高純硅。三氯甲硅烷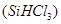 還原法是當前制備高純硅的主要方法,生產過程示意圖如下:
還原法是當前制備高純硅的主要方法,生產過程示意圖如下:
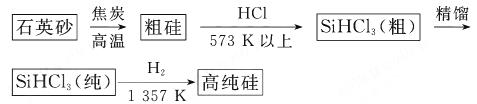
①寫出由純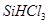 制備高純硅的化學方程式: 。
制備高純硅的化學方程式: 。
②整個制備過程必須嚴格控制無水無氧。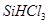 遇水劇烈反應生成
遇水劇烈反應生成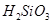 、HCl和另一種物質,配平后的化學反應方程式為? ;
、HCl和另一種物質,配平后的化學反應方程式為? ; 還原
還原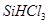 過程中若混入
過程中若混入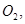 可能引起的后果是? 。
可能引起的后果是? 。
(2)下列有關硅材料的說法正確的是? (填字母)。
A.碳化硅化學性質穩定,可用于生產耐高溫水泥
B.氮化硅硬度大、熔點高,可用于制作高溫陶瓷和軸承
C.高純度的二氧化硅可用于制造高性能通訊材料——光導纖維
D.普通玻璃是由純堿、石灰石和石英砂制成的,其熔點很高
E.鹽酸可以與硅反應,故采用鹽酸為拋光液拋光單晶硅
(3)硅酸鈉水溶液俗稱水玻璃。取少量硅酸鈉溶液于試管中,逐滴加入稀硝酸,振蕩。寫出實驗現象并給予解釋 。
(10分)硅單質及其化合物應用范圍很廣。請回答下列問題:
(1)制備硅半導體材料必須先得到高純硅。三氯甲硅烷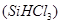 還原法是當前制備高純硅的主要方法,生產過程示意圖如下:
還原法是當前制備高純硅的主要方法,生產過程示意圖如下: 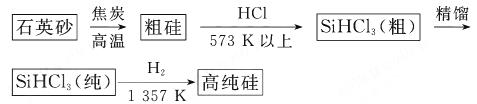
①寫出由純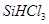 制備高純硅的化學方程式: 。
制備高純硅的化學方程式: 。
②整個制備過程必須嚴格控制無水無氧。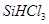 遇水劇烈反應生成
遇水劇烈反應生成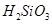 、HCl和另一種物質,配平后的化學反應方程式為? ;
、HCl和另一種物質,配平后的化學反應方程式為? ;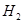 還原
還原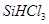 過程中若混入
過程中若混入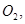 可能引起的后果是? 。
可能引起的后果是? 。
(2)下列有關硅材料的說法正確的是? (填字母)。
| A.碳化硅化學性質穩定,可用于生產耐高溫水泥 |
| B.氮化硅硬度大、熔點高,可用于制作高溫陶瓷和軸承 |
| C.高純度的二氧化硅可用于制造高性能通訊材料——光導纖維 |
| D.普通玻璃是由純堿、石灰石和石英砂制成的,其熔點很高 |
16.(1)水 濃硫酸 ;(2)檢查氣密性,將G彎管浸沒在盛有水的燒杯中,溫熱燒瓶B,觀察G管口,若有氣泡逸出,說明裝置的氣密性良好;
(3)先從A瓶逐滴滴加液體, 檢驗H2的純度;(4) ,
,  。
。
17.(1) 2Fe3++H2S
= S↓+2Fe2++2H+, Na2S+2H2O S↓+H2↑+2NaOH
S↓+H2↑+2NaOH
或S2-+2H2O S↓+H2↑+2OH-,產物NaOH可循環使用,也可得副產品H2;
S↓+H2↑+2OH-,產物NaOH可循環使用,也可得副產品H2;
(2)陽離子(Na+),鈦(或石墨);
(3)4, 正四面體。
18.(1)Al(OH)3+OH---=AlO2-+2H2O ; (2) ;
;
(3)SO2+Cl2+2H2O=H2SO4+2HCl ; (4)HCl>H2S;
(5)S2->Cl ->Na+>Al3+;(6)Cl2O7(l)+H2O(l)=2HClO4(aq);△H=-4QkJ/mol。
19. (1) ①SiHCl3+H2= Si+3HClwww. Ks5 u.com
②3SiHCl3+3H2O===H2SiO3+H2↑+3HCl;高溫下,H2遇O2發生爆炸。(2)ABCE
(3)生成白色絮狀沉淀,又刺激性氣味的氣體生成。
20.
(1)NaCl; (2)Cu+2H2SO4 CuSO4+ SO2↑+2H2O,高溫、催化劑; (3)CH3CH2OH。
CuSO4+ SO2↑+2H2O,高溫、催化劑; (3)CH3CH2OH。
21. ⑴b ; ⑵加熱褪色后的溶液,若溶液恢復紅色,則原通入氣體為SO2,若溶液不變紅,則原通入氣體是O3 ; ⑶2Fe+3Cl2 2FeCl3 Fe+S
2FeCl3 Fe+S FeS(其他合理答案均給分);
FeS(其他合理答案均給分);
⑷①H-C≡N ; ⑸16w1:(44w2-aw1)。
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com