
一定溫度下,向1.0L密閉容器中加入0.60molX(g),發生反應X(g)  Y(s)+2Z(g)△H>0測得反應物X濃度與反應時間的數據如下表
Y(s)+2Z(g)△H>0測得反應物X濃度與反應時間的數據如下表
| 反應時間t/min | 0 | 1 | 2 | 3 | 4 | 6 | 8 |
| c(X)/(mol·L-1) | 0.60 | 0.42 | 0.30 | 0.21 | 0.15 | a | 0.0375 |
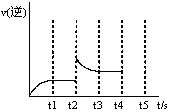
(10分)
(1)0.26mol·L-1·min-1(2分)
(2)每間隔2min,X的濃度為原來的一半(2分);0.075(2分)
(3)加入Z 增大體系的壓強(2分)
(4)ACD(2分)
解析試題分析:
3min是△c(X)=0.39mol·L-1,v(X)=0.39mol·L-1/3min=0.13mol·L-1·min-1,而2v(X)="v(Z)=" 0.26mol·L-1·min-1。
根據題中數據,可見每間隔2min,X的濃度為原來的一半;由此規律推出反應在6min時反應物的濃度a為0.075 mol·L-1
t2時刻,v逆增大,可能的因素為加入生成物Z或增大體系的壓強。
A、生成物Y是固體,未建立平衡時氣體總質量在變化,密度也在變化,達平衡是不再變化,故可以說明,正確;B、平衡常數只與溫度有關,錯誤;C、左右兩邊氣體分子質量不同,只有平衡時氣體的平均相對分子質量不隨時間而變化,正確;D、Y的量不在變化,達到平衡,正確;E、2倍的Z的生成速率等于X的消耗速率才是平衡態,錯誤。
考點:本題考查化學反應速率、影響速率的因素、平衡的特征等相關知識。


 階梯計算系列答案
階梯計算系列答案科目:高中化學 來源: 題型:填空題
對于A(g)+B(g)  xC(g) ΔH 有:
xC(g) ΔH 有: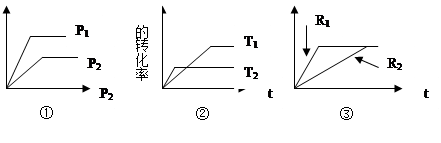
(1)①圖表明P1 P2 ,且x的值為 ;
(2)②圖表明T1 T2 ,且ΔH 0;
(3)如果③圖R1,R2分別表示改變壓強,則R1 R2 ,x的值為 ;
(4)如果③圖分別表示有無催化劑,則R1表示 催化劑。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
在一定體積的密閉容器中,進行如下反應:A(g) B(g)+C(g),其化學平衡常數K和溫度t的關系如下表所示:
| toC | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |

| 時間t/min | 0 | 1 | 2 | 4 | 8 | 16 | 20 |
| C(A)/(mol·L-1) | 10.4 | 8.6 | 7.5 | 6.6 | 5.9 | 5.5 | 5.5 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
如圖是煤化工產業鏈的一部分,試運用所學知識,解決下列問題:
(1)已知該產業鏈中某反應的平衡常數表達式為: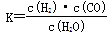 ,它所對應反應的化學方程式是
,它所對應反應的化學方程式是
_________________________________。
(2)合成甲醇的主要反應是:2H2(g)+CO(g) CH3OH(g)+90.8kJ,t℃下此反應的平衡常數為160。此溫度下,在密閉容器中開始只加入CO、H2,反應l0min后測得各組分的濃度如下:
CH3OH(g)+90.8kJ,t℃下此反應的平衡常數為160。此溫度下,在密閉容器中開始只加入CO、H2,反應l0min后測得各組分的濃度如下:
| 物質 | H2 | CO | CH3OH |
| 濃度(mol/L) | 0.2 | 0.1 | 0.4 |
| 反應 | 大氣固氮 | 工業固氮 | ||||
| 溫度/℃ | 27 | 2000 | 25 | 350 | 400 | 450 |
| K | 3.84×10-31 | 0.1 | 5×108 | 1.847 | 0.507 | 0.152 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
已知A(g)+B(g)  C(g)+D(g)反應的平衡常數和溫度的關系如下:
C(g)+D(g)反應的平衡常數和溫度的關系如下:
| 溫度/℃ | 700 | 900 | 830 | 1000 | 1200 |
| 平衡常數 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
 A(g)+B(g)的平衡常數的值為___________________。
A(g)+B(g)的平衡常數的值為___________________。 2P(g)+Q(s)反應,按下表數據投料,反應達到平衡狀態,測得體系壓強升高,簡述該反應的平衡常數與溫度的變化關系:__________________________________________________________________________________。
2P(g)+Q(s)反應,按下表數據投料,反應達到平衡狀態,測得體系壓強升高,簡述該反應的平衡常數與溫度的變化關系:__________________________________________________________________________________。| 物 質 | M | N | P | Q |
| 起始投料/mol | 2 | 1 | 2 | 0 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
鋼鐵是21世紀用途最廣的結構材料和功能材料。其成分主要是Fe和少量C。
(1)工業上在煉鐵高爐中用CO熱還原Fe2O3冶煉鐵。寫出該反應的化學方程式并用單線橋表示電子轉移的方向和數目 。
(2)鐵鎂合金是目前已發現的儲氫密度最高的儲氫材料之一,其晶胞結構如圖(黑球代表Fe,白球代表Mg)。則鐵鎂合金的化學式為 。
(3)Fe3+的電子排布式為 ;CH3+微粒的中心原子雜化軌道類型為 ;
(4)向一定量的FeCl3溶液中加入適量KSCN溶液,溶液變紅色。該反應體系中存在化學平衡 (用反應式表示);向上述紅色溶液中加入Mg(OH)2固體,可觀察到溶液紅色變淺,有紅褐色沉淀析出。試用平衡移動原理解釋該現象 。(不考慮SCN—與Mg2+反應)
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
將 4 mol A 氣體和 2 mol B 氣體在 2 L 的容器中混合并在一定條件下發生如下反應:2A(g)+B(g) 2C(g),若經 2 s(秒)后測得C 的濃度為 0.6 mol·L-1 ,則:① 用物質 A 表示的反應的平均速率 ② 2 s 時物質 B 的濃度為 。
2C(g),若經 2 s(秒)后測得C 的濃度為 0.6 mol·L-1 ,則:① 用物質 A 表示的反應的平均速率 ② 2 s 時物質 B 的濃度為 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
在一體積為10 L的容器中,通過一定量的CO和H2O,850 ℃時發生反應:
CO(g)+H2O(g)  CO2(g)+H2(g)
CO2(g)+H2(g)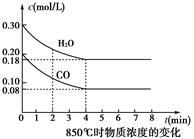
(1)CO和H2O濃度變化如圖,則0~4 min的平均反應速率v(CO)=______mol·L-1·min-1。
(2)如圖中4~5min之間該反應________(填“是”或“否”)處于平衡狀態,判斷理由________________________________________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:問答題
(18分)鈦被譽為“二十一世紀的金屬”,用途廣泛。按下圖所示組成的產業鏈可以大大提高資源利用率并能減少環境污染。請回答下列問題:
(1)已知中FeTiO3元素的化合價為+3,鈦鐵礦經氯化法得到四氯化鈦的過程中________元素被氧化,每生產1. 9kgTiCl4消耗Cl2在標準狀況下的體積為________L。
則金屬Mg還原TiCl4制取金屬Ti (s)的熱化學方程式為___________.
(3)某化學興趣小組探究外界條件對合成甲醇反應的影響。
①在300℃時,向體積為1L的密閉容器中加入2mol H2和1mol CO,CO和CH3OH(g)的濃度隨時間變化如圖所示。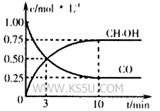
則從反應開始到建立平衡,v(H2)為___________ ;
該溫度下 的化學平衡常
的化學平衡常
數為___________ 。
。
②在其它條件不變,只改變其中的一個條件,該小組同學
根據實驗繪制如下圖像,其中與事實相符的是為___________(填
序號)。
(4)電解飽和食鹽水是氯堿工業的基礎。
①電解飽和食鹽水的離子方程式為為___________ 。
②電解時用鹽酸控制陽極區溶液的pH在2~3,鹽酸的作用為為___________。(用必要的離子方程式和文字說明)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com