
有H、D、T三種原子,各自可形成雙原子分子H2、D2、T2,請填寫下列各題。
(1)標準狀況下,它們的密度之比為________。
(2)相同物質的量的三種單質中,質子數之比為________。
(3)各1 g三種單質中,它們的質子數之比為________。
(4)同溫同壓下,1 L各單質氣體中所含電子數之比為________。
科目:高中化學 來源: 題型:填空題
下表列出前20號元素中的某些元素性質的一些數據:
| 元素 性質 | A | B | C | D | E | F | G | H | I | J |
| 原子半徑 (10-10m) | 1.02 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 1.17 |
| 最高價態 | +6 | +1 | - | +3 | +4 | +5 | +7 | +1 | +5 | +4 |
| 最低價態 | -2 | - | -2 | - | -4 | -3 | -1 | - | -3 | -4 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
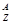 X表示原子:
X表示原子:
(1)中性原子的中子數N=______。
(2)AXn+共有x個電子,則該陽離子的中子數N=______。
(3)AXn-共有x個電子,則該陰離子的中子數N=______。
(4)12C16O2分子中的中子數N=________。
(5)A2-原子核內有x個中子,其質量數為m,則n g A2-所含電子的物質的量為________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
最新報道,我國科學家通過與多個國家進行科技合作,成功研發出銫(Cs)原子噴泉鐘,使我國時間頻率基準的精度從30萬年不差1秒提高到600萬年不差1秒,標志著我國時間頻率基準研究進入世界先進行列。已知銫位于元素周期表中第六周期第ⅠA族,根據銫在元素周期表中的位置,推斷下列內容:
(1)銫的原子核外共有________層電子,最外層電子數為________,銫的原子序數為________。
(2)銫單質與水劇烈反應,放出________色氣體,同時使紫色石蕊試液顯________色,因為____________________(寫出化學方程式)。
(3)預測銫單質的還原性比鈉單質的還原性________(填“弱”或“強”)。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
已知某物質主要成分的化學式為XY2,X原子的結構示意圖為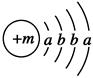 ,X的陽離子與Y的陰離子的電子層結構相同。元素Z、W均為短周期元素,它們原子的最外層電子數均是其電子層數的2倍,Z與Y相鄰且Z、W能形成一種WZ2型分子。
,X的陽離子與Y的陰離子的電子層結構相同。元素Z、W均為短周期元素,它們原子的最外層電子數均是其電子層數的2倍,Z與Y相鄰且Z、W能形成一種WZ2型分子。
(1)m=________,該物質主要成分的化學式為________。
(2)Z、W元素的名稱為________、________。
(3)下列說法正確的是________。
| A.XY2和WZ2都為離子化合物 |
| B.XY2分子中僅含離子鍵,WZ2中僅含極性共價鍵 |
| C.H2Z比HY的穩定性強 |
| D.X的陽離子比Y的陰離子半徑大 |

查看答案和解析>>
科目:高中化學 來源: 題型:填空題
短周期元素A、B、C、D、E、F六種元素,它們的原子序數由A到F依次增大。在周期表中,A的原子半徑最小。B元素的原子最外層電子數是內層電子數的兩倍,C為地殼中含量最多的元素,D是原子半徑最大的短周期主族元素,D單質燃燒時呈現黃色火焰,D的單質在高溫下與C的單質充分反應,可以得到與E單質顏色相同的淡黃色固態化合物。D與F形成的離子化合物DF是常用的調味品。試根據以上敘述回答:
(1)元素名稱:
A________、B________、C________、D________。
(2)E在元素周期表中的位置:_________________________________________________。
(3)F離子結構示意圖:_____________________________________________________。
(4)A、B組成的最簡單化合物的名稱是____________________________________________。
(5)C、D按原子個數比1∶1組成的一種化合物與水發生反應的化學方程式為___________________________________________________________。
(6)能說明E的非金屬性比F的非金屬性____(填“強”或“弱”)的事實是________(舉一例)。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
A、B、C為短周期元素,在周期表中所處的位置如圖所示。A、C兩元素的原子核外電子數之和等于B原子的質子數。B原子核內質子數和中子數相等。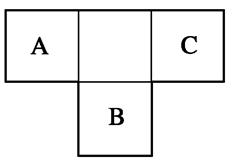
(1)A、B、C三種元素的名稱分別為__________、________、________。
(2)B位于元素周期表中第________周期第________族。
(3)C的原子結構示意圖為________,C的單質與H2反應的化學方程式為_______________________________________________________________________。
(4)寫出A的氣態氫化物與B的最高價氧化物對應水化物反應的化學方程式__________________________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
利用化石燃料開采、加工過程產生的H2S廢氣制取氫氣,既價廉又環保。
(1)工業上可用組成為K2O·M2O3·2RO2·nH2O的無機材料純化制取的氫氣。
①已知元素M、R均位于元素周期表中第三周期,兩種元素原子的質子數之和為27,則R的原子結構示意圖為________。
②常溫下,不能與M單質發生反應的是________(填序號)。
a.CuSO4溶液 b.Fe2O3 c.濃硫酸 d.NaOH溶液 e.Na2CO3固體
(2)利用H2S廢氣制取氫氣的方法有多種。
①高溫熱分解法
已知:H2S(g) H2(g)+
H2(g)+ S2(g)
S2(g)
在恒容密閉容器中,控制不同溫度進行H2S分解實驗。以H2S起始濃度均為c mol·L-1測定H2S的轉化率,結果見下圖。圖中a為H2S的平衡轉化率與溫度關系曲線,b曲線表示不同溫度下反應經過相同時間且未達到化學平衡時H2S的轉化率。據圖計算985℃時H2S按上述反應分解的平衡常數K=________;說明隨溫度的升高,曲線b向曲線a逼近的原因:____________________________________。
②電化學法
該法制氫過程的示意圖如下。反應池中反應物的流向采用氣、液逆流方式,其目的是______________________________;
反應池中發生反應的化學方程式為____________________。反應后的溶液進入電解池,電解總反應的離子方程式為_______________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
A、B、C、D、E、F均為短周期元素,且原子序數依次增大,A是原子半徑最小的元素,B的最高價氧化物的水化物可與其氫化物反應形成離子化合物甲;A與D可以按照原子個數比4∶1形成化合物乙,且乙分子中含有18個電子,E與B同主族,C的陽離子與F的陰離子相差一個電子層,且可形成離子個數比為2∶1的離子化合物丙。
(1)D的原子結構示意圖為 ________ ,丙的電子式為___________ ,E在周期表中的位置為 。
(2)下列說法正確的有 。
①化合物乙分子中只含有極性共價鍵
②C、D、E、F原子半徑由大到小的順序為C>D>E>F
③B、E形成的氫化物中,B的氫化物更穩定
④化合物甲和化合物丙都含有離子鍵和共價鍵
(3)將F燃燒的產物通入BaCl2和HNO3的混合溶液中,生成白色沉淀并放出無色氣體,請用一個離子方程式表示該反應 __________________ 。
(4)寫出一個由以上元素構成的10電子微粒與18電子微粒反應的離子方程式 ____________________________ 。
(5)甲溶液顯 (填“酸性”、“堿性”或“中性”),原因是 (用離子方程式表示)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com