
氫化熱是指一定條件下,1 mol 不飽和化合物加氫時放出的熱量。表中是環己烯( )、環己二烯(
)、環己二烯( )和苯的氫化熱數據。
)和苯的氫化熱數據。
| 化合物 | 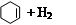  | 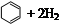  | 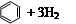  |
| 氫化熱 (kJ/mol) | 119.7 | 232.7 | 208.4 |
 轉變為
轉變為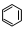 時放熱
時放熱 科目:高中化學 來源: 題型:單選題
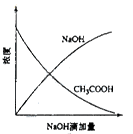
下列各圖有關量的變化趨勢中錯誤的是
A B C D
| A.圖A為向鹽酸中滴加NaOH發生中和反應過程中溶液溫度的變化趨勢 |
| B.圖B為向醋酸中滴加NaOH發生中和反應過程中各物質濃度的變化趨勢 |
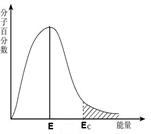
| C.圖C中能量≥Ec的分子稱為活化分子,E為分子平均能量,則活化能為Ec-E |
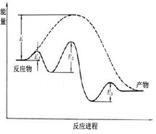
| D.圖D為未加入催化劑和加入催化劑的反應進程中的能量變化 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
含20.0 g NaOH的稀溶液與稀鹽酸完全反應時,放出28.7 kJ的熱量,表示該反應的熱化學方程式正確的是
A.NaOH(aq)+HCl(aq)=NaCl(aq)+H20(l) =" +28.7" kJ·mol-1 =" +28.7" kJ·mol-1 |
B.NaOH(aq)+HCl(aq)=NaCl(aq)+H20(l) =" -28.7" kJ·mol-1 =" -28.7" kJ·mol-1 |
C.NaOH(aq)+HCl(aq)=NaCl(aq)+H20(l) =" +57.4" kJ·mol-1 =" +57.4" kJ·mol-1 |
D.NaOH(aq)+HCl(aq)=NaCl(aq)+H20(l) =" -57.4" kJ·mol-1 =" -57.4" kJ·mol-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列有關熱化學方程式的敘述中,正確的是
| A.含20.0g NaOH的稀溶液與稀鹽酸完全中和,放出28.7kJ的熱量,則表示該反應中和熱的熱化學方程式為NaOH(aq)+HCl(aq)=NaC1(aq)+H2O(1) ΔH=+57.4kJ/mo1 |
| B.已知C(石墨,s)=C(金剛石,s) ΔH>0,則石墨比金剛石穩定 |
| C.已知2H2(g)+O2(g)=2H2O(g) ΔH =—483.6kJ/mol,則H2燃燒熱為241.8kJ/mol |
| D.己知2C(s)+2O2(g)=2CO2(g) ΔH 1;2C(s)+O2(g)="2CO(g)" ΔH 2;則ΔH 1<ΔH 2 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
氫氟酸(HF)是一種弱酸。25℃時,向20mL0.1mol/L氫氟酸中加入VmL 0.1mol/LNaOH溶液充分反應。已知:
HF(aq)+OH-(aq)=F-(aq)+H2O(l) △H=-67.7kJ/mol
H+(aq)+OH-(aq)=H2O(l) △H=-57.3kJ/mol
根據題意,下列判斷或結論正確的是
| A.氫氟酸的電離過程是吸熱的 |
| B.當V=20時,溶液中:c(F-)<c(Na+)=0.1mol/L |
| C.當V<20時,溶液中離子濃度關系可能為:c(Na+)=c(F-) |
| D.當V>20時,溶液中離子濃度關系一定為:c(Na+)>c(F-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
X、Y、Z、R、W是5種短周期元素,原子序數依次增大,它們可組成離子化合物Z2Y和共價化合物RY3、XW4,已知Y、R同主族,Z、R、W同周期。下列說法不正確的是( )
| A.原子半徑:Z>R>W |
| B.X2W6分子中各原子均滿足8電子結構 |
| C.氣態氫化物的穩定性:HmW>HnR |
| D.Y、Z形成的化合物中只可能存在離子鍵 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
“天宮一號”目標飛行器與“神舟九號”載人飛船的交會對接,標志著我國具備了建設空間站的基本能力。下列有關說法正確的是
| A.火箭升空的動力主要來源于化學能 |
| B.“神舟九號”飛船的太陽能帆板將太陽能直接轉換為動能 |
| C.“天宮一號”中的氫氧燃料電池將電能轉換為化學能 |
| D.“天宮一號”利用太陽能將水加熱分解為氫氣和氧氣 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列有關反應熱的說法正確的是( )
| A.任何強酸與強堿反應生成1 mol H2O的過程中,放出的熱量均相同 |
| B.等量的硫蒸氣和硫固體分別完全燃燒,后者放出熱量多 |
| C.對于任何一個吸熱反應,使用催化劑后,ΔH將降低 |
| D.已知:O=O鍵鍵能為a kJ/ mol、H-H鍵鍵能為b kJ/ mol、水蒸氣中H-O鍵能為c kJ/ mol。又知:H2O(g)= H2O(l)ΔH=" -d" kJ/ mol。則反應2H2 (g) + O2(g) = 2H2O(l) 的ΔH為:(a+2b-4c-2d)kJ/ mol |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
25 ℃、101 kPa下,碳、氫氣、甲烷和葡萄糖的燃燒熱依次是ΔH=-393.5 kJ·mol-1、ΔH=-285.8 kJ·mol-1、ΔH=-890.3 kJmol-1、ΔH=-2 800 kJ·mol-1,則下列熱化學方程式正確的是 ( )。
A.C(s)+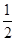 O2(g)===CO(g) ΔH=-393.5 kJ·mol-1 O2(g)===CO(g) ΔH=-393.5 kJ·mol-1 |
| B.2H2(g)+O2(g)===2H2O(l) ΔH=-571.6 kJ·mol-1 |
| C.CH4(g)+2O2(g)===CO2(g)+2H2O(g)ΔH=-890.3 kJ·mol-1 |
D.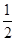 C6H12O6(s)+3O2(g)===3CO2(g)+3H2O(g)ΔH=-1 400 kJ·mol-1 C6H12O6(s)+3O2(g)===3CO2(g)+3H2O(g)ΔH=-1 400 kJ·mol-1 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com