
甲醇可通過將煤氣化過程中生成的CO和H2在一定條件下,發生如下反應制得:CO(g)+2H2(g) CH3OH(g)。請根據圖示回答下列問題:
CH3OH(g)。請根據圖示回答下列問題: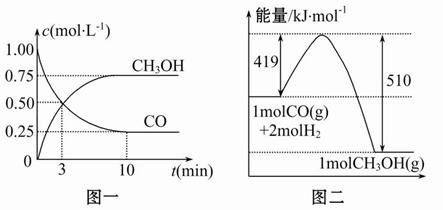
(1)從反應開始到平衡,用H2濃度變化表示平均反應速率v(H2)= ,CO的轉化率為 。
(2)該反應的平衡常數表達式為 ,溫度升高,平衡常數 (填“增大”、“減小”或“不變”)。
(3)若在一體積可變的密閉容器中充入1 mol CO、2 mol H2和1 mol CH3OH,達到平衡時測得混合氣體的密度是同溫同壓下起始的1.6倍,則加入各物質后該反應向 (填“正”、“逆”)反應方向移動,理由是 。
 寒假大串聯黃山書社系列答案
寒假大串聯黃山書社系列答案科目:高中化學 來源: 題型:填空題
加0.1 mol MnO2粉末于50 mL過氧化氫(H2O2,ρ=1.1 g· mL-1)中,在標準狀況下放出氣體的體積和時間的關系如圖所示。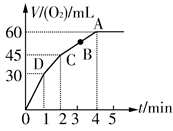
(1)實驗時放出氣體的總體積是_____________________________。
(2)放出一半氣體所需時間為_______________________________。
(3)反應放出氣體總體積的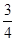 所需的時間約為__________________
所需的時間約為__________________
(4)A、B、C、D各點反應速率快慢的順序為____________________
(5)解釋反應速率變化的原因___________________________________________________
(6)計算H2O2的初始物質的量濃度____________________
(7)求反應到2 min時,H2O2的質量分數_________________________
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
在2 L密閉容器中,800℃時反應2NO(g)+O2(g) 2NO2(g)體系中,n(NO)隨時間的變化如表:
2NO2(g)體系中,n(NO)隨時間的變化如表:
| 時間/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |

查看答案和解析>>
科目:高中化學 來源: 題型:填空題
合成氨工業的核心反應是:N2(g)+3H2(g)  2NH3(g) ΔH=Q kJ·mol-1,能量變化如下圖,回答下列問題:
2NH3(g) ΔH=Q kJ·mol-1,能量變化如下圖,回答下列問題: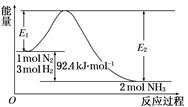
(1)在反應體系中加入催化劑,反應速率增大,E1和E2的變化是:E1________,E2________(填“增大”、“減小”或“不變”)。
(2)在500℃、2×107Pa和催化劑條件下向一密閉容器中充入0.5 mol N2和1.5 mol H2,充分反應后,放出的熱量________ 46.2 kJ(填“<”、“>”或“=”)。
(3)關于該反應的下列說法中,正確的是________。
A.ΔH>0,ΔS>0 B.ΔH>0,ΔS<0
C.ΔH<0,ΔS>0 D.ΔH<0,ΔS<0
(4)將一定量的N2(g)和H2(g)放入1 L密閉容器中,在500℃、2×107Pa下達到平衡,測得N2為0.10 mol,H2為0.30 mol,NH3為0.10 mol。計算該條件下達到平衡時H2轉化為NH3的轉化率________。若升高溫度,K值變化________(填“增大”、“減小”或“不變”)。
(5)在上述(4)反應條件的密閉容器中,欲提高合成氨中H2的轉化率,下列措施可行的是________(填字母)。
A.向容器中按原比例再充入原料氣
B.向容器中再充入惰性氣體
C.改變反應的催化劑
D.分離出氨氣
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
能源問題是人類社會面臨的重大課題,甲醇是未來重要的綠色能源之一。以CH4和H2O為原料,通過下列反應來制備甲醇。
Ⅰ.CH4(g)+H2O(g)=CO(g)+3H2(g)ΔH=+206.0 kJ/mol
Ⅱ.CO(g)+2H2(g)=CH3OH(g)ΔH=-129.0 kJ/mol
(1)CH4(g)與H2O(g)反應生成CH3OH(g)和H2(g)的熱化學方程式為_____。
(2)將1.0 mol CH4和2.0 mol H2O(g)通入容積為100 L的反應室,在一定條件下發生反應Ⅰ,測得在一定的壓強下CH4的轉化率與溫度的關系如圖。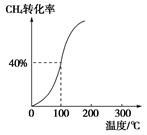
①假設100 ℃時達到平衡所需的時間為5 min,則用H2表示該反應的平均反應速率為________;
②100 ℃時反應Ⅰ的平衡常數為________。
(3)在壓強為0.1 MPa、溫度為300 ℃條件下,將1.0 mol CO與2.0 mol H2的混合氣體在催化劑作用下發生反應Ⅱ生成甲醇,平衡后將容器的容積壓縮到原來的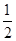 ,其他條件不變,對平衡體系產生的影響是________(填字母序號)。
,其他條件不變,對平衡體系產生的影響是________(填字母序號)。
| A.c(H2)減小 |
| B.正反應速率加快,逆反應速率減慢 |
| C.CH3OH的物質的量增加 |
D.重新平衡時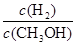 減小 減小 |
 CO(g)+2H2(g),此反應能自發進行的原因是:___。
CO(g)+2H2(g),此反應能自發進行的原因是:___。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
甲醇是重要的化學工業基礎原料和清潔液體燃料。工業上可利用CO或CO2來生產燃料甲醇。已知甲醇制備的有關化學反應以及在不同溫度下的化學反應平衡常數如下表所示:
(1)反應②是 (填“吸熱”或“放熱”)反應。
(2)某溫度下反應①中H2的平衡轉化率(a)與體系總壓強(P)的關系,如圖所示。則平衡狀態由A變到B時,平衡常數K(A) K(B)(填“>”、“<”或“=”)。據反應①與②可推導出K1、K2與K3之間的關系,則K3= (用K1、K2表示)。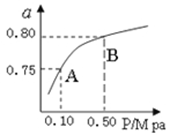
(3)在3 L容積可變的密閉容器中發生反應②,已知c(CO)與反應時間t變化曲線Ⅰ如圖所示,若在t0時刻分別改變一個條件,曲線Ⅰ變為曲線Ⅱ和曲線Ⅲ。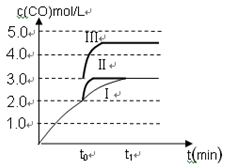
當曲線Ⅰ變為曲線Ⅱ時,改變的條件是 。
當曲線Ⅰ變為曲線Ⅲ時,改變的條件是 。
(4)甲醇燃料電池有著廣泛的用途,同時Al-AgO電池是應用廣泛的魚雷電 池,其原理如圖所示。該電池的負極反應式是 。
(5)一定條件下甲醇與一氧化碳反應可以合成乙酸。通常狀況下,將a mol/L的醋酸與b mol/LBa(OH)2溶液等體積混合,反應平衡時,2c(Ba2+)= c(CH3COO-),用含a和b的代數式表示該混合溶液中醋酸的電離常數為 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
黨的十八大報告中首次提出“美麗中國”的宏偉目標。節能減排是中國轉型發展的必經之路,工業生產中聯合生產是實現節能減排的重要措施,下圖是幾種工業生產的聯合生產工藝: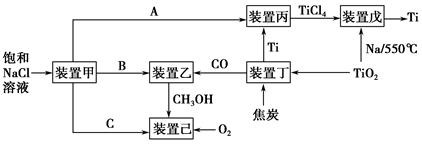
請回答下列問題:
(1)裝置甲為電解池,根據圖示轉化關系可知:A為____________(填化學式),陰極反應式為____________。
(2)裝置丙的反應物為Ti,而裝置戊的生成物為Ti,這兩個裝置在該聯合生產中并不矛盾,原因是_________________________________________________
裝置戊進行反應時需要的環境為________(填字母序號)。
A.HCl氣體氛圍中 B.空氣氛圍中 C.氬氣氛圍中 D.水中
(3)裝置乙中發生的是工業合成甲醇的反應:CO(g)+2H2(g)??CH3OH(g) ΔH<0。
①該反應在不同溫度下的化學平衡常數(K)如下表:
| 溫度/℃ | 250 | 350 |
| K | 2.041 | x |
| | c(CO) | c(H2) | c(CH3OH) |
| 0 min | 0.8 mol·L-1 | 1.6 mol·L-1 | 0 |
| 2 min | 0.6 mol·L-1 | y | 0.2 mol·L-1 |
| 4 min | 0.3 mol·L-1 | 0.6 mol·L-1 | 0.5 mol·L-1 |
| 6 min | 0.3 mol·L-1 | 0.6 mol·L-1 | 0.5 mol·L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
在450℃并有催化劑存在下,在體積為1L的密閉恒溫容器中,二氧化硫和氧氣發生如下反應:2SO2+O2 2SO3
2SO3
(1)已知:64g SO2完全轉化為SO3會放出85kJ熱量。SO2轉化為SO3的熱化學方程式是 。
(2)該反應的化學平衡常數表達式K= 。
(3)降低溫度,化學反應速度 。該反應K值將 。壓強將 。(填“增大”或“減小”或“不變”)
(4)450℃時,在一密閉容器中,將二氧化硫與氧氣混合,反應過程中SO2、O2、SO3物質的量變化如圖,反應處于平衡狀態的時間段是 。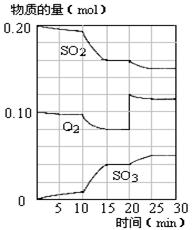
a.10-15min b.15-20min c.20-25min d.25-30min
(5)據圖判斷,10min到15min的曲線變化的原因可能是 (填寫編號)。
a.增加SO3的物質的量 b.縮小容器體積 c.降低溫度 d.催化劑
(6)在15分鐘時,SO2的轉化率是 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
某恒容容器內發生的可逆反應的化學平衡常數表達式為: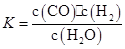 。能判斷該反應一定達到化學平衡狀態的依據是( )
。能判斷該反應一定達到化學平衡狀態的依據是( )
①容器中氣體的平均相對分子質量不隨時間而變化
②v正(H2O)=v逆(H2)
③容器中氣體的密度不隨時間而變化
④容器中氣體總質量不隨時間而變化
⑤消耗n mol H2的同時消耗n mol CO
| A.①②③ | B.①②③④ | C.② | D.①④⑤ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com