
【題目】對于可逆反應:2A(g)+B(g)2C(g)△H<0,下列各圖中正確的是( )
A.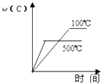
B.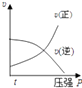
C.
D.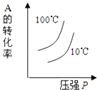
【答案】A
【解析】解:A、該反應為放熱反應,溫度升高平衡向逆反應方向移動,C的質量分數減小,故A正確;B、根據反應前后的化學計量數的大小可以看出,增大壓強平衡向正反應方向移動,正逆反應速率都增大,且V正>V逆 , 故B錯誤;
C、催化劑同等程度地改變正逆反應速率,平衡不發生移動,故C錯誤;
D、該反應為放熱反應,溫度升高平衡向逆反應方向移動,A的轉化率降低,根據反應前后的化學計量數的大小可以看出,增大壓強平衡向正反應方向移動,A的轉化率增大,本題溫度的曲線不正確,故D錯誤.
故選A.
做題時首先分析化學方程式的特征,如反應前后計量數的大小關系、反應熱等問題,
A、根據反應溫度的不同結合反應熱判斷平衡移動的方向,可判斷出C的質量分數的變化是否正確
B、根據反應前后的化學計量數的大小關系,結合壓強對反應速率的影響判斷平衡移動方向,從而判斷出正逆反應速率的變化;
C、從催化劑對平衡是否有影響來判斷濃度的變化是否正確;
D、從兩個方面考慮,一是壓強對平衡的影響,二是溫度對平衡的影響,二者結合判斷A的轉化率是否正確.


科目:高中化學 來源: 題型:
【題目】“探險隊員”﹣鹽酸,不小心走進了化學迷宮,不知怎樣走出來,因為迷宮有許多“吃人的野獸”(即能與鹽酸反應的物質或者是水溶液),鹽酸必須避開它們,否則就無法通過.
(1)在能“吃掉”鹽酸的化學反應中,屬于酸堿中和反應的有個,屬于氧化還原反應的有個,其中能“吃掉”鹽酸的鹽是(填化學式),寫出該反應的離子方程式 .
(2)在不能與鹽酸反應的物質中,屬于電解質的是(填寫物質序號,下同),屬于非電解質的是 .
(3)請你幫助它走出迷宮(用圖中物質前的序號連接起來表示所走的路線) .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】新能源的特點是資源豐富,在使用時對環境無污染或污染很小,且可以再生.下列屬于新能源的是( )
①太陽能 ②天然氣 ③地熱能④煤 ⑤生物質能⑥石油 ⑦風能 ⑧氫能.
A.①②③⑦⑧
B.①③⑤⑦⑧
C.①③⑤⑧
D.②④⑤⑥⑦
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在恒容密閉容器中通入X并發生反應:2X(g)Y(g),溫度T1、T2下X的物質的量濃度c(X)隨時間t變化的曲線如圖所示.下列敘述正確的是( ) 
A.該反應進行到M點放出的熱量大于進行到W點放出的熱量
B.T2下,在0~t1時間內,v(Y)= ![]() mol?L﹣1?min﹣1
mol?L﹣1?min﹣1
C.M點的正反應速率V正大于N點的逆反應速率V逆
D.M點時再加入一定量X,平衡后X的轉化率減小
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一定溫度下,將氣體X和氣體Y各0.16mol充入10L恒容密閉容器中,發生反應X(g)+Y(g)2Z(g)△H<0,一段時間后達到平衡,反應過程中測定的數據如下表.下列說法正確的是( )
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
A.反應前2min的平均速率v(Z)=2.0×10﹣5mol/(Lmin)
B.其他條件不變,降低溫度,反應達到新平衡前v(逆)>v(正)
C.該溫度下此反應的平衡常數K=1.44
D.其他條件不變,再充入0.2mol Z,平衡時X的體積分數增大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某小組同學以碳棒為電極電解CuCl2溶液時,發現陰極碳棒上除了有紅色物質析出外,還有少量白色物質析出.為探究陰極碳棒上的產物,同學們閱讀資料并設計了如下過程:
Ⅰ.有關資料:銅的化合物顏色性質如下
物質 | 顏色、性質 | 物質 | 顏色、性質 |
氫氧化銅Cu(OH)2 | 藍色固體不溶于水 | 硫酸銅(CuSO4) | 溶液呈藍色 |
氧化亞銅(Cu2O) | 紅色固體不溶于水 | 氯化銅(CuCl2) | 濃溶液呈綠色,稀溶液呈藍色 |
氯化亞銅(CuCl) | 白色固體不溶于水 | 堿式氯化銅 | 綠色固體不溶于水 |
Ⅱ.探究實驗:
(1)提出假設:
①紅色物質一定有銅,還可能有Cu2O;
②白色物質為銅的化合物,其化學式可能為 .
(2)實驗驗證:
取電解CuCl2溶液后的陰極碳棒,洗滌、干燥,連接下列裝置進行實驗,驗證陰極產物,
①實驗前,檢查裝置A氣密性的方法是 .
②實驗時,各裝置從左至右的連接順序為A→→→B→→
(3)觀察現象,得出結論
實驗結束后,碳棒上的白色物質變為紅色,F中物質不變色,D中出現白色沉淀,根據現象①碳棒上的紅色物質是否有Cu2O(填“是”或“否”),理由是;
②裝置(填上圖中裝置編號)中的現象說明提出假設②中的白色物質一定存在;
③寫出裝置B中發生反應的化學方程式 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列敘述正確的是( )
①其它條件不變時,縮小容器體積,平衡H2(g)+I2(g)2HI(g)不移動,體系顏色不變
②常溫下, ![]() =10﹣10的溶液中:Na+、Al3+、SO42﹣、NO3﹣可大量共存
=10﹣10的溶液中:Na+、Al3+、SO42﹣、NO3﹣可大量共存
③將pH=4的醋酸溶液稀釋后,溶液中所有離子的濃度均降低
④為確定某酸H2A是強酸還是弱酸,可測NaHA溶液的pH.若pH>7,則H2A是弱酸;若pH<7,則H2A是強酸.
A.全錯
B.只有④正確
C.①③④正確
D.①②③正確
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com