
【題目】溫度相同,濃度均為0.2molL﹣1的①(NH4)2SO4 , ②NaNO3 , ③NH4HSO4 , ④NH4NO3 , ⑤CH3COONa溶液,它們的pH由小到大的排列順序是( )
A.③①④②⑤
B.①③⑤④②
C.③②①⑤④
D.⑤②④①③
【答案】A
【解析】解:①(NH4)2SO4、④NH4NO3水解呈酸性,pH<7;③NH4HSO4電離出H+呈酸性,pH<7;②NaNO3不水解,pH=7;⑤CH3COONa水解呈堿性,pH>7,①、④比較,前者c(NH ![]() )大,水解生成c(H+)大,pH小,①③比較,后者電離出c(H+)比前者水解出c(H+)大,pH小,所以③①④②⑤,故選A.
)大,水解生成c(H+)大,pH小,①③比較,后者電離出c(H+)比前者水解出c(H+)大,pH小,所以③①④②⑤,故選A.
【考點精析】本題主要考查了弱電解質在水溶液中的電離平衡的相關知識點,需要掌握當弱電解質分子離解成離子的速率等于結合成分子的速率時,弱電解質的電離就處于電離平衡狀態;電離平衡是化學平衡的一種,同樣具有化學平衡的特征.條件改變時平衡移動的規律符合勒沙特列原理才能正確解答此題.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】下列關于S、SO2、H2SO4的敘述中,正確的是
A.硫是一種易溶于水的黃色晶體 B.SO2溶于水生成H2SO4
C.用氫氧化鈉溶液處理含有SO2的尾氣 D.濃H2SO4不穩定,光照易分解
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】中國科學家制得一種藍色鎢的氧化物(WOa),其中鎢的質量分數為0.7985.
(1)a=(保留2位小數).
(2)WOa中存在五價和六價兩種價態的鎢.則藍色鎢的氧化物中這兩種價態的鎢原子數之比為 . 將鐵錳的鎢酸鹽[(Fe,Mn)WO4]堿熔,發生如下反應(設空氣中N2、O2的體積分數分別為0,.8和0.2):4FeWO4+4Na2CO3+O2 ![]() 4Na2WO4+2Fe2O3+4CO2 ①
4Na2WO4+2Fe2O3+4CO2 ①
2MnWO4+2Na2CO3+O2 ![]() 2Na2WO4+2MnO2+2CO2 ②
2Na2WO4+2MnO2+2CO2 ②
(3)根據反應①,若反應前空氣為100L,反應后氣體為160L(氣體體積在同溫同壓下測定),則反應后所得氣體中CO2的體積分數為 .
(4)某工廠投料550mol Na2CO3制備Na2WO4 , 每反應1mol O2時,氣體就增加1.5mol,則生成物中Fe2O3與MnO2的物質的量之比為;若反應后氣體增加300mol,制得Na2WO4mol.
(5)由Na2WO4制備W的第一步反應為:Na2WO4+2HCl→H2WO4↓+2NaCl.往1L密度為1,.190g/cm3的37%的濃鹽酸加入6.030mol Na2WO4 , 恰好完全反應.將產生的沉淀過濾后,溶液中溶質只有NaCl,求該溶液中NaCl的質量分數(25℃時NaCl的溶解度為36.0g/100g水):
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】等體積的硫酸鋁、硫酸鋅、硫酸鈉溶液分別與足量氯化鋇溶液反應。若生成硫酸鋇沉淀的質量比為1:2:3,則三種硫酸鹽的物質的量濃度之比為
A. 1:2:3B. 1:3:6C. 1:3:3D. 1:6:9
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】屠呦呦1971年發現、分離、提純并用于治瘧新藥“青蒿素”,救了數千萬人的生命,青蒿素分子結構如圖.下列有關說法正確的是( ) 
A.青蒿素可溶于乙醚和水
B.青蒿素的晶體為分子晶體,化學式為C16H20O5
C.青蒿素與NaOH溶液不反應
D.青蒿素含有過氧鍵,一定條件下有氧化性
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室常用的玻璃儀器①試管;②燒杯;③量筒;④普通漏斗;⑤分液漏斗;⑥燒瓶;⑦滴管;⑧容量瓶。其中把碘水中的碘提取出來用到的儀器有 ( )
A. ②④⑥B. ②⑤C. ③⑤⑥⑧D. ②③④⑥⑦
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學小組利用如圖裝置進行某些氣體的制備和性質實驗,圖中加持裝置有省略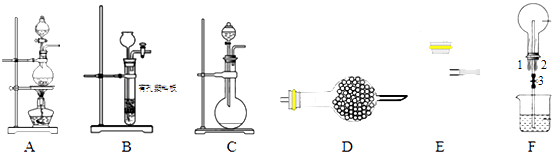
(1)為制取干燥氨氣,可將裝置C與裝置D連接,則裝置D中 的固體宜選用a.堿石灰 b.無水氯化鈣 c.五氧化二磷 d.生石灰
(2)裝置A、E、E連接可制取純凈干燥的氯氣,則兩個E裝置內的藥品依次是
(3)裝置F可用于探究氯氣和氨氣反應,實驗室打開開關1、3,關閉2,先向燒瓶中通入 , 然后關閉1、3,打開2,向燒瓶中緩慢通入一定量的另一種氣體.實驗一段時間后燒瓶內出現濃厚的白煙并在容器內壁凝結,請設計一個實驗方案鑒定該固體中的陽離子 .
(4)利用裝置A、E,可設計實驗比較氯離子和溴離子的還原性強弱,能證明結論的實驗現象是 . 若利用裝置A、E進行乙烯與溴水反應的實驗,必須對裝置A進行的改動是 .
(5)將裝置B、C分別于F相連后,進行硫化氫和二氧化硫反應的實驗,燒杯中的試劑所起的作用是 .
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com