
【題目】H2O2分解速率受多種因素影響。實驗測得70 ℃時不同條件下H2O2濃度隨時間的變化如圖所示。下列說法正確的是
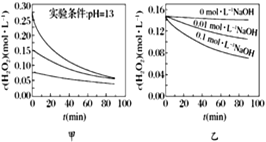
A. 圖甲表明,其他條件相同時,H2O2濃度越小,其分解速率越快
B. 圖乙表明,其他條件相同時,溶液堿性越弱,H2O2分解速率越快
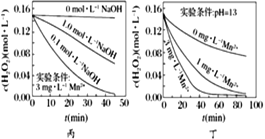
C. 圖丙表明,少量Mn2+存在時,溶液堿性越強,H2O2分解速率越快
D. 圖丁表明,堿性溶液中,Mn2+對H2O2分解速率的影響大
科目:高中化學 來源: 題型:
【題目】關于有機物的下列說法正確的是![]()
![]()
A. 在酸性條件下,![]() 的水解產物是
的水解產物是![]() 和
和![]()
B. 油脂在堿性條件下的水解反應稱為皂化反應,反應生成甘油和高級脂肪酸
C. 淀粉與纖維素通式相同,但二者不互為同分異構體
D. 鑒定蔗糖水解產物中的葡萄糖:在水解液中直接加入銀氨溶液并水浴加熱
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溶液中含有大量的下列離子:Fe3+、SO42-、Al3+和M離子,經測定Fe3+、SO42-、Al3+和M離子的物質的量之比為2:4:1:1,則M離子可能是下列中的( )
A.Na+B.OH-C.Mg2+D.Cl-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】灰錫(以粉末狀存在)和白錫是錫的兩種同素異形體。已知:
①Sn (s、白)+2HCl (aq)=SnCl2 (aq)+H2 (g);DH1
②Sn (s、灰)+2HCl (aq)=SnCl2 (aq)+H2 (g);DH2
③Sn (s、灰)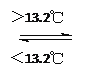 Sn (s、白);DH3=+2.1 kJ/mol
Sn (s、白);DH3=+2.1 kJ/mol
下列說法正確的是( )
A. DH1>DH2
B. 錫在常溫下以灰錫狀態存在
C. 灰錫轉化為白錫的反應是放熱反應
D. 錫制器皿長期處于低于13.2 ℃的環境中,會自行毀壞
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】按以下步驟從![]() 合成
合成![]() 。(部分試劑和反應條件已略去)
。(部分試劑和反應條件已略去)
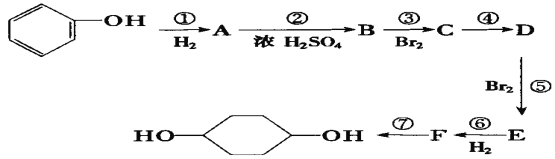
請回答下列問題:
(1)分別寫出B、D的結構簡式:B_________、D_________。
(2)反應①~⑦中屬于消去反應的是_______________。(填數字代號)
(3)如果不考慮⑥、⑦反應,對于反應⑤,得到的E可能的結構簡式為______________________ 、_____________________、_____________________。
(4)寫出下列反應的化學方程式(并注明反應條件) A→B _________;C→D____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】甲醛是一種重要的化工產品,可利用甲醇催化脫氫制備。甲醛與氣態甲醇之間轉化的能量關系如圖所示。

(1)甲醇催化脫氫轉化為甲醛的反應是_______(填“吸熱”或“放熱”)反應;
(1)過程Ⅰ與過程Ⅱ的反應熱______(填“相同”或“不同”),原因是___________________________________________________________;
(2)寫出甲醇催化脫氫轉化為甲醛的熱化學方程式
__________________________________________________________;
(3) 甲醇催化脫氫轉化為甲醛的過程中,如果要使反應溫度維持在700℃,需向體系中通入空氣,通過計算確定進料甲醇與空氣的物質的量理論比值為___________________________。(假設:H2(g)+1/2O2(g)===H2O(g) ΔH=-a kJ·mol-1,空氣中氧氣含量為20%)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】依據題意,完成下列各題:
(1)1.0 g乙醇完全燃燒生成液態水放出1.37 kJ熱量,表示乙醇的燃燒熱的熱化學方程式為__________________________________________________;
(2) “長征”2號火箭的發動機中用“偏二甲肼”(分子式為C2H8N2)和四氧化二氮作為液態燃料。已知a g偏二甲肼與b g四氧化二氮在發動機內燃燒生成穩定的、對環境友好的物質。若生成1 mol N2(g) 的反應熱為c kJ,寫出熱化學方程式______________________________________________;
(3) T ℃時,如圖所示, 對應的化學方程式為______________________;
(4) 向足量的H2SO4溶液中加入100 mL 0.4 mol·L-1的Ba(OH)2溶液,放出的熱量是5.12 kJ。向足量的Ba(OH)2溶液中加入100 mL 0.4 mol·L-1的HCl溶液,放出的熱量為2.2 kJ。則Na2SO4溶液與BaCl2溶液反應的熱化學方程式為Ba2+(aq)+SO42-(aq)===BaSO4(s) ΔH=______________;
(5) 研究表明,化學反應的能量變化(ΔH)與反應物和生成物的鍵能有關。鍵能可以簡單地理解為斷開1 mol化學鍵時所需吸收的能量。下表是部分化學鍵的鍵能數據:
化學鍵 | P—P | P—O | O==O | P==O |
鍵能kJ/mol | 197 | 360 | 499 | x |
已知白磷(P4)的燃燒熱為2378.0 kJ/mol,白磷完全燃燒的產物(P4O10)的結構如圖所示,則上表中x=_________________。


查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】恒溫條件下,在體積不變的5L密閉容器中,充入2molCO、3molH2發生反應:CO(g)+2H2(g)![]() CH3OH(g),平衡后CH3OH的物質的量為1mol。下列敘述正確的是
CH3OH(g),平衡后CH3OH的物質的量為1mol。下列敘述正確的是
A. 隨反應的進行,氣體的平均相對分子質量逐漸減小
B. H2的平衡轉化率為50%
C. 該溫度反應的平衡常數K=25L2·mol-2
D. 平衡后再往容器中通入3mol CO,平衡不移動
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知下列反應的熱化學方程式:
6C(s)+5H2(g)+3N2(g)+9O2(g)=2C3H5(ONO2)3(l)△H1
2 H2(g)+ O2(g)= 2H2O(g)△H2
C(s)+ O2(g)=CO2(g)△H3
則反應4C3H5(ONO2)3(l)= 12CO2(g)+10H2O(g) + O2(g) +6N2(g)的△H為
A. 12△H3+5△H2-2△H1 B. 2△H1-5△H2-12△H3
C. 12△H3-5△H2-2△H1 D. △H1-5△H2-12△H3
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com