
【題目】新冠病毒爆發期間,各類消毒劑大顯身手,ClO2泡騰片就是一種,使用時將其投入水中即可產生ClO2對水體、環境消毒。已知ClO2是一種易溶于水而難溶于有機溶劑的氣體,實驗室制備ClO2的原理是用亞氯酸鈉固體與氯氣反應:2NaClO2+Cl2=2ClO2+2NaCl。如圖是實驗室用于制備和收集一定量純凈的ClO2的裝置(某些夾持裝置和墊持用品省略)。其中E中盛有CCl4液體(用于除去ClO2中的未反應的Cl2)。


(1)儀器P的名稱是__。
(2)寫出裝置A中燒瓶內發生反應的離子方程式__。
(3)B裝置中所盛試劑是__。
(4)F為ClO2收集裝置,應選用的裝置是__(從①②③中選擇),其中與E裝置導管相連的導管口是__(填導管口的字母)
(5)相同條件下,ClO2的消毒能力是Cl2的__倍(以等物質的量的消毒劑得電子的數目計算)。
【答案】分液漏斗 ![]() 飽和食鹽水 ② d 2.5
飽和食鹽水 ② d 2.5
【解析】
裝置A即實驗室制取氯氣的裝置,采用二氧化錳和濃鹽酸反應,B和C是氯氣的凈化裝置,分別是飽和食鹽水和濃硫酸,純凈的氯氣進入D中反應,得到![]() 氣體,E中的裝置可以除去未反應的氯氣,而F是
氣體,E中的裝置可以除去未反應的氯氣,而F是![]() 的收集裝置,據此來分析本題即可。
的收集裝置,據此來分析本題即可。
(1)儀器P是分液漏斗,用于向裝置A中滴加濃鹽酸;
(2)裝置A即實驗室制氯氣,離子方程式為![]() ;
;
(3)B裝置為了除去氯氣中混雜的![]() 氣體,因此是飽和食鹽水;
氣體,因此是飽和食鹽水;
(4)![]() 易溶于水,因此不能用排水集氣法,故只能選用裝置②,其密度大于空氣,因此要向上排空氣法,即d口進,c口出;
易溶于水,因此不能用排水集氣法,故只能選用裝置②,其密度大于空氣,因此要向上排空氣法,即d口進,c口出;
(5)1分子氯氣可以得到2個電子,而1分子![]() 最多能得到5個電子,從+4價降低到-1價,故消毒能力是氯氣的2.5倍。
最多能得到5個電子,從+4價降低到-1價,故消毒能力是氯氣的2.5倍。


 名師指導期末沖刺卷系列答案
名師指導期末沖刺卷系列答案科目:高中化學 來源: 題型:
【題目】有研究表明,內源性H2S作為氣體信號分子家族新成員,在抗炎、舒張血管等方面具有重要的生理作用,而籠狀COS(羰基硫)分子可作為H2S的新型供體(釋放劑)。試回答下列有關問題
(1)COS的分子結構與CO2相似,COS的結構式為______。
(2)已知:①COS(g)+H2(g)H2S(g)+CO(g)△H1=-15kJmol-1,②COS(g)+H2(g)H2S(g)+CO2(g)△H2=-36kJmol-1,③CO(g)+H2O(g)H2(g)+CO2(g)△H3,則△H=______。
(3)COS可由CO和H2S在一定條件下反應制得。在恒容的密閉容器中發生反應并達到平衡:CO(g)+H2S(g)COS(g)+H2(g),數據如表所示、據此填空
實驗 | 溫度/℃ | 起始時 | 平衡時 | |||
n(CO)/mol | n(H2S)/mol | n(COS)/mol | n(H2)/mol | n(CO)/mol | ||
1 | 150 | 10.0 | 10.0 | 0 | 0 | 7.0 |
2 | 150 | 7.0 | 8.0 | 2.0 | 4.5 | x |
3 | 400 | 20.0 | 20.0 | 0 | 0 | 16.0 |
①該反應為______(選填“吸熱反應”或“放熱反應”)。
②實驗2達到平衡時,x______7.0(選填“>”、“<”或“=”)
③實驗3達到平衡時,CO的轉化率α=______
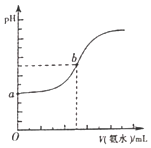
(4)已知常溫下,H2S和NH3H2O的電離常數分別為向pH=a的氫硫酸中滴加等濃度的氨水,加入氨水的體積(V)與溶液pH的關系如圖所示:
酸/堿 | 電離常數 | |
H2S | Ka1=1.0×10-7 | Ka2=7.0×10-15 |
NH3H2O | Kb=1.0×10-5 | |
①若c(H2S)為0.1mol/L,則a=______
②若b點溶液pH=7,則b點溶液中所有離子濃度大小關系是______。
(5)將H2S通入裝有固體FeCl2的真空密閉燒瓶內,恒溫至300℃,反應達到平衡時,燒瓶中固體只有FeCl2和FeSx(x并非整數),另有H2S、HCl和H2三種氣體,其分壓依次為0.30P0、0.80P0和0.04P0(P0表示標準大氣壓)。當化學方程式中FeCl2的計量數為1時,該反應的氣體壓強平衡常數記為Kp。計算:
①x=______(保留兩位有效數字)。
②Kp=______(數字用指數式表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列實驗裝置能達到實驗目的的是
A.除去淀粉溶液中的NaCl 
B.比較NaHCO3和Na2CO3的熱穩定性
C.制備Fe(OH)2 
D.測定過氧化鈉的純度
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】甘氨酸亞鐵[(NH2CH2COO)2Fe]是一種補鐵強化劑。實驗室利用FeCO3與甘氨酸(NH2CH2COOH)制備甘氨酸亞鐵,實驗裝置如下圖所示(夾持和加熱儀器已省略)。
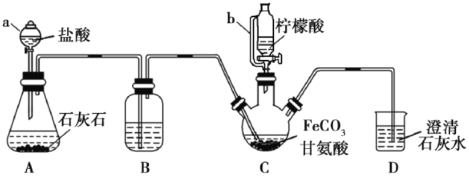
查閱資料:
①甘氨酸易溶于水,微溶于乙醇;甘氨酸亞鐵易溶于水,難溶于乙醇。
②檸檬酸易溶于水和乙醇,具有較強的還原性和酸性。
實驗過程:
I.裝置C中盛有17.4gFeCO3和200mL1.0mol·L-1甘氨酸溶液。實驗時,先打開儀器a的活塞,待裝置c中空氣排凈后,加熱并不斷攪拌;然后向三頸瓶中滴加檸檬酸溶液。
Ⅱ.反應結束后過濾,將濾液進行蒸發濃縮;加入無水乙醇,過濾、洗滌并干燥。
(1)儀器a的名稱是________;與a相比,儀器b的優點是_______________。
(2)裝置B中盛有的試劑是:____________;裝置D的作用是________________。
(3)向FeSO4溶液中加入NH4HCO3溶液可制得FeCO3,該反應的離子方程式為____________________________。
(4)過程I加入檸檬酸促進FeCO3溶解并調節溶液pH,溶液pH與甘氨酸亞鐵產率的關系如圖所示。
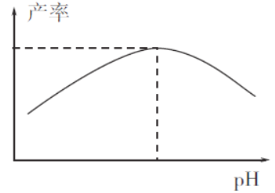
①pH過低或過高均導致產率下降,其原因是_____________________;
②檸檬酸的作用還有________________________。
(5)過程II中加入無水乙醇的目的是_______________________。
(6)本實驗制得15.3g甘氨酸亞鐵,則其產率是_____%。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】NaNO2因外觀和食鹽相似,又有咸味,容易使人誤食中毒。已知NaNO2能發生反應:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。
(1)上述反應中氧化劑是__,還原性I-__NO(填“>”或“<”)。
(2)根據上述反應,鑒別NaNO2和NaCl。可選用的物質有①水、②碘化鉀淀粉試紙、③淀粉、④白酒、⑤食醋,你認為必須選用的物質有__(填序號)。
(3)請配平以下化學方程式:__Al+__NaNO3+__NaOH=__NaAlO2+__N2↑+_H2O
若反應過程中轉移5mol電子,則生成標準狀況下N2的體積為__L。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】納米級Fe3O4可用于以太陽能為熱源分解水制H2,過程如下圖所示。下列說法正確的是:

A.過程Ⅰ的反應為6FeO+O2![]() 2Fe3O4
2Fe3O4 ![]()
B.過程Ⅱ中H2為還原劑
C.整個過程的總反應為:2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
D.FeO是過程Ⅰ的氧化產物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25℃ 時,三種酸的電離平衡常數如下:
化學式 | CH3COOH | H2CO3 | HClO |
電離平衡常數 | 1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
回答下列問題:
(1)一般情況下,當溫度升高時,Ka________(填“增大”、“減小”或“不變”)。
(2)下列四種離子結合質子能力由大到小的順序是___________________(填字母)。
a.CO32- b.ClO- c.CH3COO- d.HCO3-
(3)下列反應不能發生的是________(填字母)。
a. 2ClO-+CO2+H2O = CO32-+2HClO
b. ClO-+CH3COOH = CH3COO-+HClO
c. CO32-+2HClO = CO2↑+H2O+2ClO-
d. CO32-+2CH3COOH = 2CH3COO-+CO2↑+H2O
(4)用蒸餾水稀釋0.10mol·L-1的醋酸,下列各式表示的數值隨水量的增加而增大的是________(填字母)。
a.c(CH3COOH)/c(H+) b.c(CH3COO-)/c(CH3COOH) c.c(H+)/Ka d.c(H+)/c(OH-)
(5)體積均為10 mL、pH均為2的醋酸溶液與HX溶液分別加水稀釋至1000 mL,稀釋過程中pH變化如圖所示。

則醋酸的電離平衡常數________(填“>”、“=”或“<”,下同)HX的電離平衡常數;稀釋后,醋酸溶液中水電離出來的c(H+)____ HX溶液中水電離出來的c(H+);用同濃度的NaOH溶液分別中和上述兩種酸溶液,恰好中和時消耗NaOH溶液的體積:醋酸________HX。
(6)25℃時,若測得CH3COOH與CH3COONa的混合溶液的pH=6,則溶液中c(CH3COO-)-c(Na+)=________mol·L-1(填精確數值)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列變化中,屬于吸熱反應的是( )
①液態水的汽化 ②將膽礬加熱變為白色粉末
③濃硫酸稀釋 ④KCl03分解制氧氣
⑤生石灰跟水反應生成熟石灰
⑥CaCO3高溫分解⑦CO2+C![]() 2CO
2CO
⑧Ba(OH)2·8H2O與固體NH4Cl混合
⑨C(s)+H2O(g)![]() CO(g)+H2(g)⑩Al與鹽酸反應
CO(g)+H2(g)⑩Al與鹽酸反應
A. ②③④⑤⑥⑦⑧⑨ B.②④⑥⑦⑧⑨ C.②④⑥⑧ D.②③④⑧⑨
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖為從海帶中提取碘的工業生產過程圖,按照要求回答問題:

(1)海水中碘的總藏量很大,目前工業上___(填“直接”或“不直接”)用海水提取碘。
(2)工業生產過程中通常將干海帶粉碎的目的是___。
(3)“濾液”中加入硫酸酸化的離子方程式是___;“氧化”步驟發生反應的離子方程式是___。
(4)生產過程圖中“提純”的方法是___。
(5)下列有關從海帶中提取碘的說法錯誤的是___。
A.“過濾”操作若在實驗室進行,需要用到的玻璃儀器有漏斗、燒杯、玻璃棒
B.“堿化”時加入NaOH溶液的主要作用是可溶性有機質在堿性溶液中可形成沉淀
C.現在工業上從海帶中提取碘時,也有用離子交換法處理含碘離子的溶液以提高碘的提取率
D.可用淀粉溶液檢驗“濾液”中的離子是否氧化完全
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com