
常溫下,下列各組離子在指定溶液中一定能大量共存的是( )
A.1.0 mol·L-1KNO3溶液:H+,Fe2+,Cl-,SO42-
B.石蕊溶液呈紅色的溶液:NH4+,Ba2+,AlO2-,Cl—
C.與鋁反應產生大量氫氣的溶液:Na+,K+,NH4+,NO3-
D.pH=12的溶液:K+,Na+,NO3—,Cl—
科目:高中化學 來源:2016屆吉林省高一上學期期末質量檢測化學試卷(解析版) 題型:選擇題
下列說法不正確的是
A.二氧化硅可用于制光導纖維
B.工藝師利用氫氟酸刻蝕石英制作藝術品
C.金屬鋁既能溶于酸又能溶于堿
D.從海水中提取溴的過程中,既發生化學變化又發生物理變化
查看答案和解析>>
科目:高中化學 來源:2016屆云南省高一下學期第一次月考化學試卷(解析版) 題型:選擇題
已知KClO3與濃HCI反應的化學方程式為:KClO3+6HCl=KCl+3C12+3H2O,若用K35C1O3與H37Cl作用,則下列說法正確的是 ( )
A.所得氯氣的相對分子質量約為71
B.KCl中只含35C1
C.所得的KCl中既含35C1又含37Cl
D.被氧化和被還原的氯原子數之比為5∶1
查看答案和解析>>
科目:高中化學 來源:2016屆云南省高一下學期第一次月考化學試卷(解析版) 題型:選擇題
下列說法正確的是( )
A.39K+和40Ca2+微粒中的電子數和中子數都相等
B.在標準狀況下,若D2和He體積相等,則質量不相等
C.7.8 g Na2O2與足量的CO2反應時失去的電子數為0.2 NA
D.把1 mol NaCl溶于1 L水中,所得NaCl溶液的物質的量濃度為1mol/L
查看答案和解析>>
科目:高中化學 來源:2015屆福建省龍巖市高二第一學期教學質量檢測化學試卷(解析版) 題型:選擇題
有人建議用AG表示溶液酸度,AG定義為 AG=lg[c(H+)/c(OH-)]。回答下列問題:
(1)25℃時,溶液的AG與其pH之間的關系為AG= 。
(2)25℃時,一元弱堿MOH溶液的AG=-8。取20mL該MOH溶液,當與16.2mL 0.05 mol/L硫酸混合時,兩者恰好完全中和。求此條件下該一元弱堿的電離平衡常數。
查看答案和解析>>
科目:高中化學 來源:2015屆福建省龍巖市高二第一學期教學質量檢測化學試卷(解析版) 題型:選擇題
某化學興趣小組為探究電化學原理,設計了如圖裝置(鐵、銅為電極,燒杯中盛裝硫酸銅溶液)。下列敘述不正確的是
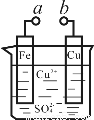
A.a和b不連接時,鐵片上會有金屬銅析出
B.a和b用導線連接時,鐵片上發生的反應為:Fe-3e- = Fe3+
C.無論a和b是否連接,鐵片均會溶解,溶液從藍色逐漸變成淺綠色
D.a和b分別連接直流電源正、負極,Cu2+向銅電極移動
查看答案和解析>>
科目:高中化學 來源:2015屆福建省四地六校高二下學期第一次月考化學試卷(解析版) 題型:填空題
A、B、C、D、E代表5種元素。請填空:
(1)A元素基態原子的最外層有3個未成對電子,次外層有2個電子,其元素符號為 ;
(2)B元素的負一價離子的電子層結構都與氬相同,B的原子結構示意圖為
(3)C元素是第三周期中無未成對電子的主族元素,它的軌道排布式為 ;
(4)D元素基態原子的M層全充滿,N層只有一個未成對電子,D基態原子的電子排布式為
(5)E原子共有3個價電子,其中一個價電子位于第三能層d軌道,指出該元素在周期表中所處的周期數和族序數
查看答案和解析>>
科目:高中化學 來源:2015屆湖北省黃石市高二上學期期末考試化學試卷(解析版) 題型:填空題
銅單質及其化合物在工業生產和科研中有重要作用。
(1)已知:2Cu2O(s) + O2(g) = 4CuO(s) △H=-292kJ·mol-1
2C(s)+O2(g) =2CO(g) △H=-221kJ·mol-1
請寫出用足量炭粉還原CuO(s)制備Cu2O(s)的熱化學方程式: ;
(2)現用氯化銅晶體(CuCl2·2H2O,含氯化亞鐵雜質)制取純凈的CuCl2·2H2O。先將其制成水溶液,后按如圖步驟進行提純:
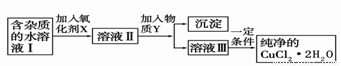
已知Cu2+、Fe3+和Fe2+的氫氧化物開始沉淀和沉淀完全時的pH見下表
金屬離子 | Fe3+ | Fe2+[來源:學&科& | Cu2+ |
氫氧化物開始沉淀時的pH | 1.9 | 7.0 | 4.7 |
氫氧化物完全沉淀時的pH | 3.2 | 9.0 | 6.7 |
請回答下列問題:
①現有氧化劑NaClO、H2O2、KMnO4,X加哪種好,為什么?
;該反應的離子方程式為 。
②溶液II中除Cu2+外,還有 金屬離子,如何檢驗其存在 。
③物質Y不能為下列的
a.CuO b.Cu(OH)2 c.CuCO3 d.Cu2(OH)2CO3 e.CaO f.NaOH
④若向溶液Ⅱ中加入碳酸鈣,產生的現象是 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com