
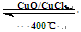 2Cl2(g)+2H2O(g) ΔH=" —115.6" kJ/mol
2Cl2(g)+2H2O(g) ΔH=" —115.6" kJ/mol 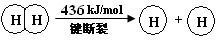

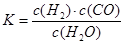 ,它所對應的化學方程式為:
,它所對應的化學方程式為:  2NH3(g) △H<0 的K=0.5,則400℃時,在0.5L的反應容器中進行合成氨反應,一段時間后,測得N2、H2、NH3的物質的量分別為2mol、1mol、2mol,則此時反應v(N2)正 v(N2)逆(填:>、<、=、不能確定)(1分)
2NH3(g) △H<0 的K=0.5,則400℃時,在0.5L的反應容器中進行合成氨反應,一段時間后,測得N2、H2、NH3的物質的量分別為2mol、1mol、2mol,則此時反應v(N2)正 v(N2)逆(填:>、<、=、不能確定)(1分) 2C(g) + D(s) ΔH,其化學平衡常數K與溫度t的關系如下表:
2C(g) + D(s) ΔH,其化學平衡常數K與溫度t的關系如下表:| t/K | 300 | 400 | 500 | … |
| K/(mol·L—1)2 | 4×106 | 8×107 | K1 | … |
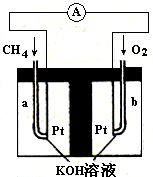
 H2(g) + CO(g)(2)= (1分), A (1分) (3)①>(1分) ② CD (4)①CH4-8e—+10OH—= CO32—+7H2O ②c(K+)>c(HCO3—)>c(CO32—)>c(OH—)>c(H+)
H2(g) + CO(g)(2)= (1分), A (1分) (3)①>(1分) ② CD (4)①CH4-8e—+10OH—= CO32—+7H2O ②c(K+)>c(HCO3—)>c(CO32—)>c(OH—)>c(H+)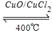 2Cl2(g)+2H2O(g),△H=-115.6kJ/mol,②H2(g)+Cl2(g)═2HCl(g)△H=-184kJ/mol,依據蓋斯定律:①+②×2得到熱化學方程式為:2H2(g)+O2(g)=2H2O(g)△H="-483.6" kJ/mol;(2)依據反應的熱化學方程式:2H2(g)+O2(g)=2H2O(g)△H="-483.6" kJ/mol,△H=斷裂化學鍵吸收的能量-形成化學鍵放出的能量="2×436KJ+498KJ-4×H-O=-483.6" kJ,則得到H-O的鍵能=463.4kJ;
2Cl2(g)+2H2O(g),△H=-115.6kJ/mol,②H2(g)+Cl2(g)═2HCl(g)△H=-184kJ/mol,依據蓋斯定律:①+②×2得到熱化學方程式為:2H2(g)+O2(g)=2H2O(g)△H="-483.6" kJ/mol;(2)依據反應的熱化學方程式:2H2(g)+O2(g)=2H2O(g)△H="-483.6" kJ/mol,△H=斷裂化學鍵吸收的能量-形成化學鍵放出的能量="2×436KJ+498KJ-4×H-O=-483.6" kJ,則得到H-O的鍵能=463.4kJ; 2C(g) + D(s)是一個氣體系數發生變化的反應,故容器內壓強保持不變或混合氣體的密度保持不變均可使此反應達到平衡。(4)①正極發生還原反應,氧氣在正極放電生成氫氧根離子,正極電極反應式為:O2+4e-+2H2O=4OH-;②參與反應的氧氣在標準狀況下體積為8960mL,物質的量為8.96L/22.4L/mol =0.4mol,根據電子轉移守恒可知,生成二氧化碳為(0.4mol×4 )/8 =0.2mol,n(NaOH)=0.1L×3.0mol?L-1=0.3mol,n(NaOH):n(CO2)=0.3mol:0.2mol=3:2,介于1:1與2:1之間,故生成碳酸鉀、碳酸氫鉀,令碳酸鉀、碳酸氫鉀的物質的量分別為xmol、ymol,則x+y=0.2,2x+y=0.3,解得x=0.1,y=0.1,溶液中碳酸根水解,碳酸氫根的水解大于電離,溶液呈堿性,故c(OH-)>c(H+),碳酸根的水解程度大于碳酸氫根,故c(HCO3-)>c(CO32-),鉀離子濃度最大,水解程度不大,碳酸根濃度原大于氫氧根離子,故c(K+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+);
2C(g) + D(s)是一個氣體系數發生變化的反應,故容器內壓強保持不變或混合氣體的密度保持不變均可使此反應達到平衡。(4)①正極發生還原反應,氧氣在正極放電生成氫氧根離子,正極電極反應式為:O2+4e-+2H2O=4OH-;②參與反應的氧氣在標準狀況下體積為8960mL,物質的量為8.96L/22.4L/mol =0.4mol,根據電子轉移守恒可知,生成二氧化碳為(0.4mol×4 )/8 =0.2mol,n(NaOH)=0.1L×3.0mol?L-1=0.3mol,n(NaOH):n(CO2)=0.3mol:0.2mol=3:2,介于1:1與2:1之間,故生成碳酸鉀、碳酸氫鉀,令碳酸鉀、碳酸氫鉀的物質的量分別為xmol、ymol,則x+y=0.2,2x+y=0.3,解得x=0.1,y=0.1,溶液中碳酸根水解,碳酸氫根的水解大于電離,溶液呈堿性,故c(OH-)>c(H+),碳酸根的水解程度大于碳酸氫根,故c(HCO3-)>c(CO32-),鉀離子濃度最大,水解程度不大,碳酸根濃度原大于氫氧根離子,故c(K+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+);

 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源:不詳 題型:填空題
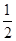 O2(g)=H2O(g) ΔH1=-241.8 kJ·mol-1
O2(g)=H2O(g) ΔH1=-241.8 kJ·mol-1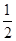 O2(g)=CO(g) ΔH2=-110.5 kJ·mol-1
O2(g)=CO(g) ΔH2=-110.5 kJ·mol-1
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
 CH3OH(g) △H
CH3OH(g) △H| 化學鍵 | C—C | C—H | H—H | C—O | C≡O | H—O |
| 鍵能/kJ·mol-1 | 348 | 413 | 436 | 358 | 1072 | 463 |
| 反應時間/min | 0 | 5 | 10 | 15 | 20 | 25 |
| 壓強/MPa | 12.6 | 10.8 | 9.5 | 8.7 | 8.4 | 8.4 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
 CH3OH(g) ΔH1
CH3OH(g) ΔH1 CH3OH(g) + H2O(g) ΔH2
CH3OH(g) + H2O(g) ΔH2| 溫度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
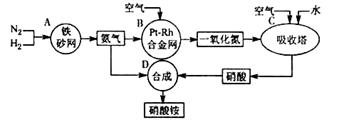
| 時間/min | 0 | 5 | 10 | 15 | 20 | 25 | 35 | 50 | 60 | 70 | 80 |
| 溫度/℃ | 25 | 26 | 26 | 26 | 26 | 26 | 26.5 | 27 | 27 | 27 | 27 |
| 實驗 編號 | 銅片 質量/g | 0.1mol·L-1的 硝酸體積/mL | 硝酸銅 晶體/g | 亞硝酸鈉 晶體/g | 實驗目的 |
| ① | 5 | 20 | _______ | _______ | 實驗①和②探究_________的影響;實驗①和③探究亞硝酸根的影響。 |
| ② | 5 | 20 | 0.5 | 0 | |
| ③ | 5 | 20 | 0 | 0.5 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
 2SO3(g) △H<0反應,某溫度下,SO2的平衡轉化率(α)與體系總壓強(p)的關系如下圖所示,根據圖示回答下列問題:
2SO3(g) △H<0反應,某溫度下,SO2的平衡轉化率(α)與體系總壓強(p)的關系如下圖所示,根據圖示回答下列問題:
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題

 CO2(g)+H2(g),該反應的△H________0(選填:“>”、“<”、“=”);在900K時,該反應平衡常數的對數值(lgK)=_____________.
CO2(g)+H2(g),該反應的△H________0(選填:“>”、“<”、“=”);在900K時,該反應平衡常數的對數值(lgK)=_____________.
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
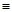 N鍵吸收941kJ熱量,則1molN4氣體轉化為2molN2時要放出______________ kJ能量。
N鍵吸收941kJ熱量,則1molN4氣體轉化為2molN2時要放出______________ kJ能量。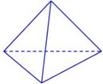
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
 W (s) + 3H2O (g)
W (s) + 3H2O (g) | 溫度 | 25℃ ~ 550℃ ~ 600℃ ~ 700℃ |
| 主要成份 | WO3 W2O5 WO2 W |
 W (s) + 2H2O (g);ΔH = +66.0 kJ·mol-1
W (s) + 2H2O (g);ΔH = +66.0 kJ·mol-1  W (s) + 2H2O (g);ΔH = -137.9 kJ·mol-1
W (s) + 2H2O (g);ΔH = -137.9 kJ·mol-1  WO2 (g) 的ΔH = ______________________。
WO2 (g) 的ΔH = ______________________。 WI4 (g)。下列說法正確的有____________。
WI4 (g)。下列說法正確的有____________。查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com