
┼╝░Ųõ╗»║Ž╬’į┌─═¾{£ž║ŽĮ╣żśIĪó┤▀╗»ä®ųŲįņĪó¾{─▄╚╝┴ŽĄ╚ĘĮ├µæ¬ė├ÅVĘ║ĪŻ
Ż©1Ż®Ą¬╗»┼╩Ūę╗ĘN─═Ė▀£ž▓─┴ŽŻ¼╦╚ų¬ŽÓĻPĘ┤æ¬Ą─¤ß╗»īWĘĮ│╠╩Į╚ńŽ┬Ż║
2B(s)+N2(g)= 2BN(s) ”żH="a" kJ ? mol-1
B2H6 (g)=2B(s) + 3H2 (g) ”żH =b kJ ? mol-1
N2 (g) + 3H2 (g) 2NH3 (g) ”żH ="c" kJ? mol-1
2NH3 (g) ”żH ="c" kJ? mol-1
ó┘Ę┤æ¬B2H6(g)+2NH3(g)=2BN(s)+6H2(g) ”żH = (ė├║¼aĪóbĪócĄ─┤·öĄ╩Į▒Ē╩Š)kJ Īżmol-1ĪŻ
ó┌B2H6╩Ūę╗ĘN¾{─▄╚╝┴ŽŻ¼īæ│÷Ųõ┼cCl2Ę┤æ¬╔·│╔ā╔ĘN┬╚╗»╬’Ą─╗»īWĘĮ│╠╩ĮŻ║ ĪŻ
Ż©2Ż®┼Ą─ę╗ą®╗»║Ž╬’Ą─¬Ü╠žąį┘|╚šęµ╩▄ĄĮ╚╦éāĄ─ĻPūóĪŻ
ó┘ūŅĮ³├└ć°╗»īW╝ęĮ▄╬„Īż╦_░═Ą┘─ß░l¼Fė╔╠╝╗»┼ųŲū„Ą─ŠG╔½čµ╗▒╚é„Įyčµ╗Ż©Ž§╦ßõ^Ż®Ė³░▓╚½Ż¼╠╝╗»┼ųą┼Ą─┘|┴┐ĘųöĄ×ķ78. 6%Ż¼ät╠╝╗»┼Ą─╗»īW╩Į×ķ ĪŻ
ó┌Į³─ĻüĒ╚╦éāīóLiBH4║═LiNH2Ū“─ź╗»║Ž┐╔ą╬│╔ą┬Ą─╗»║Ž╬’Li3BN2H8║═Li4BN3 H10Ż¼Li3BN2H8Ū“─ź╩Ū░┤╬’┘|Ą─┴┐ų«▒╚n(LiNH2) : n(LiBH4) =" 2" : 1╝ė¤ßŪ“─źą╬│╔Ą─Ż¼Ę┤æ¬▀^│╠ųąĄ─Xč▄╔õłDūV╚ńłD╦∙╩ŠĪŻ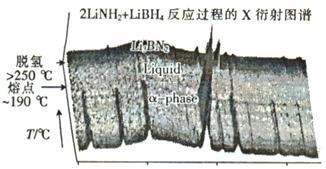
Li3BN2H8į┌┤¾ė┌250ĪµĢrĘųĮŌĄ─╗»īWĘĮ│╠╩Į×ķ Ż¼Li3BN2H8┼cLi4BN3H10Ą─╬’┘|Ą─┴┐ŽÓ═¼ĢrŻ¼│õĘųĘųĮŌŻ¼Ę┼│÷Ą╚┴┐Ą─H2Ż¼Li4BN3 H10ĘųĮŌĢr▀ĆĢ■«a╔·╣╠¾wLi2NH║═┴Ēę╗ĘNÜŌ¾wŻ¼įōÜŌ¾w╩Ū ĪŻ
Ż©3Ż®ų▒Įė┼Üõ╗»╬’╚╝┴ŽļŖ│žĄ─įŁ└Ē╚ńłDŻ¼žōśOĄ─ļŖśOĘ┤æ¬╩Į×ķ ĪŻļŖ│ž┐éĘ┤æ¬Ą─ļxūėĘĮ│╠╩Į×ķ ĪŻ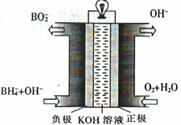
Ż©1Ż®ó┘a+b-c ó┌B2H6Ż½6Cl2=2BCl3Ż½6HCl
Ż©2Ż®ó┘B4C ó┌Li3BN2H8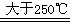 Li3BN2Ż½4H2Ī³Ż╗NH3
Li3BN2Ż½4H2Ī³Ż╗NH3
Ż©3Ż®BH4ŻŁŻ½8OHŻŁŻŁ8eŻŁ=BO2ŻŁŻ½6H2OŻ╗BH4ŻŁŻ½2O2=BO2ŻŁŻ½2H2O
ĮŌ╬÷įćŅ}Ęų╬÷Ż║Ż©1Ż®ó┘īóĄ┌ę╗éĆĘĮ│╠╩Į┼cĄ┌Č■éĆĘĮ│╠╩ĮŽÓ╝ėŻ¼£p╚źĄ┌╚²éĆĘĮ│╠╩ĮŻ¼┐╔Ą├─┐ś╦ĘĮ│╠╩ĮŻ¼Ę┤欤ßū„ŽÓæ¬ūā╗»╝┤┐╔ĪŻ
ó┌╔·│╔ā╔ĘN┬╚╗»╬’Ż¼Ė∙ō■įŁūė╩ž║Ńų╗─▄╩ŪBCl3║═HClĪŻ
Ż©2Ż®ó┘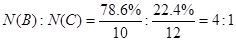 Ż¼ę“┤╦Ęųūė╩Į×ķB4CĪŻ
Ż¼ę“┤╦Ęųūė╩Į×ķB4CĪŻ
ó┌Ė∙ō■č▄╔õłDŻ¼£žČ╚┤¾ė┌250ĪµŻ¼ĘųĮŌ«a╬’ų«ę╗╩ŪLi3BN2Ż¼ät┴Ēę╗«a╬’╩ŪH2ĪŻÅ─╦∙║¼ėąĄ─į¬╦ž┐┤Ż¼▀Ć─▄ą╬│╔Ą─ÜŌ¾w╩ŪNH3ĪŻ
Ż©3Ż®Å─ļŖ│ž╩ŠęŌłD┐╔ų¬Ż¼žōśO═©╚ļBH4ŻŁ║═OHŻŁŻ¼╔·│╔BO2-Ż¼ō■┤╦┐╔īæ│÷ļŖśOĘ┤æ¬╩ĮĪŻÅ─╩ŠęŌłD╔Ž┐╔ų¬Ż¼š²śOĘ┤æ¬×ķO2║═H2O╔·│╔OH-Ż¼š²ĪóžōśOĘ┤æ¬╩ĮŽÓ╝ė┐╔Ą├ļŖ│ž┐éĘ┤æ¬ĪŻ
┐╝³cŻ║┐╝▓ķ╔w╦╣Č©┬╔Ż¼ĘĮ│╠╩ĮĢ°īæŻ¼╗»īWėŗ╦ŃŻ¼įŁļŖ│žĄ╚ĪŻ


 ā×╗»ū„śI╔Ž║Ż┐Ų╝╝╬─½I│÷░µ╔ńŽĄ┴ą┤░Ė
ā×╗»ū„śI╔Ž║Ż┐Ų╝╝╬─½I│÷░µ╔ńŽĄ┴ą┤░Ė
| ─Ļ╝ē | Ė▀ųąšn│╠ | ─Ļ╝ē | │§ųąšn│╠ |
| Ė▀ę╗ | Ė▀ę╗├Ō┘Mšn│╠═Ų╦]ŻĪ | │§ę╗ | │§ę╗├Ō┘Mšn│╠═Ų╦]ŻĪ |
| Ė▀Č■ | Ė▀Č■├Ō┘Mšn│╠═Ų╦]ŻĪ | │§Č■ | │§Č■├Ō┘Mšn│╠═Ų╦]ŻĪ |
| Ė▀╚² | Ė▀╚²├Ō┘Mšn│╠═Ų╦]ŻĪ | │§╚² | │§╚²├Ō┘Mšn│╠═Ų╦]ŻĪ |
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║╠Ņ┐šŅ}
Ż©1Ż®ßt»¤╔Ž│Żė├ØŌČ╚×ķ75%Ą──│ėąÖC╬’╦«╚▄ę║ū„Ųż─wŽ¹ČŠę║ĪŻįōėąÖC╬’Ą─ĮYśŗ║å╩Į╩Ū ĪŻ
Ż©2Ż®ę╗Č©Śl╝■Ž┬Ż¼0.1mol░▒ÜŌ┼cč§ÜŌĘ┤æ¬╔·│╔ā╔ĘN¤oČŠÜŌ¾wŻ¼Ę┼│÷31.67kJ¤ß┴┐ĪŻīæ│÷║╦Ę┤æ¬Ą─¤ß╗»īWĘĮ│╠╩ĮŻ║ ĪŻ
Ż©3Ż®¼Fėą╣╠¾wXŻ¼┐╔─▄║¼ėąCuĪóSiO2ĪóKNO3ĪóNH4ClųąĄ─ę╗ĘN╗“ÄūĘNĪŻ×ķ┴╦╠ĮŠ┐Ųõ│╔ĘųŻ¼─│īW┴ĢąĪĮM╚ĪįōśėŲĘ▀Mąą╚ńŽ┬īŹ“ׯ©▓┐Ęų«a╬’ęč┬į╚źŻ®ĪŻ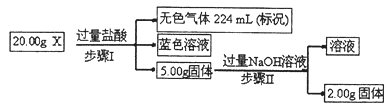
ó┘▓Į¾EIųą░l╔·Ę┤æ¬Ą─ļxūėĘĮ│╠╩Į×ķ ĪŻ
ó┌20.00gXųąCuĄ─┘|┴┐ĘųöĄ×ķ ĪŻ
ó█×ķ▀Mę╗▓Į┤_Č©╣╠¾wXĄ─ĮM│╔Ż¼│Ż£žŽ┬Ż¼īW┴ĢąĪĮM┴Ē╚Ī╣╠¾wX╝ė╦«Ż¼│õĘųöć░Ķ║¾▀^×VŻ¼£yĄ├×Vę║Ą─pHŻ╝7ĪŻ╦¹éā┼ąöÓę╗Č©ėąNH4ClŻ¼└Ēė╔╩Ū ĪŻ
Ż©4Ż®╣żśI╔Ž│Żė├ļŖØB╬÷Ę©╔·«aHIŻ¼Ųõ─ŻöMīŹ“×╚ńłDĪŻīæ│÷ĻÄśOĄ─ļŖśOĘ┤æ¬╩ĮŻ║ ĪŻ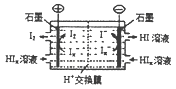
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║╠Ņ┐šŅ}
╣żśI╔ŽęįNH3×ķįŁ┴ŽĮø▀^ę╗ŽĄ┴ąĘ┤æ¬┐╔ęįĄ├ĄĮHNO3ĪŻ
Ż©1Ż®╣żśI╔ŽNH3Ą─┤▀╗»č§╗»Ę┤æ¬ĘĮ│╠╩Į×ķ Ż╗×ķ┴╦▒M┐╔─▄ČÓĄžīŹ¼F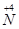 Ž“
Ž“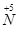 Ą─▐D╗»Ż¼šł─Ń╠ß│÷ę╗Śl┐╔ąąąįĮ©ūh ĪŻ
Ą─▐D╗»Ż¼šł─Ń╠ß│÷ę╗Śl┐╔ąąąįĮ©ūh ĪŻ
Ż©2Ż®īó╣żśIÅUÜŌNO┼cCO╗ņ║ŽŻ¼Įø╚²į¬┤▀╗»ä®▐D╗»Ų„╠Ä└Ē╚ńŽ┬Ż║2CO+2NO 2CO2+N2ĪŻ
2CO2+N2ĪŻ
ęčų¬Ż║
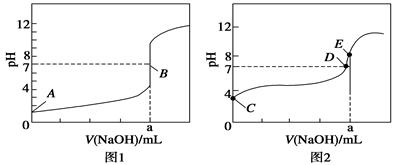
CO(g)+ 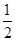 O2(g)=CO2(g) Ī„H=-283.0kJĪżmol-1
O2(g)=CO2(g) Ī„H=-283.0kJĪżmol-1
N2(g)+O2(g)=2NO(g) Ī„H=+180.0kJĪżmol-1
╚²į¬┤▀╗»ä®▐D╗»Ų„ųą░l╔·Ę┤æ¬Ą─¤ß╗»īWĘĮ│╠╩Į×ķ Ż╗
×ķ┴╦£yČ©į┌─│ĘN┤▀╗»ä®ū„ė├Ž┬Ą─Ę┤æ¬╦┘┬╩Ż¼į┌─│£žČ╚Ž┬ė├ÜŌ¾wé„ĖąŲ„£yĄ├▓╗═¼ĢrķgĄ─NO║═COØŌČ╚▓┐ĘųöĄō■ėøõø╚ńŽ┬Ż║
| Ģrķg/s | 0 | 2 | 3 | 4 |
| c(NO)/molĪżL-1 | 1.00Ī┴10-3 | 1.50Ī┴10-4 | 1.00Ī┴10-4 | 1.00Ī┴10-4 |
 C(CO)/molĪżL-1 C(CO)/molĪżL-1 | |  |  2.70Ī┴10-3 2.70Ī┴10-3 | |
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║å¢┤Ņ}
Ż©12ĘųŻ® (1)ęčų¬Ż║š¶░l1 mol Br2(l)ąĶę¬╬³╩šĄ──▄┴┐×ķ 30 kJŻ¼Ųõ╦¹ŽÓĻPöĄō■╚ńŽ┬▒ĒŻ║
| ╬’┘| | H2(g) | Br2(g) | HBr(g) |
| 1 molĘųūėųą╗»īWµIöÓ┴čĢrąĶę¬╬³╩šĄ──▄┴┐/kJ | 436 | 200 | 369 |
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║å¢┤Ņ}
Ż©15ĘųŻ®
╝ū┤╝╩Ūę╗ĘN┐╔į┘╔·─▄į┤Ż¼Š▀ėąÅVĘ║Ą─ķ_░l║═æ¬ė├Ū░Š░Ż«šł╗ž┤Ž┬┴ą┼c╝ū┤╝ėąĻPĄ─å¢Ņ}Ż«
Ż©1Ż®╝ū┤╝Ęųūė╩Ū____ĘųūėŻ©╠ŅĪ░śOąįĪ▒╗“Ī░ĘŪśOąįĪ▒Ż®Ż«
Ż©2Ż®╣żśI╔Žę╗░Ń┐╔▓╔ė├╚ńŽ┬Ę┤æ¬üĒ║Ž│╔╝ū┤╝Ż║CO(g)+2H2(g) CH3OH(g)Ī„H=-86.6kJ/molŻ¼į┌TĪµĢrŻ¼═∙ę╗éĆ¾wĘe╣╠Č©×ķ1LĄ─├▄ķ]╚▌Ų„ųą╝ė╚ļ1mol CO║═2mol H2Ż║Ż¼Ę┤æ¬▀_ĄĮŲĮ║ŌĢrŻ¼╚▌Ų„ā╚Ą─ē║ÅŖ╩Ūķ_╩╝ĢrĄ─3/5Ż«
CH3OH(g)Ī„H=-86.6kJ/molŻ¼į┌TĪµĢrŻ¼═∙ę╗éĆ¾wĘe╣╠Č©×ķ1LĄ─├▄ķ]╚▌Ų„ųą╝ė╚ļ1mol CO║═2mol H2Ż║Ż¼Ę┤æ¬▀_ĄĮŲĮ║ŌĢrŻ¼╚▌Ų„ā╚Ą─ē║ÅŖ╩Ūķ_╩╝ĢrĄ─3/5Ż«
ó┘▀_ĄĮŲĮ║ŌĢrŻ¼COĄ─▐D╗»┬╩×ķ ĪŻ
ó┌Ž┬┴ą▀xĒŚ─▄┼ąöÓįōĘ┤æ¬▀_ĄĮŲĮ║ŌĀŅæBĄ─ę└ō■Ą─ėą____ ĪŻ
AŻ« | BŻ«COĄ─Ž¹║─╦┘┬╩Ą╚ė┌CH3OHĄ─╔·│╔╦┘┬╩ |
| CŻ«╚▌Ų„ā╚Ą─ē║ÅŖ▒Ż│ų▓╗ūā | DŻ«╗ņ║ŽÜŌ¾wĄ─├▄Č╚▒Ż│ų▓╗ūā |
 Ż©3Ż®ęčų¬į┌│Ż£ž│Żē║Ž┬Ż║
Ż©3Ż®ęčų¬į┌│Ż£ž│Żē║Ž┬Ż║

▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║å¢┤Ņ}
ę└ō■╩┬īŹŻ¼īæ│÷Ž┬┴ąĘ┤æ¬Ą─¤ß╗»īWĘĮ│╠╩ĮĪŻ
Ż©1Ż®1molC2H4(g)┼c▀m┴┐O2(g)Ę┤æ¬╔·│╔CO2Ż©gŻ®║═H2O(l)Ż¼Ę┼│÷1411kJ¤ß┴┐ĪŻ
Ż©2Ż®1molC2H5OH(l)┼c▀m┴┐O2(g)Ę┤æ¬╔·│╔CO2Ż©gŻ®║═H2O(l)Ż¼Ę┼│÷1366Ż«8kJ¤ß┴┐ĪŻ
Ż©3Ż®2molAlŻ©sŻ®┼c▀m┴┐O2(g)Ę┤æ¬╔·│╔Al2O3Ż©sŻ®Ż¼Ę┼│÷1669Ż«8kJ¤ß┴┐ĪŻ
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║ėŗ╦ŃŅ}
╠╝║═╠╝Ą─╗»║Ž╬’į┌╔·«aĪó╔·╗ŅųąĄ─æ¬ė├ĘŪ│ŻÅVĘ║Ż¼į┌╠ß│½ĮĪ┐Ą╔·╗Ņęč│╔│▒┴„Ą─Į±╠ņŻ¼Ī░Ą═╠╝╔·╗ŅĪ▒▓╗į┘ų╗╩Ūę╗ĘN└ĒŽļŻ¼Ė³╩Ūę╗ĘNųĄĄ├Ų┌┤²Ą─ą┬Ą─╔·╗ŅĘĮ╩ĮĪŻ
Ż©1Ż®īóCO2┼cĮ╣╠┐ū„ė├╔·│╔COŻ¼CO┐╔ė├ė┌¤ÆĶFĄ╚ĪŻ
ó┘ęčų¬Ż║Fe2O3(s)Ż½3C(╩»─½)ŻĮ2Fe(s)Ż½3CO(g) ”żH1ŻĮ +489.0 kJ/mol
C(╩»─½)Ż½CO2(g)ŻĮ2CO(g) ”żH2ŻĮ+172.5 kJ/mol
ätCO▀ĆįŁFe2O3Ą─¤ß╗»īWĘĮ│╠╩Į×ķ Ż╗
ó┌┬╚╗»ŌZŻ©PdCl2Ż®╚▄ę║│Ż▒╗æ¬ė├ė┌Öz£y┐šÜŌųą╬ó┴┐COĪŻPdCl2▒╗▀ĆįŁ│╔å╬┘|Ż¼Ę┤æ¬Ą─╗»īWĘĮ│╠╩Į×ķ Ż╗
Ż©2Ż®īóā╔éĆ╩»─½ļŖśO▓Õ╚ļKOH╚▄ę║ųąŻ¼Ž“ā╔śOĘųäe═©╚ļC3H8║═O2śŗ│╔▒¹═ķ╚╝┴ŽļŖ│žĪŻ
ó┘žōśOļŖśOĘ┤æ¬╩Į╩ŪŻ║ Ż╗
ó┌─│═¼īW└¹ė├▒¹═ķ╚╝┴ŽļŖ│žįOėŗ┴╦ę╗ĘNļŖĮŌĘ©ųŲ╚ĪFe(OH)2Ą─īŹ“×čbų├Ż©╚ńŽ┬łD╦∙╩ŠŻ®Ż¼═©ļŖ║¾Ż¼╚▄ę║ųą«a╔·┤¾┴┐Ą─░ū╔½│┴ĄĒŻ¼Ūę▌^ķLĢrķg▓╗ūā╔½ĪŻŽ┬┴ąšfĘ©ųąš²┤_Ą─╩Ū Ż©╠Ņą“╠¢Ż®
AŻ«ļŖį┤ųąĄ─aę╗Č©×ķš²śOŻ¼bę╗Č©×ķžōśO
BŻ«┐╔ęįė├NaCl╚▄ę║ū„×ķļŖĮŌę║
CŻ«AĪóBā╔Č╦Č╝▒žĒÜė├ĶFū„ļŖśO
DŻ«ĻÄśO░l╔·Ą─Ę┤æ¬╩ŪŻ║2H+Ż½2eŻŁŻĮH2Ī³
Ż©3Ż®īó▓╗═¼┴┐Ą─CO(g)║═H2O(g)Ęųäe═©╚ļ¾wĘe×ķ2LĄ─║Ń╚▌├▄ķ]╚▌Ų„ųąŻ¼▀MąąĘ┤æ¬Ż║CO(g)Ż½H2O(g)  CO2(g)Ż½H2(g)Ż¼Ą├ĄĮ╚ńŽ┬╚²ĮMöĄō■Ż║
CO2(g)Ż½H2(g)Ż¼Ą├ĄĮ╚ńŽ┬╚²ĮMöĄō■Ż║
| īŹ“×ĮM | £žČ╚/Īµ | Ų╩╝┴┐/mol | ŲĮ║Ō┴┐/mol | ▀_ĄĮŲĮ║Ō╦∙ąĶĢrķg/min | |
| H2O | CO | CO2 | |||
| 1 | 650 | 2 | 4 | 1.6 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 3 |
| 3 | 900 | 1 | 2 | 0.4 | 1 |
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║ėŗ╦ŃŅ}
IŻ«Ė▀Āt¤ÆĶF╩Ūę▒¤ÆĶFĄ─ų„ę¬ĘĮĘ©Ż¼░l╔·Ą─ų„ę¬Ę┤æ¬×ķŻ║
Fe2O3(s) + 3CO(g) 2Fe(s)+3CO2(g) Ī„H
2Fe(s)+3CO2(g) Ī„H
Ż©1Ż®ęčų¬Ż║ó┘Fe2O3(s) + 3C(╩»─½)="2Fe(s)" + 3CO(g) Ī„H1
ó┌C(╩»─½Ż®+ CO2(g) = 2CO(g) Ī„H2
ätĪ„H___________________(ė├║¼Ī„H1 ĪóĪ„H2Ą─┤·öĄ╩Į▒Ē╩Š)ĪŻ
Ż©2Ż®Ė▀Āt¤ÆĶFĘ┤æ¬Ą─ŲĮ║Ō│ŻöĄ▒Ē▀_╩ĮK=____________________________ĪŻ
Ż©3Ż®į┌─│£žČ╚ĢrŻ¼įōĘ┤æ¬Ą─ŲĮ║Ō│ŻöĄK=64Ż¼į┌2L║Ń╚▌├▄ķ]╚▌Ų„╝ū║═ęęųąŻ¼Ęųäe░┤Ž┬▒Ē╦∙╩Š╝ė╚ļ╬’┘|Ż¼Ę┤æ¬Įø▀^ę╗Č╬Ģrķg║¾▀_ĄĮŲĮ║ŌĪŻ
| | Fe2O3 | CO | Fe | CO2 |
| ╝ū/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| ęę/mol | 1.0 | 1.5 | 1.0 | 1.0 |
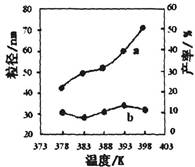
| ŠÄ╠¢ | £žČ╚/K | Ę┤æ¬Ģrķg/h | Ę┤æ¬╬’╬’┘|Ą─┴┐┼õ▒╚ | īŹ“×─┐Ą─ |
| ó┘ | 378 | 4 | 3Ī├1 | īŹ“×ó┌║═ó▄╠ĮŠ┐________ ______________________ īŹ“×ó┌║═__________╠ĮŠ┐ Ę┤æ¬Ģrķgī”«a┬╩Ą─ė░ĒæĪŻ |
| ó┌ | 378 | 4 | 4Ī├1 | |
| ó█ | 378 | 3 | _______ | |
| ó▄ | 398 | 4 | 4Ī├1 |
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║å╬▀xŅ}
į┌ę╗Č©£žČ╚Ž┬─│├▄ķ]╚▌Ų„ųą,┐╔─µĘ┤æ¬A(g)+3B(g)  2C(g)+2D(s)▀_ĄĮŲĮ║ŌŻ¼Ž┬┴ą├Ķ╩÷ę╗Č©š²┤_Ą─╩Ū
2C(g)+2D(s)▀_ĄĮŲĮ║ŌŻ¼Ž┬┴ą├Ķ╩÷ę╗Č©š²┤_Ą─╩Ū
ó┘CĄ─╔·│╔╦┘┬╩┼cCĄ─ĘųĮŌ╦┘┬╩ŽÓĄ╚ ó┌å╬╬╗Ģrķgā╚╔·│╔amolA,═¼Ģr╔·│╔3amolB
ó█AĪóBĪóCĄ─ØŌČ╚▓╗į┘ūā╗» ó▄Ę┤æ¬╬’Ą─▐D╗»┬╩▓╗į┘ūā╗»
ó▌╗ņ║ŽÜŌ¾wĄ─ē║ÅŖ▓╗į┘ūā╗» ó▐╗ņ║ŽÜŌ¾wĄ─╬’┘|Ą─┴┐▓╗į┘ūā╗»
ó▀å╬╬╗Ģrķgā╚Ž¹║─amolA,═¼Ģr╔·│╔ 3amolB óÓAĪóBĪóCĪóDĄ─ĘųūėöĄų«▒╚×ķ1:3:2:2
AŻ« ó┘ó┌ó█ó▄ó▌ó▐ó▀ BŻ«ó┘ó█ó▄ó▌ó▐ó▀
CŻ«ó┘ó█ó▄ó▐ó▀ DŻ«ó┘ó█ó▌ó▐ó▀óÓ
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
ć°ļHīWąŻā×▀x - ŠÜ┴Ģāį┴ą▒Ē - įćŅ}┴ą▒Ē
║■▒▒╩Ī╗ź┬ōŠW▀`Ę©║═▓╗┴╝ą┼Žó┼eł¾ŲĮ┼_ | ŠW╔Žėą║”ą┼Žó┼eł¾īŻģ^ | ļŖą┼įp“_┼eł¾īŻģ^ | ╔µÜv╩Ę╠ō¤oų„┴xėą║”ą┼Žó┼eł¾īŻģ^ | ╔µŲ¾ŪųÖÓ┼eł¾īŻģ^
▀`Ę©║═▓╗┴╝ą┼Žó┼eł¾ļŖįÆŻ║027-86699610 ┼eł¾Ó]ŽõŻ║58377363@163.com