
現有三種元素的基態原子的電子排布式如下:① 1s22s22p63s23p1;②1s22s22p63s23p3;③1s22s22p5。則下列有關比較中正確的是
| A.第一電離能:③>②>① | B.原子半徑:③>②>① |
| C.電負性:①>②>③ | D.最高正化合價:③>②>① |
A
解析試題分析:由核外電子排布式可知,①1s22s22p63s23p1為Al元素,②1s22s22p63s23p3為P元素,③1s22s22p5為F元素。A、同周期自左而右,第一電離能增大,即P元素的第一電離能大于Al元素的。F元素的非金屬性強于P元素,因此F元素的第一電離能大于P元素的,即第一電離能:③>②>①,A正確;B、同周期自左而右,原子半徑減小,同主族自上而下原子半徑增大,故原子半徑Al>P>F,即①>②>③,故B錯誤;C、同周期自左而右,電負性增大,同主族自上而下降低,故電負性③>②>①,故C錯誤;D、Al元素最高正化合價為+3,P元素最高正化合價為+5,F沒有正化合價,故最高正化合價:②>①>③,故D錯誤,答案選A。
考點:考查核外電子排布、電離能、電負性、原子半徑以及化合價判斷


科目:高中化學 來源: 題型:單選題
圖中a、b、c、d、e、f為元素周期表中前4周期的一部分元素,下列有關敘述正確的是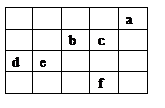
| A.b、c、e三種元素的原子半徑大小關系:e>c>b |
| B.六種元素分別形成的單質固體中,d的熔、沸點最高 |
| C.c的氫化物沸點比f的氫化物沸點低 |
| D.b元素除0價外,只有一種化合價 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
短周期主族元素A、B、C、D、E的原子序數依次遞增,A、B兩元素相鄰,B、C、E原子的最外層電子數之和為13,E原子最外層電子數是B原子內層電子數的3倍或者C原子最外層電子數的3倍,B、D原子最外層電子數之和等于C、E原子最外層電子數之和。下列說法正確的是
A.元素B和E的氧化物對應的水化物均為強酸
B.C的單質能與A的氧化物發生置換反應
C.元素C、D、E的最高價氧化物對應的水化物之間均可相互反應
D.工業上常用電解元素C、D的氯化物來制取它們的單質
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
關于鹵素(F、Cl、Br、I)的化學性質的敘述,錯誤的是
| A.隨原子序數逐漸增大,單質跟水的反應能力逐漸減弱 |
| B.隨原子序數逐漸增大,單質的氧化性逐漸減弱 |
| C.將氯水加到KI-淀粉溶液中,溶液變藍 |
| D.隨原子序數逐漸增大,氫化物的穩定性逐漸增強 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列比較中正確的是
| A.金屬性:Mg>Al>Na | B.原子半徑:S>O>F |
| C.堿性:KOH>Mg(OH)2>NaOH | D.氫化物的穩定性:HBr>HCl>PH3 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列事實中,不能用于判斷元素失電子能力強弱的是
| A.金屬間發生的置換反應 |
| B.金屬元素的最高價氧化物對應水化物的堿性強弱 |
| C.金屬元素的單質與水或酸反應置換出氫氣的難易 |
| D.每摩爾金屬單質在反應中失去電子數目的多少 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
短周期元素X.Y.Z.W的原子序數依次增大,X原子最外層電子數是其內層電子總數的3倍,Y原予最外層只有2個電子,Z單質可制成半導體材料,W寫X屬于同一主族。下列敘述正確的是
| A.元素X的簡單氣態氫化物的熱穩定性最弱 |
| B.元素W的最高價氧化物對應水化物的酸性比Z弱 |
| C.原子半徑的大小順序:r(Y)>r(Z)>r(W)>r(X) |
| D.化合物YX、ZX2、 WX3中化學鍵類型相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
YBa2Cu8Ox(Y為元素釔)是磁懸浮列車中的重要超導材料,關于8939Y的說法不正確的是( )
| A.屬于金屬元素 |
| B.質子數與中子數之差為50 |
| C.原子的核外電子數是39 |
| D.8939Y和9039Y是兩種不同的核素 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
X、Y、Z、W、T是元素周期表中前四周期的五種元素。有關這五種元素的信息如下表:
| 元素代號 | 相關信息 |
| X | 它的一種核素的原子核內沒有中子 |
| Y | 能組成很多種性質不同的單質,也是形成化合物種類最多的一種元素 |
| Z | 基態原子的最外層電子排布式為nsnnpn+1 |
| W | 與鉀元素能組成多種化合物,這些化合物與水反應均生成堿;大氣平流層中W3被譽為地球生物“保護傘” |
| T | 主要化合價有+1和+2價,且[T(X2W)4]2+和[T(ZX3)4]2+均呈藍色 |
 YZ- (aq)+X3W+(aq) ΔH="+45.6" KJ/mol
YZ- (aq)+X3W+(aq) ΔH="+45.6" KJ/mol查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com