
ĪŠŅ}─┐Ī┐Ż©1Ż®Ž“MnSO4║═┴“╦ߥ─╗ņ║Ž╚▄ę║└’╝ė╚ļK2S2O8(▀^Č■┴“╦ßŌø)Ż¼╚▄ę║ųąĢ■░l╔·╚ńŽ┬Ę┤æ¬Ż║Mn2++ S2O82-+H2OĪ·MnO4-+SO42ę╗╩«H+įōĘ┤æ¬│Żė├ė┌Öz“×Mn2+Ą─┤µį┌ĪŻŲõ╠žš„¼FŽ¾╩Ū_____________ĪŻ╚¶Ę┤æ¬ųąėą0Ż«1 mol▀ĆįŁä®ģó╝ėĘ┤æ¬Ż¼ätŽ¹║─č§╗»ä®Ą─╬’┘|Ą─┴┐×ķ____________molĪŻ
Ż©2Ż®╚¶įōĘ┤æ¬╦∙ė├Ą─┴“╦ßÕiĖ─×ķ┬╚╗»ÕiŻ¼«ö╦³Ė·▀^┴┐Ą─▀^Č■┴“╦ßŌøĘ┤æ¬ĢrŻ¼│²ėąĖ▀Õi╦ßŌøĪó┴“╦ßŌøĪó┴“╦ß╔·│╔═ŌŻ¼Ųõ╦¹Ą─╔·│╔╬’▀Ćėą___________________ĪŻ
Ż©3Ż®īóNaBiO3╣╠¾w(³S╔½╬ó╚▄)╝ė╚ļĄĮMnSO4║═H2SO4Ą─╗ņ║Ž╚▄ę║└’╝ė¤ßŻ¼╣╠¾w╚▄ĮŌūā×ķ│╬ŪÕ╚▄ę║Ż¼░l╔·╚ńŽ┬Ę┤æ¬Ż║
___NaBiO3+ MnSO4+ H2S04Ī· Na2S04+ Bi2(SO4)3+ NaMnO4+ H2OĪŻ
ó┘┼õŲĮ╔Ž╩÷Ę┤æ¬Ą─╗»īWĘĮ│╠╩ĮŻ╗
ó┌╔Ž╩÷Ę┤æ¬ųą▀ĆįŁ«a╬’╩Ū_______________ĪŻ
ó█ė├å╬ŠĆś“▒Ē╩Šįōč§╗»▀ĆįŁĘ┤æ¬▐DęŲļŖūėŪķør:_______________________________________________________________________ĪŻ
ĪŠ┤░ĖĪ┐ ╚▄ę║ė╔¤o╔½ūā×ķūŽ╔½ 0.25 Cl2 10 NaBiO3+ 4 MnSO4+ 14 H2S04Ī· 3Na2S04+ 5 Bi2(SO4)3+ 4 NaMnO4+ 14 H2OĪŻ Bi2(SO4)3 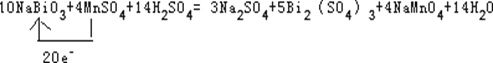
ĪŠĮŌ╬÷Ī┐įćŅ}Ęų╬÷Ż║Ż©1Ż®ė╔ė┌Ę┤æ¬╔·│╔Ė▀Õi╦ßĖ∙ļxūėŻ¼╚▄ę║ė╔¤o╔½ūā×ķūŽ╔½Ż╗Ę┤æ¬ųąÕiļxūėū÷▀ĆįŁä®Ż¼Õiį¬╦ž╗»║Žār╔²Ė▀5ārŻ¼┴“į¬╦ž╗»║ŽārĮĄĄ═1ārŻ¼╦∙ęį▀ĆįŁä®║═č§╗»ä®Ą─▒╚└²×ķ2:5Ż¼╦∙ęį«öėą0.1─”Ā¢▀ĆįŁä®Ę┤æ¬Ż¼Ž¹║─č§╗»ä®×ķ0.25─”Ā¢ĪŻ Ż©2Ż®ę“×ķĖ▀Õi╦ßĖ∙Ą─č§╗»ąį┤¾ė┌┬╚ÜŌŻ¼╦∙ęįĘ┤æ¬ųą▀ĆėąCl2╔·│╔ĪŻŻ©3Ż® ó┘Ė∙ō■ŃGį¬╦ž╗»║ŽārÅ─+5ĮĄĄ═ĄĮ+3Ż¼ĮĄĄ═2ārŻ¼Õiį¬╦ž╗»║ŽārÅ─+2╔²Ė▀ĄĮ+7Ż¼╔²Ė▀5ārŻ¼╦∙ęįč§╗»ä®║═▀ĆįŁä®Ą─▒╚└²×ķ5:2Ż¼į┘Ė∙ō■įŁūė╩ž║Ń┼õŲĮŻ¼Ą├ŽĄöĄ×ķ10Īó4Īó14Īó3Īó5Īó4Īó14Ż╗ó┌ŃGį¬╦ž╗»║ŽārĮĄĄ═Ż¼╦∙ęį▀ĆįŁ«a╬’×ķBi2(SO4)3ĪŻ
ó█Ė∙ō■┼õŲĮ▀^│╠Ęų╬÷ŃGį¬╦žĄ├ĄĮ20éĆļŖūėŻ¼Õiį¬╦ž╩¦╚ź20éĆļŖūėŻ¼╦∙ęįå╬ŠĆś“×ķ
![]()


 ╠ņ╠ņŽ“╔Žę╗▒Š║├ŠĒŽĄ┴ą┤░Ė
╠ņ╠ņŽ“╔Žę╗▒Š║├ŠĒŽĄ┴ą┤░Ė ąĪīW╔·10ĘųńŖæ¬ė├Ņ}ŽĄ┴ą┤░Ė
ąĪīW╔·10ĘųńŖæ¬ė├Ņ}ŽĄ┴ą┤░Ė
| ─Ļ╝ē | Ė▀ųąšn│╠ | ─Ļ╝ē | │§ųąšn│╠ |
| Ė▀ę╗ | Ė▀ę╗├Ō┘Mšn│╠═Ų╦]ŻĪ | │§ę╗ | │§ę╗├Ō┘Mšn│╠═Ų╦]ŻĪ |
| Ė▀Č■ | Ė▀Č■├Ō┘Mšn│╠═Ų╦]ŻĪ | │§Č■ | │§Č■├Ō┘Mšn│╠═Ų╦]ŻĪ |
| Ė▀╚² | Ė▀╚²├Ō┘Mšn│╠═Ų╦]ŻĪ | │§╚² | │§╚²├Ō┘Mšn│╠═Ų╦]ŻĪ |
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐į┌ś╦£╩ĀŅørŽ┬Ż¼CO║═CO2Ą─╗ņ║ŽÜŌ¾w╣▓8.96 LŻ¼┘|┴┐×ķ12.8 gŻ¼ätā╔ĘNÜŌ¾wĄ─╬’┘|Ą─┴┐ų«║═×ķ_______molŻ¼ŲõųąCO2×ķ_______molŻ¼COĄ─┘|┴┐ĘųöĄ_______Ż¼╗ņ║ŽÜŌ¾wĄ──”Ā¢┘|┴┐×ķ_______ĪŻ
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐ė├ÅVūVĖ▀ą¦Ą─Č■č§╗»┬╚Ż©ClO2Ż®╠µ┤·ę║┬╚▀MąąŽ¹ČŠŻ¼┐╔▒▄├Ō«a╔·ī”╚╦¾wĮĪ┐Ąėą║”Ą─ėąÖC┬╚┤·╬’Ż«
Ż©1Ż®Č■č§╗»┬╚Ż©ClO2Ż®╩Ū─┐Ū░ć°ļH╔Ž╣½šJĄ─Ą┌╦─┤·Ė▀ą¦Īó¤oČŠĄ─ÅVūVŽ¹ČŠä®Ż¼╦³┐╔ė╔KClO3į┌H2SO4┤µį┌Ž┬┼cNa2SO3Ę┤æ¬ųŲĄ├Ż«šłīæ│÷Ę┤æ¬Ą─ļxūėĘĮ│╠╩ĮŻ║ Ż«
Ż©2Ż®Ų»░ūä®üå┬╚╦ßŌcŻ©NaClO2Ż®į┌│Ż£ž║┌░Ą╠Ä┐╔▒Ż┤µę╗─ĻŻ¼üå┬╚╦ß▓╗ĘĆČ©┐╔ĘųĮŌŻ¼Ę┤æ¬Ą─ļxūėĘĮ│╠╩Į×ķŻ║HClO2Ī·ClO2Ī³+H++Cl®ü+H2OŻ©╬┤┼õŲĮŻ®Ż««ö1molHClO2░l╔·ĘųĮŌĘ┤æ¬ĢrŻ¼▐DęŲĄ─ļŖūėéĆöĄ╩Ū Ż«
Ż©3Ż®ėąą¦┬╚║¼┴┐╩Ū║¼┬╚Ž¹ČŠä®Ą─ę╗éĆųžę¬ųĖś╦Ż¼ėąą¦┬╚║¼┴┐Ą─Č©┴x×ķŻ║Å─HIųąč§╗»│÷ŽÓ═¼┴┐Ą─I2╦∙ąĶCl2Ą─┘|┴┐┼cųĖČ©║¼┬╚Ž¹ČŠä®Ą─┘|┴┐ų«▒╚Ż¼│Żė├░┘ĘųöĄ▒Ē╩ŠŻ«ätClO2Ą─ėąą¦┬╚║¼┴┐╩Ū Ż«
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐į┌£yČ©ųą║═Ę┤æ¬Ę┤æ¬¤ßĄ─īŹ“×ųąŻ¼Ž┬┴ąöó╩÷Õeš`Ą─╩Ū
A. Ž“ąĪ¤²▒Łųą╝ė╚ļ¹}╦߯¼£y┴┐Ą─£žČ╚×ķ¹}╦ߥ─Ų╩╝£žČ╚
B. īŹ“×ųą┐╔╩╣╦ß╗“ēA┬į▀^┴┐
C. Ž“ąĪ¤²▒Łųą╝ėēAę║ĢrŻ¼ēAę║Ą─£žČ╚æ¬┼c╦ߥ─£žČ╚ŽÓ═¼
D. ┐╔ęįė├Üõč§╗»Ōø┤·╠µÜõč§╗»ŌcŻ¼ØŌ┴“╦ß┤·╠µ¹}╦ß
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐(1)┼õŲĮč§╗»▀ĆįŁĘ┤æ¬ĘĮ│╠╩ĮŻ║
C2O![]() Ż½____MnO
Ż½____MnO![]() Ż½____HŻ½===____CO2Ī³Ż½____Mn2Ż½Ż½____H2O
Ż½____HŻ½===____CO2Ī³Ż½____Mn2Ż½Ż½____H2O
(2)ĘQ╚Ī6.0 g║¼H2C2O4Īż2H2OĪóKHC2O4║═K2SO4Ą─įćśėŻ¼╝ė╦«╚▄ĮŌŻ¼┼õ│╔250 mL╚▄ę║ĪŻ┴┐╚Īā╔Ę▌┤╦╚▄ę║Ė„25 mLŻ¼Ęųäeų├ė┌ā╔éĆÕFą╬Ų┐ųąĪŻ
ó┘Ą┌ę╗Ę▌╚▄ę║ųą╝ė╚ļĘė╠¬įćę║Ż¼Ą╬╝ė0.25 molĪżLŻŁ1NaOH╚▄ę║ų┴20 mLĢrŻ¼╚▄ę║ė╔¤o╔½ūā×ķ£\╝t╔½ĪŻįō╚▄ę║▒╗ųą║═Ą─HŻ½Ą─┐é╬’┘|Ą─┴┐×ķ________molĪŻ
ó┌Ą┌Č■Ę▌╚▄ę║ųąĄ╬╝ė0.10 molĪżLŻŁ1Ą─╦ßąįĖ▀Õi╦ßŌø╚▄ę║ĪŻ
KMnO4╚▄ę║į┌Ą╬Č©▀^│╠ųąū„________(╠ŅĪ░č§╗»ä®Ī▒╗“Ī░▀ĆįŁä®Ī▒)Ż¼įōĄ╬Č©▀^│╠________(╠ŅĪ░ąĶę¬Ī▒╗“Ī░▓╗ąĶę¬Ī▒)┴Ē╝ėųĖ╩Šä®ĪŻĄ╬ų┴16 mLĢrĘ┤æ¬═Ļ╚½Ż¼┤╦Ģr╚▄ę║Ņü╔½ė╔________ūā×ķ__________ĪŻ
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐ųŲ╚Īę╗┬╚ęę═ķūŅ║├▓╔ė├Ą─ĘĮĘ©╩Ū(ĪĪĪĪ)
A. ęę═ķ║═┬╚ÜŌĘ┤æ¬ B. ęꎮ║═┬╚ÜŌĘ┤æ¬
C. ęꎮ║═┬╚╗»ÜõĘ┤æ¬ D. ęꎮ║═┬╚ÜŌĪóÜõÜŌĘ┤æ¬
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐ĪŠīÄŽ─┴∙▒P╔ĮĖ▀╝ēųąīW2017ī├Ė▀╚²Ą┌╦─┤╬─ŻöM┐╝įćĪ┐ė╔Ž┬┴ą╩┬īŹĄ├│÷Ą─ĮYšōš²┤_Ą─╩Ū
╩┬ īŹ | ĮY šō | |
A | HClO┼cH2SO3Ę┤æ¬╔·│╔H2SO4║═HCl | ĘŪĮī┘ąįŻ║Cl>S |
B | N2▒╚░ū┴ūĘĆČ©Ą├ČÓ | ĘŪĮī┘ąįŻ║N<P |
C | į┌╝s800ĪµĢrŻ¼Įī┘Ōc┐╔Å─╚█╚┌Ą─KClųąų├ōQ│÷K | Įī┘ąįŻ║Na>K |
D | ╣żśI╔ŽļŖĮŌNa3AlF6║═Al2O3Ą─╚█╚┌╗ņ║Ž╬’Ą├ĄĮAl | Įī┘╗ŅäėąįŻ║Na>Al |
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐ęčų¬Ż║2CO(g)Ż½O2(g)===2CO2(g)ĪĪ”żHŻĮŻŁ566 kJĪżmolŻŁ1
Na2O2(s)Ż½CO2(g)===Na2CO3(s)Ż½![]() O2(g)ĪĪ”żHŻĮŻŁ266 kJĪżmolŻŁ1
O2(g)ĪĪ”żHŻĮŻŁ266 kJĪżmolŻŁ1
Ė∙ō■ęį╔Ž¤ß╗»īWĘĮ│╠╩Į┼ąöÓŻ¼Ž┬┴ąšfĘ©š²┤_Ą─╩Ū(ĪĪĪĪ)
A. COĄ─╚╝¤²¤ß×ķ283 kJ
B. ėęłD┐╔▒Ē╩Šė╔CO╔·│╔CO2Ą─Ę┤æ¬▀^│╠║═─▄┴┐ĻPŽĄ
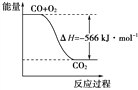
C. 2Na2O2(s)Ż½2CO2(s)===2Na2CO3(s)Ż½O2(g)ĪĪ”żH > ŻŁ532 kJĪżmolŻŁ1
D. CO(g)┼cNa2O2(s)Ę┤æ¬Ę┼│÷549 kJ¤ß┴┐ĢrŻ¼ļŖūė▐DęŲöĄ×ķ6.02Ī┴1023
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐öÓķ_1mol Hę╗HµIĪó1mol Nę╗HµIĪó1mol NĪįN µIĘųäeąĶę¬╬³╩š─▄┴┐×ķ436kJĪó391kJĪó946kJŻ¼Ū¾Ż║H2┼cN2Ę┤æ¬╔·│╔0.5molNH3╠Ņ Ż©Ī░╬³╩šĪ▒╗“Ī░Ę┼│÷Ī▒Ż®─▄┴┐ kJŻ«
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
ć°ļHīWąŻā×▀x - ŠÜ┴Ģāį┴ą▒Ē - įćŅ}┴ą▒Ē
║■▒▒╩Ī╗ź┬ōŠW▀`Ę©║═▓╗┴╝ą┼Žó┼eł¾ŲĮ┼_ | ŠW╔Žėą║”ą┼Žó┼eł¾īŻģ^ | ļŖą┼įp“_┼eł¾īŻģ^ | ╔µÜv╩Ę╠ō¤oų„┴xėą║”ą┼Žó┼eł¾īŻģ^ | ╔µŲ¾ŪųÖÓ┼eł¾īŻģ^
▀`Ę©║═▓╗┴╝ą┼Žó┼eł¾ļŖįÆŻ║027-86699610 ┼eł¾Ó]ŽõŻ║58377363@163.com