
【題目】1gH2燃燒生成液態水放出142.9KJ的熱量,表示該反應的熱化學方程式正確的是( )
A.2H2(g)+O2(g)=2H2O(l)△H=﹣142.9kJmol﹣1
B.2H2(g)+O2(g)=2H2O(l)△H=﹣571.6kJmol﹣1
C.2H2+O2=2H2O△H=﹣571.6kJmol﹣1
D.H2(g)+1/2O2(g)=H2O(g)△H=﹣285.8kJmol﹣1
科目:高中化學 來源: 題型:
【題目】下列實驗基本操作中正確的是
A. 稀釋濃硫酸時,將濃硫酸沿器壁緩慢注入水中,并不斷攪拌
B. 過濾時,漏斗里液體的液面要高于濾紙的邊緣
C. 膠頭滴管的管口直接伸入試管里滴加液體,以免外濺
D. 實驗結束后,用嘴吹滅酒精燈
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列遞變規律不正確的是( )
A.Na、Mg、Al原子的失電子能力逐漸減弱
B.Si、P、S元素的最高正化合價依次降低
C.C、N、O的原子半徑依次減小
D.Cl、Br、I的氣態氫化物的穩態性依次減弱
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學興趣小組利用如圖裝置進行“鐵與水反應”的實驗,并檢驗產物的性質,請回答下列問題:

(1)A裝置的作用是________________,B中反應的化學方程式為_____________。
(2)D的作用是____________________________________________________________。
(3)E中的現象是__________________________________________________________。
(4)A、B兩個裝置中應先點燃_______處的酒精燈,點燃E處酒精燈之前應進行的操作是_______________________________________________________________________。
【答案】 產生水蒸氣 3Fe+4H2O(g) ![]() Fe3O4+4H2 吸收未反應的水蒸氣 黑色固體變為紅色,右端管壁有水珠生成 A 收集H2,并檢驗其純度
Fe3O4+4H2 吸收未反應的水蒸氣 黑色固體變為紅色,右端管壁有水珠生成 A 收集H2,并檢驗其純度
【解析】(1)鐵與水蒸氣反應的條件是高溫,水的狀態是氣體,所以A裝置的作用是產生水蒸氣,B中是鐵與水蒸氣反應生成氫氣和四氧化三鐵,方程式為3Fe+4H2O(g)![]() Fe3O4+4H2;(2)生成的氫氣中含有水蒸氣,則D中堿石灰的作用是吸收未反應的水蒸氣;(3)氫氣還原氧化銅得到銅和水即H2+CuO
Fe3O4+4H2;(2)生成的氫氣中含有水蒸氣,則D中堿石灰的作用是吸收未反應的水蒸氣;(3)氫氣還原氧化銅得到銅和水即H2+CuO![]() Cu+H2O,所以實驗現象是硬質玻璃管中黑色固體變為紅色,硬質玻璃管右端管壁有液滴生成;(4)若先點燃B處,鐵會與氧氣先發生反應,所以須先點燃A處;氫氣是可燃性氣體混有空氣會發生爆炸,所以點燃E處酒精燈之前應進行的操作是驗證氫氣的純度。
Cu+H2O,所以實驗現象是硬質玻璃管中黑色固體變為紅色,硬質玻璃管右端管壁有液滴生成;(4)若先點燃B處,鐵會與氧氣先發生反應,所以須先點燃A處;氫氣是可燃性氣體混有空氣會發生爆炸,所以點燃E處酒精燈之前應進行的操作是驗證氫氣的純度。
【題型】實驗題
【結束】
20
【題目】某研究性學習小組為研究氯氣是否具有漂白性,設計如圖所示實驗裝置。試根據實驗裝置回答下列問題:

A、C中為干燥的有色布條,B為無色液體,D中為NaOH溶液。
(1)在常溫下,KMnO4固體可以與濃鹽酸反應生成氯氣,其反應方程式為2KMnO4+16HCl(濃)===2KCl+2MnCl2+5Cl2↑+8H2O,則其反應裝置應選用甲、乙、丙中的_______。
(2)B中的液體為____________,其作用為____________________________________。
(3)A、C中有色布條的顏色變化分別為__________________________________,A、C的實驗現象說明氯氣是否具有漂白性?________(填“是”或“否”)。
(4)D中NaOH溶液的作用是________________________________________(用離子方程式說明)。
(5)將產生的氯氣通入滴有酚酞的NaOH溶液中,溶液紅色褪去。小組內有甲、乙兩種意見:
甲:氯氣溶于水后溶液顯酸性,中和了NaOH,使溶液褪為無色;
乙:氯氣溶于水生成漂白性物質,使溶液褪為無色。
丙同學在褪色后的溶液中逐漸加入足量的NaOH溶液,溶液一直未見紅色,則______(填“甲”或“乙”)的意見正確。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將氯堿工業與燃料電池聯合能夠有效降低能源消耗,如圖是該工藝的圖示(電源及電極未標出),請回答下列問題: 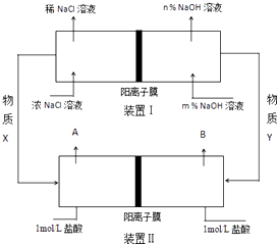
(1)電解飽和食鹽水(氯堿工業)的化學方程式為 .
(2)物質X為 , 裝置Ⅰ和Ⅱ中屬于燃料電池的是 .
(3)裝置Ⅰ中,NaOH溶液濃度m%n% (填“>”或“<”).
(4)利用裝置Ⅱ可獲得10mol/L鹽酸,該產品出口為(填“A”或“B”),請說明理由 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】室溫下如圖,關閉活塞,在左右兩室(體積相同)各充入一定量H2和Cl2 , 且恰好使兩容器內氣體密度相同,打開活塞,點燃使H2與Cl2充分反應生成氯化氫氣體:H2+Cl2=2HCl,恢復到原溫度后,下列判斷正確的是( ) 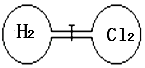
A.開始時左右兩室分子數相同
B.最終容器內無H2存在
C.反應前后H2室壓強相同
D.最終容器內密度與原來相同
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】取一定量飽和FeCl3溶液,進行如下實驗:
(1)加入少量NaOH(s),FeCl3的水解程度(填“增強”“減弱”或“不變”).
(2)將溶液加熱蒸干,并灼熱,最后得到的固體是(寫化學式).
(3)向FeCl3溶液中通入HCl(g),溶液的pH(填“增大”“減小”或“不變”),FeCl3的水解程度(填“增強”“減弱”或“不變”).
(4)向FeCl3溶液中滴加石蕊試液,現象是 .
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com