
【題目】下列說法正確的是()
A.紅外光譜只能檢測化學鍵,不能檢測官能團
B.核磁共振氫譜顯示二甲苯只有兩組吸收峰且面積比為3:2
C.煤是由苯和甲苯等有機物和無機物組成的混合物
D.石油中溶有![]() 的烷烴
的烷烴
【答案】D
【解析】
A.紅外光譜可以用來檢測物質具有的化學鍵及官能團;
B.甲苯存在三種同分異構體,鄰間對位的二甲苯;
C.煤是由有機物和少量無機物組成的復雜的混合物;
D.石油是由各種烷烴、環烷烴、芳香烴等組成的混合物,汽油是由石油分餾所得的低沸點烷烴,其分子中的碳原子數一般在![]() 范圍內,據此解題。
范圍內,據此解題。
![]() 紅外光譜可以檢測有機物具有的化學鍵和官能團,故A錯誤;
紅外光譜可以檢測有機物具有的化學鍵和官能團,故A錯誤;
B.二甲苯存在三種同分異構體,鄰間對位的二甲苯,其中對二甲苯只有兩組吸收峰且面積比為3:2,鄰二甲苯存在三組峰,間二甲苯四組峰,故B錯誤;
C.煤是由有機物和少量無機物組成的復雜的混合物,主要含有C元素,苯和甲苯等有機物是煤干餾的產物,故C錯誤;
D.石油是由各種烷烴、環烷烴、芳香烴等組成的混合物,石油中溶有![]() 的烷烴,故D正確;
的烷烴,故D正確;
答案選D。


科目:高中化學 來源: 題型:
【題目】(1)配平以下方程式
K2Cr2O7+__HC1=__KC1+__CrCl3+__H2O+__Cl2↑
以上反應中失電子的物質是_________,還原產物是______,每生成lmol這種還原產物,將有_________mol電子發生轉移.氧化劑與還原劑的物質的量之比為_________.
(2)人體內的鐵元素以Fe2+和Fe3+的形式存在。Fe2+易被吸收,所以補鐵時,應補充含Fe2+的亞鐵鹽。服用維生素C可使食物中的Fe3+轉化成Fe2+,利于人體對鐵的吸收。
Ⅰ人體中經常進行Fe2+與Fe3+的轉化,可表示為Fe2+![]() Fe3+。在過程A中,Fe2+作__________劑,過程B中,Fe3+作____________劑。
Fe3+。在過程A中,Fe2+作__________劑,過程B中,Fe3+作____________劑。
Ⅱ“服用維生素C可使食物中的Fe3+轉化為Fe2+”這句話指出,維生素C在這個反應中作_______劑,具有_____________性。
(3)已知反應:2H2S+H2SO3=2H2O+3S↓,若氧化產物比還原產物多1.6g,則冋時會生成水的質量為____g.
(4)除去Na2CO3粉末中混入的NaHCO3雜質用______方法,化學方程式為_______.
(5)向FeBr2溶液中通入足量Cl2(己知氧化性Cl2>Br2>Fe3+)化學方程式為_______
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據下列兩個熱化學方程式,回答下列問題:
2H2(g)+O2(g)![]() 2H2O(1) ΔH=571.6 kJ · mol1
2H2O(1) ΔH=571.6 kJ · mol1
C3H8(g)+5O2(g)![]() 3CO2(g)+4H2O(l) ΔH=2 220 kJ · mol1
3CO2(g)+4H2O(l) ΔH=2 220 kJ · mol1
(1)H2的燃燒熱為_______,C3H8的燃燒熱為_______。
(2)1 mol H2和2 mol C3H8組成的混合氣體完全燃燒釋放的熱量為______________。
(3)現有H2和C3H8的混合氣體共5 mol,完全燃燒時放熱3 847 kJ,則在混合氣體中H2和C3H8的體積比是_______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用14.2g無水硫酸鈉配制成500mL溶液,其物質的量濃度為__________molL-1。若從中取出50 mL,其物質的量濃度為__________ molL-1。若將這50 mL溶液用水稀釋到100 mL,所得溶液中![]() 的物質的量濃度為__________ molL-1,
的物質的量濃度為__________ molL-1,![]() 的物質的量濃度為__________ molL-1。
的物質的量濃度為__________ molL-1。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】銀白色固體A:①放在空氣中可氧化生成白色固體B;②將A點燃,火焰呈黃色,生成淡黃色固體C;③A、B、C均可與無色液體D反應,生成堿性物質E,其中A跟D反應時還可以生成可燃性氣體F,C跟D反應則生成另一種氣體G;④F和G混合后遇火可劇烈反應而發生爆炸,并生成D。據此判斷:
(1)A______,B______,C______,D________,E____,F_______,G_______。(填化學式)
(2)寫出有關反應的化學方程式:
①___________________________________________。
②__________________________________________。
③__________________________________________。
④__________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某小組同學探究Cu和H2O2的反應。
(猜想預測)
猜想1:Cu與H2O2不發生反應;
猜想2:Cu與H2O2可能發生氧化還原反應,H2O2作氧化劑。
(實驗探究)
實驗ⅰ:向裝有0.5 g Cu的燒杯中加入20 mL 30% H2O2溶液,一段時間內無明顯現象,10 小時后,溶液中有少量藍色渾濁,Cu片表面附著少量藍色固體。
(1)通過該實驗證明了猜想2成立,寫出該反應的化學方程式:________。
(繼續探究)
針對該反應速率較慢,小組同學查閱資料,設計并完成了下列實驗。
資料:Cu2+ + 4NH3 [ Cu(NH3)4] 2+ ,[ Cu(NH3)4] 2+為深藍色;Cu(OH)2可溶于氨水形成深藍色溶液。
裝置 | 序號 | 試劑a | 現象 |
| ⅱ | 20 mL 30% H2O與4 mL 5 mol/L H2SO4 混合液 | Cu表面很快生產少量氣泡,溶液逐漸變藍,產生較多氣泡 |
ⅲ | 20 mL 30% H2O2與4 mL5 mol/L氨水混合液 | 溶液立即變為深藍色,產生大量氣泡,Cu表面有少量藍色不溶物 |
(2)實驗ⅱ中:溶液變藍的原因是________(用化學用語解釋);經檢驗產生的氣體為氧氣,產生氧氣的原因是________。
(3)對比實驗ⅰ和ⅲ,為探究氨水對Cu的還原性或H2O2氧化性的影響,該同學利用如圖裝置繼續實驗。
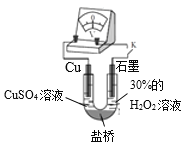
已知:電壓大小反映了物質氧化還原性強弱的差異;物質氧化性與還原性強弱差異越大,電壓越大。
a.K閉合時,電壓為x。
b.向U型管右側溶液中滴加氨水后,電壓不變。
c.繼續向U型管左側溶液中滴加氨水后,電壓增大了y。
該實驗的結論:_________。利用該方法也可證明酸性增強可提高H2O2的氧化性,導致Cu溶解速率加快。
(4)對比實驗ⅱ和ⅲ,實驗ⅲ中產生氧氣速率明顯更快,可能的原因是_______。
(5)實驗ⅲ有少量藍色不溶物,小組同學加入少量NH4Cl可使其溶解,結合文字和化學用語解釋不溶物溶解的原因:________。
(6)基于以上實驗,影響Cu與H2O2反應速率的因素有________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鋼鐵“發藍”是指在鋼鐵的表面形成一層四氧化三鐵的技術過程。其中第一步反應為:3Fe+ NaNO2+ 5 NaOH= 3Na2FeO2+ H2O+ NH3↑。關于該反應說法正確的是![]()
A.反應中N元素被氧化
B.NaFeO2既是氧化產物也是還原產物
C.整個反應過程中每有![]() 參加反應就轉移
參加反應就轉移![]() 電子
電子
D.氧化劑與還原劑的物質的量之比為3:1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將![]() 鋅粒投入500mL 2mol/L的硫酸溶液中,試計算:
鋅粒投入500mL 2mol/L的硫酸溶液中,試計算:
(1)產生的氫氣在標準狀況下的體積是__________;
(2)忽略溶液體積變化體積,反應后溶液中氫離子濃度是__________;
(3)要配制500mL 2mol/L的硫酸溶液,需用質量百分數為98%,密度為1.84g/cm3濃硫酸_______![]() 保留三位有效數字
保留三位有效數字![]() 。
。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業上60%的鎂來自海水,從海水中提取鎂工藝流程如圖所示,下列說法正確的是( )
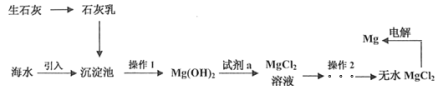
A.該工藝流程涉及的反應有分解反應、化合反應和置換反應
B.操作1為過濾,實驗室里為加快過濾速度應用玻璃棒攪拌液體
C.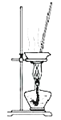 操作2實驗室可用該裝置對MgCl2溶液進行蒸發濃縮,再冷卻結晶獲得無水MgCl2
操作2實驗室可用該裝置對MgCl2溶液進行蒸發濃縮,再冷卻結晶獲得無水MgCl2
D.該工藝的優點是原料來源廣泛,同時獲得重要的化工原料氯氣
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com