
【題目】下列關于硫及其化合物的說法中,正確的是( )
A. 硫是一種易溶于水的淡黃色晶體
B. 將![]() 通入硝酸酸化的
通入硝酸酸化的![]() 溶液中,有白色沉淀生成,再加鹽酸后沉淀消失
溶液中,有白色沉淀生成,再加鹽酸后沉淀消失
C. 除去![]() 中混有的
中混有的![]() 、HCl氣體可以選用飽和的
、HCl氣體可以選用飽和的![]() 溶液
溶液
D. 濃硫酸、濃硝酸、稀硝酸都是氧化性酸,常溫下都能使金屬鐵、鋁鈍化
【答案】C
【解析】
A.硫是一種淡黃色固體,不溶于水,微溶于酒精,容易溶于CS2,A錯誤;
B.SO2具有還原性,會被硝酸氧化為硫酸,硫酸與溶液中的BaCl2發生反應產生BaSO4,BaSO4既不溶于水,也不溶于酸,B錯誤;
C.SO3與水反應產生H2SO4,硫酸與飽和的NaHSO3溶液發生反應產生SO2氣體,HCl溶于水,也會與溶液中的NaHSO3發生反應產生SO2氣體,達到除雜凈化的目的,C正確;
D.濃硫酸、濃硝酸、稀硝酸都是氧化性酸,但在常溫下,濃硫酸、濃硝酸可將Fe、Al表面氧化產生一層致密的氧化物薄膜,阻止金屬的進一步氧化,即能使金屬鐵、鋁鈍化,而稀硝酸與Fe、Al會發生劇烈反應,不會產生鈍化現象,D錯誤;
故合理選項是C。


科目:高中化學 來源: 題型:
【題目】(化學——選修3:物質結構與性質)
鎳及其化合物在工業生產和科研領域有重要的用途。請回答下列問題:
(1)基態 Ni 原子中,電子填充的能量最高的能級符號為______,價層電子排布式為________。
(2)Ni(CO)4 常用作制備高純鎳粉,其熔點為-19.3 ℃, 沸點為 43 ℃。則:
①Ni(CO)4 的熔、沸點較低的原因為________。
②寫出一種與CO 互為等電子體的分子的化學式________。
③Ni(CO)4中 σ 鍵和 π 鍵的數目之比為________。
(3)NiSO4 常用于電鍍工業,其中 SO42-的中心原子的雜化軌道類型為________,該離子中雜化軌道的作用是________。
(4)氧化鎳和氯化鈉的晶體結構相同,可看成鎳離子替換鈉離子,氧離子替換氯離子。 則:
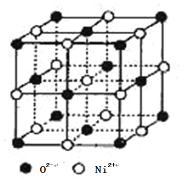
①鎳離子的配位數為________。
②天然的和人工合成的氧化鎳常存在各種缺陷,某缺陷氧化鎳的組成為Ni0.97O(相對分子質量為73), 其中 Ni 元素只有+2 和+3 兩種價態, 兩種價態的鎳離子數目之比為________;若阿伏加德羅常數的值為NA,晶體密度為 ρ g·cm-3,則該晶胞中最近的 O2-之間的距離為________pm(列出表達式)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某無色透明的強酸性溶液中,能大量共存的一組離子是
A. Mg2+、A13+、SO42-、NO3- B. Na+、HCO3-、K+、SO42-
C. MnO4-、K+、SO42-、Na+ D. NH4+、Fe2+、Cl-、NO3-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】向1LFeBr2溶液中,通入1.12L(標態下)的Cl2,測得溶液中c(Br-)=3c(Cl-),反應過程中溶液的體積變化不計,則下列說法中正確的是
A. 原溶液的濃度為0.1mol/L B. 反應后溶液中c(Fe3+)=0.1mol/L
C. 反應后溶液中c(Fe3+)=c(Fe2+) D. 原溶液中c(Br-)=0.4mol/L
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列實驗現象所對應的離子方程式不正確的是( )
選項 | 實驗 | 現象 | 離子方程式 |
A | 將稀硫酸滴加到KI淀粉溶液中 | 在空氣中放置一段時間后溶液呈藍色 |
|
B | 用硫氰化鉀溶液檢驗某溶液中含有 | 溶液變成紅色 |
|
C | 酸性 | 溶液紫色褪去 |
|
D | 將 | 有白色沉淀生成 |
|
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列各組離子能大量共存的是
A.Cu2+、Mg2+、SO42-、OH-B.Na+、H+、SO42-、ClO-
C.MnO4-、Al3+、Fe2+、SO42-D.Na+、NO3-、K+、SO42-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】ClO2氣體是一種常用的消毒劑,我國從2000年起逐步用ClO2代替氯氣對飲用水進行消毒.
(1)消毒水時,ClO2還可將水中的Fe2+、Mn2+等轉化成Fe(OH)3和MnO2等難溶物除去,在這個過程中,Fe2+、Mn2+的化合價升高,說明ClO2具有______性.
(2)工業上可以通過下列方法制取ClO2,請完成該化學反應方程式:2KClO3+SO2==2ClO2+_____。
(3)使Cl2和H2O(g)通過灼熱的炭層,生成HCl和CO2,寫出化學方程式:_____________
(4)自來水廠用ClO2處理后的水中,要求ClO2的濃度在0.1~0.8mg/L之間。碘量法可以檢測水中ClO2的濃度,步驟如下:
Ⅰ取一定體積的水樣,加入一定量的碘化鉀,再用氫氧化鈉溶液調至中性,并加入淀粉溶液,溶液變藍。
Ⅱ加入一定量的Na2S2O3溶液。(已知:2S2O32-+I2== S4O62-+2I-)
Ⅲ加硫酸調節水樣pH至1~3。
操作時,不同pH環境中粒子種類如圖所示:

請回答:
①操作Ⅰ中反應的離子方程式是_____。
②在操作Ⅲ過程中,溶液又呈藍色,反應的離子方程式是_____。
③若水樣的體積為1.0L,在操作Ⅱ時消耗了1.0×10-3mol/L的Na2S2O3溶液10ml,則水樣中ClO2的濃度是_____ mg/L。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為探究某有機化合物A的結構及性質,進行如下實驗:
I.確定分子式
(1)將有機物A置于氧氣流中充分燃燒實驗測得:生成5.4gH2O和8.8gCO2,消耗氧氣6.72L(標準狀況下),則A中各元素的原子個數比為______________。
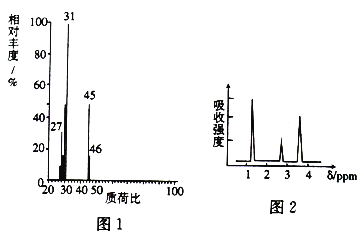
(2)A的質譜圖如圖1所示,則A的分子式為_____________。
II.結構式的確定
(3)經測定,A的核磁共振氫譜圖如圖2所示,則A的結構簡式為____________。
III.性質實驗
(4)A在一定條件下可脫水生成無色氣體B,該反應的化學方程式為____________。
(5)體育比賽中當運動員肌肉扭傷時,隊醫隨即用氯乙烷(沸點為12.27℃)對受傷部位進行局部冷凍麻醉。制備氯乙烷的一個好方法是用A與SOCl2加熱下反應,同時生成二氧化硫和氯化氫兩種氣體,則該反應的化學方程式為____________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com