
【題目】下列描述中正確的是( )
A. 氮原子的價電子排布圖:![]()
B. 價電子排布為4s24p3的元素位于第四周期第ⅤA族,是p區元素
C. 2p和3p軌道形狀均為啞鈴形,能量也相等
D. 鈉原子由1s22s22p63s1→1s22s22p63p1時,原子釋放能量,由基態轉化成激發態
【答案】B
【解析】A.根據“洪特規則”可知,2p軌道電子的自旋方向應該相同,正確的電子排布圖為:![]() ,A錯誤;B.價電子排布為4s24p3的元素有4個電子層、最外層電子數為5,位于第四周期第ⅤA族,最后填充p電子,是p區元素,B正確;C.2p和3p軌道形狀均為啞鈴形,但是原子軌道離原子核越遠,能量越高,2p軌道能量低于3p,C錯誤;D.基態Na的電子排布式為1s22s22p63s1,由基態轉化成激發態1s22s22p63p1時,電子能量增大,需要吸收能量,D錯誤;答案選B;
,A錯誤;B.價電子排布為4s24p3的元素有4個電子層、最外層電子數為5,位于第四周期第ⅤA族,最后填充p電子,是p區元素,B正確;C.2p和3p軌道形狀均為啞鈴形,但是原子軌道離原子核越遠,能量越高,2p軌道能量低于3p,C錯誤;D.基態Na的電子排布式為1s22s22p63s1,由基態轉化成激發態1s22s22p63p1時,電子能量增大,需要吸收能量,D錯誤;答案選B;
點睛;本題考查原子核外電子的排布、原子核外電子的躍遷,注意掌握樣子核外電子的躍遷過程中能量變化,核外電子排布規律及電子排布與元素位置的關系,注意洪特規則的應用。


 名師導航單元期末沖刺100分系列答案
名師導航單元期末沖刺100分系列答案 名校名卷單元同步訓練測試題系列答案
名校名卷單元同步訓練測試題系列答案科目:高中化學 來源: 題型:
【題目】下列有關實驗操作的敘述錯誤的是( )
A. 過濾操作中,漏斗的尖端應接觸燒杯內壁
B. 從滴瓶中取用試劑時,滴管的尖嘴可以接觸試管內壁
C. 滴定接近終點時,滴定管的尖嘴可以接觸錐形瓶內壁
D. 向容量瓶轉移液體時,導流用玻璃棒可以接觸容量瓶內壁
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】短周期主族元素A、B、C、D、E原子序數依次增大 ,A是元素周期表中原子半徑最小的元素,B是形成化合物種類最多的元素,C原子的最外層電子數是次外層電子數的3倍,D是同周期中金屬性最強的元素,E的負一價離子與C的某種氫化物W分子含有相同的電子數。
(1)A、C、D形成的化合物中含有的化學鍵類型為_______。W的電子式_________。
(2)在某溫度下容積均為2 L的三個密閉容器中,按不同方式投入反應物,保持恒溫恒容,使之發生反應:2A2(g)+BC(g)![]() X(g) H=-Q kJ/mol(Q>0,X為A、B、C三種元素組成的一種化合物)。初始投料與各容器達到平衡時的有關數據如下:
X(g) H=-Q kJ/mol(Q>0,X為A、B、C三種元素組成的一種化合物)。初始投料與各容器達到平衡時的有關數據如下:
實驗 | 甲 | 乙 | 丙 |
初始投料 | 2 mol A2、1 mol BC | 1 mol X | 4 mol A2、2 mol BC |
平衡時n(X) | 0.5 mol | n2 | n3 |
反應的能量變化 | 放出Q1kJ | 吸收Q2kJ | 放出Q3kJ |
體系的壓強 | P1 | P2 | P3 |
反應物的轉化率 |
|
|
|
① 計算該溫度下此反應的平衡常數K =_________________。
②三個容器中的反應分別達平衡時下列各組數據關系正確的是___________(填字母)。
A.α1+α2=1 B.Q1+Q2=Q C.α3<α1
D.P3<2P1=2P2 E.n2<n3<1.0 mol F.Q3=2Q1
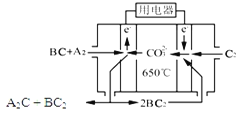
(3)熔融碳酸鹽燃料電池(MCFC)是一種高溫燃料電池,被稱為第二代燃料電池,是未來民用發電的理想選擇方案之一,其工作原理如圖所示。現以A2(g)、BC(g)為燃料,以一定比例Li2CO3和Na2CO3低熔混合物為電解質。寫出該碳酸鹽燃料電池(MCFC)正極的電極反應式____________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】測得某溶液中僅含Cu2+、K+、SO42-、Cl-四種離子,且陽離子的數量比為Cu2+:K+=3:4,則SO42-:Cl-的比值可能是
A. 3:2 B. 2:1 C. 1:8 D. 任意比
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某烴與氫氣發生反應后能生成(CH3)2CHCH2CH3,則該烴不可能是( )
A. 2-甲基-2-丁烯 B. 3-甲基-1-丁炔
C. 2-甲基-2-丁炔 D. 2-甲基-1,3-丁二烯
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于物質用途的說法中,不正確的是( )
A. Fe2O3可以做油漆的顏料
B. 王水可以雕刻玻璃
C. Al2O3可用作耐火材料
D. 赤鐵礦可用作煉鐵的原料
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鈹及其化合物的應用正日益被重視。
(l)最重要的含鈹礦物是綠柱石,含2%鉻(Cr)的綠柱石即為祖母綠。基態Cr原子價電子的軌道表示式為_____________________。
(2)鈹與相鄰主族的鋁元素性質相似。下列有關鈹和鋁的敘述正確的有_______(填標號)。
A.都屬于p區主族元素 B.電負性都比鎂大
C.第一電離能都比鎂大 D.氯化物的水溶液pH均小于7
(3)鈹、鋁晶體都是由金屬原子密置層在三維空間堆積而成(最密堆積)。鈹的熔點(155lK)比鋁的熔點(930K)高,原因是__________________________。
(4)氯化鈹在氣態時存在BeC12分子(a)和二聚分子(BeCl2)2(b),固態時則具有如下圖所示的鏈狀結構(c)。

①a屬于__________(填“極性”或“非極性”)分子。
②二聚分子(BeCl2)2中Be原子的雜化方式相同,且所有原子都在同一平面上。b 的結構式為________________________________ (標出配位鍵)。
③c中Be原子的雜化方式為__________。
④氯化鈹晶體中存在的作用力有_____(填標號)。
A.范德華力 B. σ鍵 C.極性鍵 D.非極性鍵 E.離子鍵
(5)BeO立方晶胞如下圖所示。

若BeO晶體的密度為dg/cm3,則晶胞參數a =______nm (列出計算式即可)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溫度下,在固定容積的密閉容器中,可逆反應A(g)+3B(g)![]() 2C(g)達到平衡時,各物質的物質的量之比是n(A)∶n(B) ∶n(C)=2∶2∶l。保持溫度不變,以2∶2∶1的物質的量之比再充入A,B,C,則( )
2C(g)達到平衡時,各物質的物質的量之比是n(A)∶n(B) ∶n(C)=2∶2∶l。保持溫度不變,以2∶2∶1的物質的量之比再充入A,B,C,則( )
A. 平衡向正方向移動 B. 平衡不發生移動
C. C的體積分數減小 D. C的體積分數不變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】短周期主族元素A、B、C、D、E原子序數依次增大 ,A是元素周期表中原子半徑最小的元素,B是形成化合物種類最多的元素,C原子的最外層電子數是次外層電子數的3倍,D是同周期中金屬性最強的元素,E的負一價離子與C的某種氫化物W分子含有相同的電子數。
(1)A、C、D形成的化合物中含有的化學鍵類型為_______。W的電子式_________。
(2)在某溫度下容積均為2 L的三個密閉容器中,按不同方式投入反應物,保持恒溫恒容,使之發生反應:2A2(g)+BC(g)![]() X(g) H=-Q kJ/mol(Q>0,X為A、B、C三種元素組成的一種化合物)。初始投料與各容器達到平衡時的有關數據如下:
X(g) H=-Q kJ/mol(Q>0,X為A、B、C三種元素組成的一種化合物)。初始投料與各容器達到平衡時的有關數據如下:
實驗 | 甲 | 乙 | 丙 |
初始投料 | 2 mol A2、1 mol BC | 1 mol X | 4 mol A2、2 mol BC |
平衡時n(X) | 0.5 mol | n2 | n3 |
反應的能量變化 | 放出Q1kJ | 吸收Q2kJ | 放出Q3kJ |
體系的壓強 | P1 | P2 | P3 |
反應物的轉化率 |
|
|
|
① 計算該溫度下此反應的平衡常數K =_________________。
②三個容器中的反應分別達平衡時下列各組數據關系正確的是___________(填字母)。
A.α1+α2=1 B.Q1+Q2=Q C.α3<α1
D.P3<2P1=2P2 E.n2<n3<1.0 mol F.Q3=2Q1
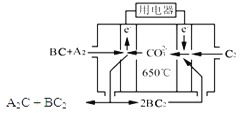
(3)熔融碳酸鹽燃料電池(MCFC)是一種高溫燃料電池,被稱為第二代燃料電池,是未來民用發電的理想選擇方案之一,其工作原理如圖所示。現以A2(g)、BC(g)為燃料,以一定比例Li2CO3和Na2CO3低熔混合物為電解質。寫出該碳酸鹽燃料電池(MCFC)正極的電極反應式____________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com