
某溫度時,Ag2SO4在水溶液中的沉淀溶解平衡曲線如圖所示,下列說法中不正確的是
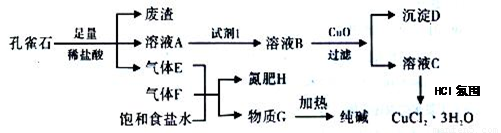

A.b點對應的Ksp等于c點對應的Ksp
B.采取蒸發溶劑的方法可以使溶液從a點變到b點
C.該溫度下,Ag2SO4的溶度積常數(Ksp)為1.6×10-5(mol·L-1)3
D.0.02mol·L-1的AgNO3溶液與的0. 2mol·L-1的Na2SO4溶液等體積混合不會生成沉淀
B
【解析】
試題分析:溶度積常數只與溫度有關系,A正確;B不正確,因為在蒸發過程中,兩種離子的濃度都是增加的;根據b點對應的離子濃度可知,該溫度下,Ag2SO4的溶度積常數(Ksp)為1.6×10-5(mol·L-1)3, C正確;0.02mol·L-1的AgNO3溶液與的0. 2mol·L-1的Na2SO4溶液等體積混合后Ag+和SO42-濃度分別是0.01mol/L和0.01mol/L,則(0.01)2×0.01=1×10-6<1.6×10-5,因此沒有沉淀生成,D正確,答案選B。
考點:考查溶度積常數的有關判斷、應用和計算
點評:該題是高考中的常見題型,屬于中等難度的試題。主要是考查學生對溶度積常數知識的熟悉掌握程度,以及靈活運用溶度積常數知識解決實際問題的能力。該題綜合性強,側重對學生解題能力的培養和訓練,有利于培養學生的邏輯推理能力。


科目:高中化學 來源: 題型:
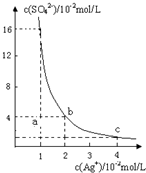 某溫度時,Ag2SO4在水溶液中的沉淀溶解平衡曲線如圖所示:
某溫度時,Ag2SO4在水溶液中的沉淀溶解平衡曲線如圖所示:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com