
【題目】在有機物分子中,若某個碳原子連接4個不同的原子或原子團,則將這種碳原子稱為“手性碳原子”.凡有一個手性碳原子的物質一定具有光學活性.物質有光學活性,它發生下列反應后生成的有機物仍有光學活性的是( ) 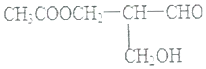
A.與NaOH溶液共熱
B.與甲酸發生酯化反應
C.與堿性Cu(OH)2懸濁液反應
D.在催化劑存在下與H2作用
【答案】B
【解析】解:A.如果該物質和NaOH溶液共熱后的產物中次亞甲基連接兩個﹣CH2OH,所以沒有手性碳原子,故A不選; B.與甲酸發生酯化反應后的產物中次亞甲基連接﹣H、﹣CHO、﹣CH2OH、CH3COOCH2﹣,所以有手性碳原子,故B選;
C.與堿性Cu(OH)2懸濁液反應后的產物中次亞甲基兩個﹣CH2OH,所以沒有手性碳原子,故C不選;
D.在催化劑存在下與H2作用,醛基被還原生成﹣CH2OH,所以次亞甲基還原兩個﹣CH2OH,沒有手性碳原子,故D不選;
故選B.
【考點精析】關于本題考查的有機物的結構和性質,需要了解有機物的性質特點:難溶于水,易溶于汽油、酒精、苯等有機溶劑;多為非電解質,不易導電;多數熔沸點較低;多數易燃燒,易分解才能得出正確答案.


科目:高中化學 來源: 題型:
【題目】有機物A可由葡萄糖發酵得到,也可從酸牛奶中提取.純凈的A為無色粘稠液體,易溶于水.為研究A的組成與結構,進行了如下實驗: ①稱取A 9.0g,升溫使其汽化,測其密度是相同條件下H2的45倍
②將此9.0gA在足量純O2充分燃燒,并使其產物依次緩緩通過濃硫酸、堿石灰,發現兩者分別增重5.4g和13.2g.
③另取A 9.0g,跟足量的NaHCO3粉末反應,生成2.24LCO2(標準狀況),若與足量金屬鈉反應則生成2.24LH2(標準狀況).
④核磁共振氫譜顯示A分子中有4種不同環境的氫原子,且4種氫原子個數比為3:1:1:1.
根據以上實驗結果,回答下列問題.
(1)A的分子結構簡式為;寫出A分子中官能團的名稱;
(2)A的系統命名是;
(3)A可在濃硫酸催化下生成一種六元環酯,寫出該反應的化學方程式;
(4)A的一種同分異構體B與A具有相同的官能團,B分子經過如下兩步反應可得到一種高分子化合物D,B ![]() C
C ![]() D,寫出D的結構簡式 .
D,寫出D的結構簡式 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】第四周期中的18中元素具有重要的用途,在現代工業中備受青睞.
(1)鉻是一種硬二脆,抗腐蝕性強的金屬,常用于電鍍和制造特種鋼.基態Cr原子中,電子占據最高能層的符號為 , 該能層上具有的原子軌道數為 , 電子數為 ,
(2)第四周期元素的第一電離能隨原子序數的增大,總趨勢是逐漸增大的,30Zn與31Ga的第一電離能是否符合這一規律?(填“是”或“否”),原因是(如果前一問填“是”,此問可以不答)
(3)鎵與第VA族元素可形成多種新型人工半導體材料,砷化鎵(GaAs)就是其中一種,其晶體結構如下圖所示(白色球代表As原子).在GaAs晶體中,每個Ga原子與個As原子相連,與同一個Ga原子相連的As原子構成的空間構型為; 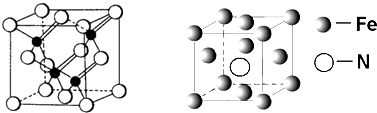
(4)與As同主族的短周期元素是N、P.AsH3中心原子雜化的類型;一定壓強下將AsH3和NH3 . PH3的混合氣體降溫是首先液化的是 , 理由是;
(5)鐵的多種化合物均為磁性材料,氮化鐵石期中一種,某氮化鐵的井胞結構如圖所示,則氮化鐵的化學式為;設晶胞邊長為acm,阿伏加德羅常數為NA , 該晶體的密度為g.cm﹣3(用含a和NA的式子表示)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】圖為①⑥六種烴分子的模型(小黑球代表碳原子,短線代表共價鍵,氫原子省略)下列說法中不正確的是( ) 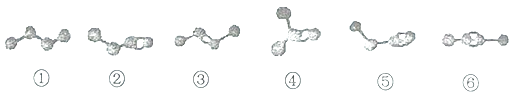
A.烴②、③、④的分子式均為C4H8 , 三者互為同分異構體
B.烴⑤和⑥的分子式均為C4H6 , 二者互為同分異構體
C.烴②、③、⑤、⑥分別與足量氧氣發生加成反應,均可得到烴①
D.等物質的量的烴②和⑤分別在氧氣中完全燃燒,烴⑤消耗的氧氣多
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列化學反應既屬于氧化還原反應,且水做氧化劑的是( )
A. 2F2+2H2O=4HF+O2 B. 2Na+2H2O=2NaOH+H2↑
C. CaO+H2O=Ca(OH)2 D. H2+CuO = Cu+H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】銅是人類最早使用的金屬之一,請結合已有知識回答下列問題:
(1)電子工業常用30%的FeCl3溶液腐蝕敷在絕緣板上的銅箔,制造印刷電路板,寫出FeCl3溶液與金屬銅發生反應的離子方程式__________________________。
(2)銅能與濃硫酸反應,寫出反應的化學方程式_______________________;將生成的氣體通入硫化氫水溶液中,其現象為__________________________。
(3)銅能與濃硝酸反應,寫出反應的離子方程式___________________;用干燥大試管集滿NO2(標準狀況下),倒置于水槽中,假設進入試管內的溶液不擴散到水槽中,則試管中溶質的物質的量濃度是______________________molL-1;
(4)工業上火法煉銅過程中發生的主要反應為:2Cu2O+Cu2S=6Cu+SO2↑,當生成19.2 g Cu時,反應轉移電子_________________mol。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】聚合物 ![]() (W是鏈節中的部分結構)是一類重要的功能高分子材料.聚合物 X是其中的一種,轉化路線如圖:
(W是鏈節中的部分結構)是一類重要的功能高分子材料.聚合物 X是其中的一種,轉化路線如圖: 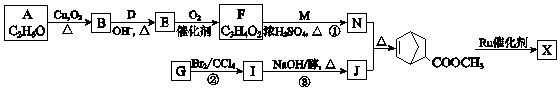
已知:
i.R1CHO+R2CH2CHO ![]()
![]()
ii. ![]()
iii.R1CH=CHR2+R3CH=CHR4 ![]() R1CH=CHR4+R3CH=CHR2
R1CH=CHR4+R3CH=CHR2
(R代表烴基或氫原子)
(1)A的結構簡式是 .
(2)B所含的官能團名稱是 .
(3)E的結構簡式是 .
(4)①的化學方程式是 .
(5)②的反應類型是 .
(6)J是五元環狀化合物,③的化學方程式是 .
(7)X的結構簡式是 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】苯甲醇與苯甲酸是重要的化工原料,可通過苯甲醛在氫氧化鈉水溶液中的歧化反應制得,反應式為: 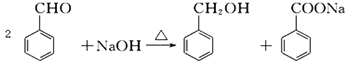
某研究小組在實驗室制備苯甲醇與苯甲酸,反應結束后對反應液按下列步驟處理: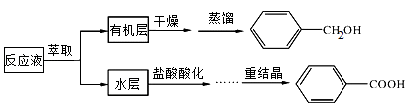
重結晶過程:溶解→活性炭脫色→趁熱過濾→冷卻結晶→抽濾→洗滌→干燥
已知:苯甲醇易溶于乙醚、乙醇,在水中溶解度較小.
請根據以上信息,回答下列問題:
(1)分離苯甲醇與苯甲酸鈉時,合適的萃取劑是 , 簡述從分液漏斗中取出上層溶液的方法 . 萃取分液后,所得水層用鹽酸酸化的目的是 .
(2)苯甲酸在A,B,C三種溶劑中的溶解度(s)隨溫度變化的曲線如圖所示: 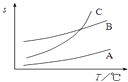
重結晶時,合適的溶劑是 , 重結晶過程中,趁熱過濾的作用是: .
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com