
【題目】配制某物質的量濃度的溶液時,下列情況會造成所配溶液濃度偏小的是
A. 容量瓶中有蒸餾水B. 溶液轉移至容量瓶時,未洗滌玻璃棒和燒杯
C. 溶液未冷至室溫就定容D. 定容時俯視
 小學生10分鐘口算測試100分系列答案
小學生10分鐘口算測試100分系列答案科目:高中化學 來源: 題型:
【題目】一定條件下,將3molA和l mol B兩種氣體混合于固定容積為2L的密閉容器中,發生如下反應:3A(g)+B(g)C(g)+2D(s).2min末該反應達到平衡,生成D的物質的量隨時間變化情況如圖.下列判斷正確的是( ) 
A.若混合氣體的密度不再改變時,該反應不一定達到平衡狀態
B.2 min后,加壓會使正反應速率加快,逆反應速率變慢,平衡正向移動
C.反應過程中A和B的轉化率之比為3:1
D.開始到平衡,用A表示該反應的化學反應速率為0.3molL﹣1min﹣1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】回收鉛蓄電池的電極填充物(鉛膏,主要含PbO、PbO2、PbSO4),可制備熱穩定劑三鹽基硫酸鉛(組成可表示為3PbOPbSO4H2O),其實驗流程如下: 
(1)物質X可以循環利用,該物質是 . 最后一次過濾之后需要洗滌,檢驗三鹽基硫酸鉛是否洗凈的方法是 .
(2)從濾液A可提取出一種含結晶水的鈉鹽副產品.若檢驗該晶體中結晶水的含量,所需的硅酸鹽材質儀器有、、、玻璃棒、石棉網、干燥器等.
(3)流程中不直接利用H2SO4溶液與PbO、PbCO3反應制取PbSO4 , 原因可能是 .
(4)生成三鹽基硫酸鉛的離子反應方程式為 .
(5)向鉛膏漿液中加入Na2SO4溶液的目的是將其中的PbO2還原為PbO.若實驗中所取鉛膏的質量為47.8g,其中PbO2的質量分數為15.0%,則要將PbO2全部還原,至少需加mL 1.0molL﹣lNa2SO3溶液.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】物質在水中可能存在電離平衡、鹽的水解平衡和沉淀的溶解平衡,它們都可看作化學平衡.請根據所學知識回答:
(1)NH4Cl溶液中各離子的濃度由大到小的順序是 .
(2)常溫下測得NaHCO3溶液的pH>7,其溶液顯堿性的原因是:(用離子反應方程式表示).
(3)實驗室中配制FeCl3溶液時通常需要向其中加入 , 其目的是;
(4)若將NaHCO3溶液和FeCl3溶液混合,會產生紅褐色沉淀和無色氣體,該反應的離子反應方程式為: .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列圖示與對應的敘述相符的是( )
A.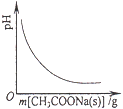
向CH3COOH溶液中逐步加入CH3COONa固體后,溶液pH的變化
B.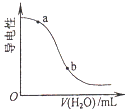
向CH3COOH溶液中加水時溶液的導電性變化,則CH3COOH溶液的pH:a>b
C.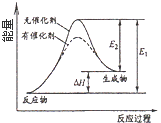
催化劑能改變化學反應的焓變
D.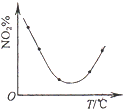
等量NO2在容積相同的恒容密閉容器中,不同溫度下分別發生反應:2NO2(g)N2O4(g),相同時間后測得NO2含量的曲線,則該反應的△H<0
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某同學設計如下元素周期表,以下說法正確的是( )
A.X、Y、Z元素分別為N、P、O
B.白格中都是主族元素,灰格中都是副族元素
C.原子半徑:Z>X>Y
D.X、Y、Z的氣態氫化物中最穩定的是Y的氫化物
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com