
【題目】向10 mL 0.1 mol·L-1的CuSO4溶液中加入10 mL 0.15 mol·L-1的NaOH溶液時,產生一種藍色沉淀。經測定溶液中的Cu2+已幾乎沉淀完全。則該沉淀的主要成分是 ( )
A.Cu(OH)2B.Cu2(OH)2SO4
C.3Cu(OH)2·CuSO4D.Cu(OH)2·3CuSO4
科目:高中化學 來源: 題型:
【題目】下列各組離子在指定溶液中可以大量共存的是( )
A. pH=11的溶液中:CO32-、Na+、AlO2+、NO3-
B. 加入Al放出H2的溶液中:SO42-、NH4+、Na+、I-
C. .pH=7溶液中:SO42-、Na+、K+、ClO-
D. 無色溶液中:K+、SO42-、Cu2+、Cl-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某學生用已知物質的量濃度的鹽酸來測定未知物質的量濃度的NaOH溶液時,選擇酚酞作指示劑。請填寫下列空白。
(1)用標準的鹽酸滴定待測的NaOH溶液時,左手握酸式滴定管的活塞,右手搖動錐形瓶,眼睛注視______________,直到因加入一滴鹽酸后,溶液由________色變為________色,并________為止。
(2)下列操作中可能使所測NaOH溶液的濃度數值偏低的是__________。
A.酸式滴定管未用標準鹽酸潤洗就直接注入標準鹽酸
B.滴定前盛放NaOH溶液的錐形瓶用蒸餾水洗凈后沒有干燥
C.酸式滴定管在滴定前有氣泡,滴定后氣泡消失
D.讀取鹽酸體積時,開始仰視讀數,滴定結束時俯視讀數
(3)若滴定開始和結束時,酸式滴定管中的液面如圖所示,則起始讀數為_______mL,終點讀數為_______mL,所用鹽酸溶液的體積為_______mL。
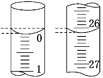
(4)某學生根據3次實驗分別記錄有關數據如下表:
滴定 次數 | 待測NaOH溶液的體積/mL | 0.100 0 mol·L-1 鹽酸的體積/mL | ||
滴定前讀數 | 滴定后讀數 | 溶液體積/mL | ||
第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
依據上表數據列式計算該NaOH溶液的物質的量濃度__________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】圖示中物質轉化最終生成乙酸和高分子涂料膠黏劑Y的合成路線如下(部分反應條件已省略):
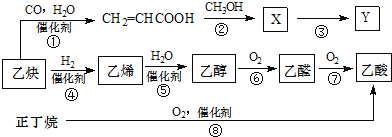
(1)化合物CH2═CHCOOH中所含官能團名稱為_____________和____________;
(2)正丁烷的一種同分異構體的結構簡式為_____________;Y的結構簡式為_____________;
(3)圖中8步反應中,原子利用率沒有達到100%的為_____________(填序號)。
(4)寫出下列反應的化學方程式(注明反應條件):反應⑥__________________________;反應⑧為(同時有水生成)_______________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關有機物的結構、性質的敘述正確的是( )
A. 苯、油脂均不能使酸性KMnO4溶液褪色
B. 甲烷和C12的反應與乙烯和Br2的反應屬于同一類型的反應
C. 乙醇、乙酸均能與Na反應放出H2,二者分子中官能團相同
D. 葡萄糖、果糖的分子式均為C6H12O6,二者互為同分異構體
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】往含0.2mol NaOH和0.1mol Ca(OH)2的溶液中持續穩定地通入CO2氣體,當通入氣體為6.72L(S.T.P)時立即停止,則這一過程中,溶液中離子的物質的量和通入CO2氣體的體積關系正確的圖象是(氣體的溶解忽略不計)( )
A.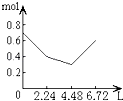
B.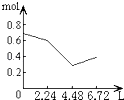
C.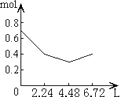
D.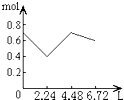
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】PCl3和PCl5都是重要的化工原料。將PCl3(g)和Cl2(g)充入體積不變的2 L密閉容器中,在一定條件下發生下述反應,10 min時達到平衡:PCl3(g) + Cl2(g)![]() PCl5(g)有關數據如下,下列判斷不正確的是
PCl5(g)有關數據如下,下列判斷不正確的是
PCl3(g) | Cl2(g) | PCl5(g) | |
初始濃度(mol/L) | 2.0 | 1.0 | 0 |
平衡濃度(mol/L) | c1 | c2 | 0.4 |
A. 10 min內,v(Cl2) = 0.04 mol/(L·min)
B. 當容器中Cl2為1.2 mol時,反應達到平衡
C. 若升高溫度(T1<T2)時,該反應平衡常數減小,則平衡時PCl3的![]()
D. 平衡后移走2.0 mol PCl3和1.0 molCl2,在相同條件下再達平衡時,c(PCl5)<0.2 mol/L
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關物質的用途中,運用了物質的化學性質的是
A. 用膠狀氫氧化鋁凝聚水中的懸浮物進行凈水
B. 用紅棕色氧化鐵制造紅色油漆
C. 氫氧化鋁作為醫用的胃酸中和劑
D. 用氧化鋁制造耐火坩堝和耐火管
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學反應2A(g)![]() B(g)+D(g)在四種不同條件下進行,B、D起始濃度為零,反應物A的濃度(mol/L)隨反應時間(min)的變化情況,根據下述數據,完成下列填空:
B(g)+D(g)在四種不同條件下進行,B、D起始濃度為零,反應物A的濃度(mol/L)隨反應時間(min)的變化情況,根據下述數據,完成下列填空:
實驗 序號 | 溫度/℃ | 時間/min | ||||||
0 | 10 | 20 | 30 | 40 | 50 | 60 | ||
1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
2 | 800℃ | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
3 | 800℃ | c 3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
(1)在實驗l過程中,10 min~20 min時間內用B表示該反應的平均化學反應速率為_________mol/(L·min)。
(2)在實驗2過程中,A的初始濃度c2=______mol/L,反應經20min就達到平衡,可推測實驗2中還隱含的條件是___________________________。
(3)設實驗3的化學反應速率為v3,實驗1的化學反應速率為v1,則v3_____v1,且c3________1.0 mol/L (填“<”、“>”或“=”)。
(4)比較實驗4和實驗l,可推測該反應是___________反應(填“吸熱”或“放熱”)。理由是______________________________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com